
Wetenschap
Wat is het verschil tussen een elektronenconfiguratie in de grondtoestand en een geëxciteerde configuratie?
De grondtoestand-elektronenconfiguratie van een atoom is de rangschikking van de elektronen in hun laagste energieniveaus, of orbitalen. Deze configuratie is het meest stabiel en heeft de laagste energie. De elektronenconfiguratie in de grondtoestand van helium is bijvoorbeeld 1s2, wat betekent dat beide elektronen zich in de 1s-orbitaal bevinden.
Opgewonden status-elektronenconfiguratie
Een elektronenconfiguratie in aangeslagen toestand is een rangschikking van de elektronen waarin een of meer elektronen zich op een hoger energieniveau bevinden dan in de grondtoestand. Deze configuratie is minder stabiel en heeft een hogere energie dan de grondtoestand. De elektronenconfiguratie van helium in de aangeslagen toestand is bijvoorbeeld 1s12s1, wat betekent dat een van zijn elektronen zich in de 1s-orbitaal bevindt en het andere elektron zich in de 2s-orbitaal bevindt.
Verschillen tussen elektronconfiguraties in grondtoestand en geëxciteerde toestand
De belangrijkste verschillen tussen elektronenconfiguraties in de grondtoestand en de geëxciteerde toestand zijn hun stabiliteit en energie. De grondtoestandconfiguratie is stabieler en heeft een lagere energie dan de aangeslagen toestandconfiguratie. Dit komt omdat de elektronen in de grondtoestand zich in hun laagste energieniveau bevinden, terwijl de elektronen in de aangeslagen toestand zich in een hoger energieniveau bevinden.
Een ander verschil tussen elektronenconfiguraties in de grondtoestand en de geëxciteerde toestand is hun reactiviteit. Atomen in aangeslagen toestanden zijn reactiever dan atomen in grondtoestanden. Dit komt omdat de elektronen in aangeslagen toestanden losser aan de kern zijn gebonden, waardoor de kans groter is dat ze reageren met andere atomen of moleculen.
Voorbeelden van elektronconfiguraties in grondtoestand en geëxciteerde toestand
De volgende tabel toont enkele voorbeelden van elektronenconfiguraties in de grondtoestand en aangeslagen toestand voor verschillende atomen:
| Atoom | Grondtoestand-elektronenconfiguratie | Opgewonden toestand elektronenconfiguratie |
|---|---|---|
| Helium | 1s2 | 1s12s1 |
| Lithium | 1s22s1 | 1s22p1 |
| Beryllium | 1s22s2 | 1s22p2 |
| Borium | 1s22s22p1 | 1s22p21s1 |
| Koolstof | 1s22s22p2 | 1s22p31s1 |
Conclusie
Elektronconfiguraties in de grondtoestand en de geëxciteerde toestand zijn twee belangrijke concepten in de atoomfysica. De grondtoestandconfiguratie is het meest stabiel en heeft de laagste energie, terwijl de aangeslagen toestandconfiguratie minder stabiel is en een hogere energie heeft. Atomen in aangeslagen toestanden zijn reactiever dan atomen in grondtoestanden.
 Aantrekkelijke bevinding suggereert waarom koeling bananenaroma's dempt
Aantrekkelijke bevinding suggereert waarom koeling bananenaroma's dempt Chemici gebruiken licht om biologisch actieve verbindingen te bouwen
Chemici gebruiken licht om biologisch actieve verbindingen te bouwen Synthese op het oppervlak van carbyne:een sp-gehybridiseerde lineaire koolstofallotroop
Synthese op het oppervlak van carbyne:een sp-gehybridiseerde lineaire koolstofallotroop  Onderzoekers turbochargeren waterstofbrandstofcellen met nieuw ionengeleidend copolymeer
Onderzoekers turbochargeren waterstofbrandstofcellen met nieuw ionengeleidend copolymeer Chemici ontwerpen mini-ecosystemen om de werking van medicijnen te testen
Chemici ontwerpen mini-ecosystemen om de werking van medicijnen te testen
 Is de wasachtige laag van een blad dikker dan de epidermis?
Is de wasachtige laag van een blad dikker dan de epidermis?  Koeienmest en micro-organismen gebruiken om luiers en maandverband te composteren
Koeienmest en micro-organismen gebruiken om luiers en maandverband te composteren  Is jouw boterham slecht voor het milieu?
Is jouw boterham slecht voor het milieu? Nieuw-Zeelands White Island zal waarschijnlijk opnieuw uitbarsten, maar een nieuw waarschuwingssysteem kan urenlang waarschuwen en levens redden
Nieuw-Zeelands White Island zal waarschijnlijk opnieuw uitbarsten, maar een nieuw waarschuwingssysteem kan urenlang waarschuwen en levens redden Financiële administratie is de sleutel voor mitigatiepaden
Financiële administratie is de sleutel voor mitigatiepaden
Hoofdlijnen
- Wetenschappers proberen oude slachtmethoden na te bootsen en leren hoe Neanderthalers vogels aten
- Hoe houdt de pH verband met de proliferatie van micro-organismen?
- De aandelen van Apple verzuren, die van Microsoft stijgen. Zeg wat?!
- Het is onthuld dat liefdeshormoon hartgenezende eigenschappen heeft
- De wilde ezel keert terug
- Kenia mannelijke leeuwen gezien in intieme daad; binding, deskundigen zeggen
- Studie:Hoe een intern organel verdubbelt
- Gedetailleerde kaart laat zien hoe virussen mensen infecteren
- Parasieten of niet? Transponeerbare elementen in fruitvliegjes
- Water efficiënter omzetten in waterstof

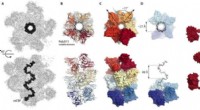
- Wetenschappers maken beelden van antilichamen die samenwerken tegen malaria
- Metaalzepen kritisch in snelheid van bederf van olieverfschilderijen

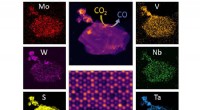
- Nieuwe 2D-legering combineert vijf metalen, breekt koolstofdioxide af
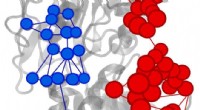
- Chemici vinden een nieuwe tool om enzymen te begrijpen:Google
 De drang naar giraal vervoer laat sommige rijders achter
De drang naar giraal vervoer laat sommige rijders achter Nieuwe manier om organische stof in de bodem te analyseren helpt klimaatverandering te voorspellen
Nieuwe manier om organische stof in de bodem te analyseren helpt klimaatverandering te voorspellen Brekende golven en vochttransport zorgen voor extreme neerslag
Brekende golven en vochttransport zorgen voor extreme neerslag Kernfusieproject bereikt halverwege bouwmijlpaal
Kernfusieproject bereikt halverwege bouwmijlpaal Onderzoek suggereert dat het eten van bonen in plaats van rundvlees de broeikasgassen sterk zou verminderen
Onderzoek suggereert dat het eten van bonen in plaats van rundvlees de broeikasgassen sterk zou verminderen Basisregels vaststellen voor nanotechnologisch onderzoek
Basisregels vaststellen voor nanotechnologisch onderzoek Wil je bondgenootschap aanmoedigen? Benadruk de waardering ervan, blijkt uit onderzoek
Wil je bondgenootschap aanmoedigen? Benadruk de waardering ervan, blijkt uit onderzoek  Bescherming van koraalriffen in een verslechterende omgeving
Bescherming van koraalriffen in een verslechterende omgeving
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

