
Wetenschap
Wat is de aard van een waterige oplossing van borax?
1. Basiciteit :Borax is een matig basisch zout. Wanneer het in water wordt opgelost, ondergaat het hydrolyse, wat resulteert in de afgifte van hydroxide-ionen (OH-) en de vorming van boorzuur (H3BO3). Deze fundamentele aard van borax kan worden toegeschreven aan de aanwezigheid van tetraboraationen (B4O7^2-), die kunnen reageren met water om hydroxide-ionen te produceren.
2. Buffercapaciteit :Borax fungeert als buffer in waterige oplossingen. Het kan helpen een relatief constante pH binnen een bepaald bereik te handhaven door te reageren met zuren of basen die aan de oplossing worden toegevoegd. De boraationen (B4O7^2-) en boorzuur (H3BO3) die in de oplossing aanwezig zijn, nemen deel aan bufferreacties om significante pH-veranderingen te minimaliseren.
3. Complexe formatie :Borax heeft het vermogen om complexe ionen te vormen met verschillende metaalionen. In waterige oplossingen kan het reageren met metaalionen om stabiele complexen te vormen, die het chemische gedrag en de eigenschappen van de metaalionen kunnen veranderen. Borax wordt bijvoorbeeld vaak gebruikt om complexen te vormen met overgangsmetaalionen, zoals koper en nikkel, en vindt toepassingen in de galvanisatie, de metallurgie en de analytische chemie.
4. Oplosbaarheid :Borax is matig oplosbaar in water. Bij kamertemperatuur (25°C) kan ongeveer 5,3 gram borax oplossen in 100 gram water. De oplosbaarheid ervan neemt toe bij stijgende temperatuur, waardoor de bereiding van meer geconcentreerde oplossingen mogelijk is.
5. Wateronthardende eigenschappen :Borax heeft waterverzachtende eigenschappen, waardoor het nuttig is in wasmiddelen en schoonmaakproducten. Het sekwestreert calcium- en magnesiumionen, die gewoonlijk verantwoordelijk zijn voor de hardheid van het water, waardoor wordt voorkomen dat ze onoplosbare neerslagen vormen en kalkaanslag veroorzaken in leidingen, apparaten en sanitaire voorzieningen.
Over het geheel genomen vertoont een waterige oplossing van borax basiciteit, bufferend vermogen, complexvorming, oplosbaarheid en wateronthardende eigenschappen, waardoor deze waardevol is in verschillende industriële, huishoudelijke en laboratoriumtoepassingen.
 Welke dieren hebben vleugels?
Welke dieren hebben vleugels?  Hoe klimaatverandering extreme weersomstandigheden over de hele wereld beïnvloedt:nieuwe studie
Hoe klimaatverandering extreme weersomstandigheden over de hele wereld beïnvloedt:nieuwe studie  Negatieve effecten van grondwater oppompen op oppervlaktewater vermijden
Negatieve effecten van grondwater oppompen op oppervlaktewater vermijden Investeringssleutel bij aanpassing aan klimaatverandering in West-Afrika
Investeringssleutel bij aanpassing aan klimaatverandering in West-Afrika Opnieuw gemengde mantel suggereert vroege start van platentektoniek
Opnieuw gemengde mantel suggereert vroege start van platentektoniek
Hoofdlijnen
- Orkaan legt duizenden zeeschildpadnesten bloot en spoelt ze weg
- Onderzoekers ontdekken hoe griepvirussen menselijke cellen kapen
- Getoonde chimpansees die spontaan om de beurt een cijferpuzzel oplossen
- Staat, FBI onderzoekt ziekte die ziek is, dode honden
- Hoe gewas- en diersensoren de landbouw slimmer maken
- Vergelijk en contrast kunstmatige en natuurlijke selectie
- Genotypes bepalen
- Bestaat er echt een ‘mama’-gen bij vrouwen?
- Hoe ziet het celmembraan eruit?
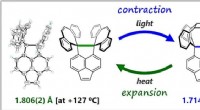
- Covalente koolstof-koolstofbindingen veel flexibeler dan verondersteld
- Eiwitten vormgeven om chaperonne-gerelateerde ziekten te begrijpen
- Video:Hoe effectief zijn stoffen maskers tegen het coronavirus?

- Nieuwe actieve ingrediënten uit de toolbox
- Ingenieurs laten zien hoe wolfraamoxide kan worden gebruikt als katalysator in duurzame chemische conversies

 Nieuw onderzoek volgt het lot van sterren die in de buurt van het centrale zwarte gat van de Melkweg leven
Nieuw onderzoek volgt het lot van sterren die in de buurt van het centrale zwarte gat van de Melkweg leven  Facebooks rattenvangende team bespioneert werknemers:rapport
Facebooks rattenvangende team bespioneert werknemers:rapport Als orkanen toeslaan, kunnen sociale media levens redden
Als orkanen toeslaan, kunnen sociale media levens redden Onderzoek naar eiwitassemblage toont aan dat moleculaire worp van de dobbelstenen winnende combinaties oplevert
Onderzoek naar eiwitassemblage toont aan dat moleculaire worp van de dobbelstenen winnende combinaties oplevert  Waarom husky’s blauwe ogen hebben
Waarom husky’s blauwe ogen hebben  Kleine nanokubussen helpen wetenschappers links van rechts te onderscheiden
Kleine nanokubussen helpen wetenschappers links van rechts te onderscheiden Hoe het betrouwbaarheidsinterval van de Mean
Hoe het betrouwbaarheidsinterval van de Mean Hoe bedrijven op uw zwakke punten azen:een vraag-en-antwoordsessie van Robert Shiller
Hoe bedrijven op uw zwakke punten azen:een vraag-en-antwoordsessie van Robert Shiller
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

