
Wetenschap
Hoe wordt een rubidium-85-atoom een rubidium-ion met 1 lading?
Specifiek in het geval van rubidium-85 heeft het in totaal 37 elektronen. In zijn neutrale toestand wordt het aantal positief geladen protonen in zijn kern in evenwicht gehouden door de 37 negatief geladen elektronen. Om een ion met 1 lading te worden, moet het één elektron verliezen, waardoor er 36 elektronen en 37 protonen overblijven. Omdat het aantal protonen nu het aantal elektronen met één overschrijdt, heeft het atoom een netto positieve lading van +1, waardoor het een rubidium-85-ion is.
Dit proces waarbij een elektron verloren gaat, is doorgaans het resultaat van chemische reacties of interacties met externe energiebronnen, zoals warmte of licht, die voldoende energie leveren om de aantrekkingskracht tussen het elektron en de positief geladen kern te overwinnen.
 Op de natuur gebaseerde oplossingen kunnen $ 50 miljard aan schade door overstromingen aan de Golfkust voorkomen
Op de natuur gebaseerde oplossingen kunnen $ 50 miljard aan schade door overstromingen aan de Golfkust voorkomen Verwoest Venetië zet zich schrap voor derde grote overstroming
Verwoest Venetië zet zich schrap voor derde grote overstroming Staalsnippers zijn veelbelovend bij het verwijderen van E. coli uit regenwater
Staalsnippers zijn veelbelovend bij het verwijderen van E. coli uit regenwater Meer dan twintig watersystemen in Colorado overschrijden de nieuwe EPA-limieten voor forever-chemicaliën
Meer dan twintig watersystemen in Colorado overschrijden de nieuwe EPA-limieten voor forever-chemicaliën  Convectie-experimenten voor kinderen
Convectie-experimenten voor kinderen
Hoofdlijnen
- Wat doodde Knut de ijsbeer? Studie biedt 'afsluiting'
- Hoe microplastics in de mariene atmosfeer terechtkomen
- Een betere manier om RNA-virusnaalden te vinden in hooibergen van databases
- Wat irriteert een chimpansee?
- Vraag ons allesWelke van de volgende is een voorbeeld van Arrhenius-zuur?
- Onderzoekers ontdekken hoe wormen kennis over een ziekteverwekker doorgeven aan hun nakomelingen
- Inheemse vissoorten lopen gevaar na verwijdering van water uit de Colorado-rivier
- Wat is de rol van enzymen in het metabolisme?
- Soorten monomeren
- De dood maakt complexiteit in chemische evolutie mogelijk

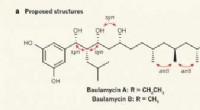
- Chemici leiden de juiste structuur af van de A- en B-baulamycinen
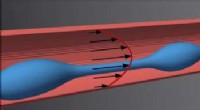
- Natuurkundigen ontdekken mechanisme voor vorming van bloedplaatjes
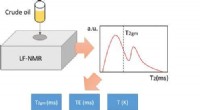
- Kunstmatige intelligentie heeft geleerd om olieviscositeit in te schatten
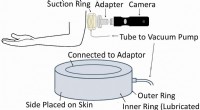
- Nieuw apparaat kan littekens bij cosmetische chirurgie helpen verminderen
 Wat is ultrasone mindcontrol?
Wat is ultrasone mindcontrol?  Hoelang blijft een vlinder in een pop?
Hoelang blijft een vlinder in een pop?  "How to Use a Centrifuge
"How to Use a Centrifuge Magnetron kookt materiaal van zonnecellen
Magnetron kookt materiaal van zonnecellen Op fosfor gebaseerde composieten als anodematerialen voor kalium-ionbatterijen
Op fosfor gebaseerde composieten als anodematerialen voor kalium-ionbatterijen Met metaaloxide doordrenkte membranen kunnen een energiezuinig alternatief bieden voor chemische scheidingen
Met metaaloxide doordrenkte membranen kunnen een energiezuinig alternatief bieden voor chemische scheidingen Uit onderzoek blijkt hoe Rembrandt baanbrekend werk verrichtte met het impregneren van canvas op loodbasis voor De Nachtwacht
Uit onderzoek blijkt hoe Rembrandt baanbrekend werk verrichtte met het impregneren van canvas op loodbasis voor De Nachtwacht  Onze toekomstige luchttaxi? Vahana zelfvliegende machine stijgt op, zweeft, landt
Onze toekomstige luchttaxi? Vahana zelfvliegende machine stijgt op, zweeft, landt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

