
Wetenschap
Welke informatie geeft een evenwichtsconstante over een reactie?
1. Omvang van de reactie:
De grootte van de evenwichtsconstante geeft aan in hoeverre de reactie onder bepaalde omstandigheden verloopt. Een grote evenwichtsconstante (Keq>> 1) suggereert dat de reactie voornamelijk in de richting van de producten verloopt, wat wijst op een hoge omzetting van reactanten in producten bij evenwicht. Omgekeerd geeft een kleine evenwichtsconstante (Keq <<1) aan dat de reactie de reactanten bevoordeelt, en dat er een beperkte conversie naar producten plaatsvindt.
2. Evenwichtspositie:
De evenwichtsconstante geeft inzicht in de evenwichtsstand. Als Keq groter is dan 1, worden de producten bij voorkeur bij evenwicht gevormd en ligt de reactie ver naar rechts (productbegunstigd). Als Keq kleiner is dan 1, zijn de reactanten bij evenwicht in hogere concentraties aanwezig en ligt de reactie ver naar links (reactant-favoriet).
3. Relatieve concentraties van reactanten en producten:
Met de evenwichtsconstante kunnen we de relatieve concentraties van reactanten en producten in evenwicht voorspellen. Voor een reactie met de algemene vergelijking:
aA + bB ⇌ cC + dD
de evenwichtsconstante-uitdrukking wordt gegeven door:
Keq =[C]^c[D]^d/[A]^a[B]^b
waarbij [A], [B], [C] en [D] de evenwichtsconcentraties van de respectieve soort vertegenwoordigen. Door de evenwichtsconstante te kennen, kunnen we de relatieve concentraties van deze soorten bij evenwicht berekenen, gegeven de initiële concentraties.
4. Veranderingen in evenwichtspositie:
De evenwichtsconstante kan worden gebruikt om de verschuiving in de evenwichtspositie te voorspellen wanneer de reactieomstandigheden veranderen. Als de concentratie van een van de reactanten of producten wordt veranderd, zal de reactie verschuiven om het evenwicht te herstellen. De richting van deze verschuiving kan worden voorspeld op basis van de veranderingen in de concentratie van de soort en de grootte van de evenwichtsconstante.
5. Het voorspellen van de producten van een reactie:
In sommige gevallen kan de evenwichtsconstante helpen bij het voorspellen van de producten van een reactie. Voor reacties met meerdere mogelijke producten is het product met de hoogste evenwichtsconstante voor vorming waarschijnlijk het belangrijkste product.
6. Spontaniteit van een reactie:
De evenwichtsconstante houdt verband met de spontaniteit van een reactie bij constante temperatuur. Voor reacties bij evenwicht is de Gibbs-vrije energieverandering (AG) nul. Wanneer Keq groter is dan 1, is ΔG negatief, wat aangeeft dat de reactie spontaan is. Omgekeerd, wanneer Keq kleiner is dan 1, is AG positief, wat aangeeft dat de omgekeerde reactie spontaan is.
Samenvattend biedt de evenwichtsconstante waardevolle inzichten in de omvang van een reactie, de evenwichtspositie, de relatieve concentraties van reactanten en producten, veranderingen in de evenwichtspositie, de voorspelling van producten en de spontaniteit van een reactie onder gespecificeerde omstandigheden.
 Nieuwe chemische mechanismen geïdentificeerd op weg naar schoner, efficiëntere verbranding
Nieuwe chemische mechanismen geïdentificeerd op weg naar schoner, efficiëntere verbranding Wat voor soort materie wordt gevormd wanneer atomen twee of meer elementen binden?
Wat voor soort materie wordt gevormd wanneer atomen twee of meer elementen binden?  DNA-enzym schudt celmembranen duizend keer sneller dan zijn natuurlijke tegenhanger
DNA-enzym schudt celmembranen duizend keer sneller dan zijn natuurlijke tegenhanger Werkende eiwitten maken goed gebruik van frustratie
Werkende eiwitten maken goed gebruik van frustratie Waarom vast natriumchloride geleiden?
Waarom vast natriumchloride geleiden?
 Milieugroep plant nieuwe Nederlandse juridische stappen voor schone lucht
Milieugroep plant nieuwe Nederlandse juridische stappen voor schone lucht Wat een mislukt Johannesburg-project ons vertelt over megasteden in Afrika
Wat een mislukt Johannesburg-project ons vertelt over megasteden in Afrika Massa's kraaien verspreiden zich C. jejuni:zijn mensen kwetsbaar?
Massa's kraaien verspreiden zich C. jejuni:zijn mensen kwetsbaar?  Alternatieve getijdenmoerassen die duidelijk zichtbaar zijn, hebben Blue Carbon-supersterren over het hoofd gezien
Alternatieve getijdenmoerassen die duidelijk zichtbaar zijn, hebben Blue Carbon-supersterren over het hoofd gezien  NASA vindt extreme regenval in tropische cycloon Kenanga
NASA vindt extreme regenval in tropische cycloon Kenanga
Hoofdlijnen
- Hoe de genoomdiversiteit van belangrijke gewassen hun evolutie vertelt
- Roept op tot regelgevende maatregelen om de openbaarmaking van biodiversiteit te versterken
- Wetenschappers publiceren nieuw onderzoek naar hoe individuele cellen reageren op virale infecties
- Scheve vissen laten zien dat symmetrie slechts oppervlakkig is
- Hoe toxoplasmose immuuncellen uitbuit om de hersenen te bereiken?
- CRISPR-octrooioorlogen benadrukken het probleem van het verlenen van brede intellectuele eigendomsrechten voor technologie die publieke voordelen biedt
- Onderzoek naar de rol van methylering bij vernalisatie en fotoperiode-route:een potentiële bloeiregulator?
- Onderzoek wijst uit hoe de identiteit van huidcellen kan worden gedemonteerd om stamcellen te creëren
- Moleculaire atlas laat zien hoe hersencellen zich ontwikkelen
- Eenvoudig apparaat bewaakt de gezondheid met behulp van zweet

- Bioluminescente worm met ijzeren superkrachten

- Een efficiëntere manier om hangende olefinen te splitsen van terpenen en soortgelijke verbindingen
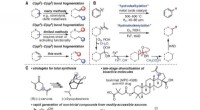
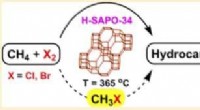
- De voetafdruk verkleinen van een broeikasgas dat krachtiger is dan koolstofdioxide
- Metamaterialen bieden multifunctionele materialen voor engineering

 Eens waren voorbij het stadium van angst, waar leggen we de schuld voor de COVID-19 pandemie?
Eens waren voorbij het stadium van angst, waar leggen we de schuld voor de COVID-19 pandemie? Wat is de pOH van een oplossing met een OH-waarde van 9,31 x 10-2 M?
Wat is de pOH van een oplossing met een OH-waarde van 9,31 x 10-2 M?  Leger ingeschakeld om door droogte getroffen Nieuw-Zeelandse steden te helpen
Leger ingeschakeld om door droogte getroffen Nieuw-Zeelandse steden te helpen Lokaal opgewekte stroom kan het antwoord zijn voor kwetsbaar energienet
Lokaal opgewekte stroom kan het antwoord zijn voor kwetsbaar energienet Wat is de pH van mierenzuur?
Wat is de pH van mierenzuur?  Chemie gebruiken om het verschil tussen koude en warme koffie te ontdekken
Chemie gebruiken om het verschil tussen koude en warme koffie te ontdekken Een op de 20 werknemers heeft een nutteloze baan – veel minder dan eerder werd gedacht
Een op de 20 werknemers heeft een nutteloze baan – veel minder dan eerder werd gedacht Switch-in-a-cell elektriseert het leven
Switch-in-a-cell elektriseert het leven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

