
Wetenschap
Waarom vast natriumchloride geleiden?
Natriumchloride in vaste toestand geleidt geen elektriciteit omdat de ionen stijf in hun roosterposities worden gehouden. De elektronen zijn niet vrij om te bewegen en lading te dragen, dus er is geen stroom.
Wanneer natriumchloride in water wordt opgelost, omringen de watermoleculen de ionen en scheiden ze van elkaar. Dit proces wordt ionisatie genoemd. De ionen kunnen zich dan vrij in het water bewegen en kunnen lading dragen. Hierdoor kan er stroom vloeien en wordt gezegd dat de oplossing een elektrolyt is.
De geleidbaarheid van een oplossing hangt af van de concentratie van de elektrolyt. Hoe geconcentreerder de oplossing, hoe meer ionen er zijn om lading te dragen, en hoe hoger de geleidbaarheid.
 Welke chemische stof of welk element heeft het grootste aantal moleculen in een evenwichtige vergelijking?
Welke chemische stof of welk element heeft het grootste aantal moleculen in een evenwichtige vergelijking?  Moderne simulaties kunnen MRI's verbeteren
Moderne simulaties kunnen MRI's verbeteren Gemultiplexte biosensoren in het voordeel van de gezondheidszorg
Gemultiplexte biosensoren in het voordeel van de gezondheidszorg Meerlagige fabricage op wafelschaal van micro-elektronica op basis van zijdefibroïne
Meerlagige fabricage op wafelschaal van micro-elektronica op basis van zijdefibroïne Zijn methylkationen stabieler dan ethylkationen?
Zijn methylkationen stabieler dan ethylkationen?
 Te gek? Water verplaatsen van overstroming naar droogte
Te gek? Water verplaatsen van overstroming naar droogte  Voor selenium in rivieren, timing is belangrijk
Voor selenium in rivieren, timing is belangrijk Globale analyse identificeert risicobossen
Globale analyse identificeert risicobossen Bewaarde pinguïnpoep onthult eerdere veranderingen in de circulatie in de Antarctische Oceaan
Bewaarde pinguïnpoep onthult eerdere veranderingen in de circulatie in de Antarctische Oceaan Mijnafvaldammen bedreigen het milieu, zelfs als ze niet falen
Mijnafvaldammen bedreigen het milieu, zelfs als ze niet falen
Hoofdlijnen
- Sectie van DNA of RNA dat niet codeert voor eiwitten
- Hoe het genoom is verpakt in chromosomen die tijdens de celdeling getrouw kunnen worden verplaatst
- Milieu op basis van evolutie indelen in twee categorieën?
- Onderzoekers ontdekken de onverwachte atomaire structuur van koude- en mentholsensor TRPM8
- Welke van de volgende DNA-strengen is een complementaire streng voor C-C-A-T-C-G A. G-G-T-A-G-C C. A-A-C-G-A-T B. G-G-A-T-G-C D. T-T-G-C-T-A?
- Hoe lepra werkt
- Onderwaterzweefvliegtuigen kunnen de manier veranderen waarop wetenschappers vissen volgen
- Wat concludeerde Thomas Hunt Morgan over de chromosomen van de fruitvlieg?
- Onderzoekers willen weten waarom beluga-walvissen nog niet zijn hersteld
- Nieuwe beeldvormingsmethode helpt bij waterzuivering

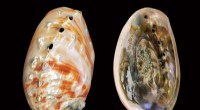
- Techniek onthult diepere inzichten in de samenstelling van parelmoer, een natuurlijk materiaal
- Zwak gebonden zout is een belangrijk ingrediënt voor zeer zuivere Li@C60-film

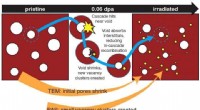
- Niet-destructieve positronenstralen sondeschade, ondersteuning van vooruitgang op het gebied van veiligheid in stralingsomgevingen
- Synthetische brandstoffen kunnen de ecologische voetafdruk verkleinen

 Hoe houd je ruimtepakondergoed schoon?
Hoe houd je ruimtepakondergoed schoon? Nieuwe ontdekking is groot op nanoschaal
Nieuwe ontdekking is groot op nanoschaal Zonnepark in Kings Park om 1 van stroom te voorzien 000 woningen
Zonnepark in Kings Park om 1 van stroom te voorzien 000 woningen Hoe te bepalen of een atoom polair of niet-polair is?
Hoe te bepalen of een atoom polair of niet-polair is?  Afbeelding:berg Fuji, Japan
Afbeelding:berg Fuji, Japan Wat zijn uw gegevens waard voor Big Tech? Bill zou een antwoord afdwingen
Wat zijn uw gegevens waard voor Big Tech? Bill zou een antwoord afdwingen Pentagon stopt verkoop van in China gemaakte smartphones als veiligheidsrisico
Pentagon stopt verkoop van in China gemaakte smartphones als veiligheidsrisico Wetenschappers ontdekken driedimensionale structuur in kleinere waterdruppels
Wetenschappers ontdekken driedimensionale structuur in kleinere waterdruppels
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

