
Wetenschap
Hoe worden ionische verbindingen geïdentificeerd?
- Formule . De formule van een ionische verbinding bestaat uit de symbolen van de samenstellende ionen, geschreven in de eenvoudigste gehele getalsverhouding van positieve tot negatieve ladingen. De formule van natriumchloride is bijvoorbeeld NaCl, wat aangeeft dat de verbinding één natriumion (Na+) en één chloride-ion (Cl-) bevat.
- Oplosbaarheid . Ionische verbindingen zijn doorgaans oplosbaar in polaire oplosmiddelen, zoals water. Dit komt omdat de polaire oplosmiddelmoleculen de ionen kunnen solvateren, ze van elkaar kunnen breken en ze kunnen oplossen. Daarentegen zijn ionische verbindingen over het algemeen onoplosbaar in niet-polaire oplosmiddelen, zoals hexaan.
- Elektrische geleidbaarheid . Ionische verbindingen in gesmolten toestand of opgelost in water zijn goede elektriciteitsgeleiders. Dit komt omdat de ionen vrij kunnen bewegen en de elektrische stroom kunnen transporteren. Daarentegen zijn ionische verbindingen in vaste vorm over het algemeen slechte geleiders van elektriciteit.
- Kristalstructuur . Ionische verbindingen vormen doorgaans een kristalrooster, waarin de positieve en negatieve ionen in een regelmatig, herhalend patroon zijn gerangschikt. Deze kristalstructuur geeft ionische verbindingen hun karakteristieke eigenschappen, zoals hardheid en hoog smeltpunt.
- Chemische eigenschappen :
* Ionische verbindingen reageren over het algemeen met water en vormen een zure of basische oplossing. Natriumchloride reageert bijvoorbeeld met water om een neutrale oplossing te vormen, natriumhydroxide reageert met water om een basische oplossing te vormen en zoutzuur reageert met water om een zure oplossing te vormen.
* Ionische verbindingen reageren over het algemeen met metalen om nieuwe verbindingen te vormen. Natriumchloride reageert bijvoorbeeld met ijzer en vormt ijzer(II)chloride en natriummetaal.
- Fysieke eigenschappen :
* Ionische verbindingen zijn doorgaans harde en broze vaste stoffen.
* Ionische verbindingen hebben hoge smelt- en kookpunten.
* Ionische verbindingen zijn doorgaans oplosbaar in water en andere polaire oplosmiddelen.
* Ionische verbindingen kunnen elektriciteit geleiden wanneer ze in water worden opgelost of gesmolten.
Door rekening te houden met de hierboven genoemde eigenschappen is het meestal mogelijk om vast te stellen of een bepaalde stof een ionische verbinding is.
 Studie vindt manieren om verborgen gevaren van geaccumuleerde spanningen op zeegras te vermijden
Studie vindt manieren om verborgen gevaren van geaccumuleerde spanningen op zeegras te vermijden Onderzoekers pakken de dringende noodzaak aan om soorten te identificeren die het meest worden bedreigd door klimaatverandering
Onderzoekers pakken de dringende noodzaak aan om soorten te identificeren die het meest worden bedreigd door klimaatverandering China ziet vier olievlekken van gezonken tanker
China ziet vier olievlekken van gezonken tanker Studie analyseert de impact van koolstofdioxide op het klimaat op aarde 30 miljoen jaar geleden
Studie analyseert de impact van koolstofdioxide op het klimaat op aarde 30 miljoen jaar geleden Nieuw bewijs suggereert dat het materie was die werd uitgestoten uit de Chicxulub-krater die leidde tot de impact op de winter
Nieuw bewijs suggereert dat het materie was die werd uitgestoten uit de Chicxulub-krater die leidde tot de impact op de winter
Hoofdlijnen
- Wat is een geest? Onderzoeker daagt percepties van gevoel uit met de kleinste wezens
- Twee artikelen beschrijven hoe een membraaneiwit zowel lipiden als ionen kan verplaatsen
- Wat zit er eigenlijk in vapes? We hebben ze uit elkaar gehaald om erachter te komen
- Mesozoïsche zoogdieren:wat weten we van China?
- De variabiliteit van het dagelijks leven heeft mogelijk minstens evenveel invloed op de evolutie gehad als zeldzame activiteiten zoals de jacht op groot wild
- Stadsuitbreiding in Perth die het seksleven van planten beïnvloedt
- Vijf belangrijke orgaansystemen van het lichaam
- Watervlooien als kanaries in een kolenmijn bieden de sleutel tot het beheersen van chemische vervuiling
- Hoe het griepvirus onze cellen hackt
- Onderzoekers bestudeerden de fabricage van polymere vezels voor gebruik in geavanceerde gezondheidszorg

- Ongrijpbare verbindingen van broeikasgas geïsoleerd

- Chemici ontwikkelen een raamwerk om een efficiënte synthese van informatierijke moleculen mogelijk te maken
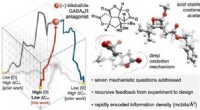
- Zullen cyborgs gemaakt worden van melanine? Pigmentdoorbraak maakt biocompatibele elektronica mogelijk
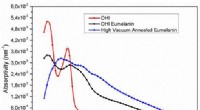
- Energieopslagmaterialen opgebouwd uit moleculaire blokken van nanoformaat
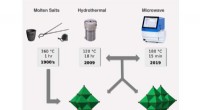
 China bereidt zich voor op lancering raket met ruimtestationbenodigdheden
China bereidt zich voor op lancering raket met ruimtestationbenodigdheden Het lichtste elektromagnetische afschermingsmateriaal ter wereld
Het lichtste elektromagnetische afschermingsmateriaal ter wereld als een lithiumkern 3 protonen en 4 neutronen bevat. Wat is de atoommassa?
als een lithiumkern 3 protonen en 4 neutronen bevat. Wat is de atoommassa?  Nanomoleculaire origami-dozen zijn veelbelovend voor energieopslag
Nanomoleculaire origami-dozen zijn veelbelovend voor energieopslag Gebruik van glaskeramiek in kaslampen faciliteert plantengroei
Gebruik van glaskeramiek in kaslampen faciliteert plantengroei Hoe kunnen bedrijven consumenten aanspreken die afkerig zijn van producten die gebruik maken van een nieuwe technologie?
Hoe kunnen bedrijven consumenten aanspreken die afkerig zijn van producten die gebruik maken van een nieuwe technologie?  Wakker worden:wat gebeurt er als marketingcommunicatie niet overeenkomt met de bedrijfspraktijk?
Wakker worden:wat gebeurt er als marketingcommunicatie niet overeenkomt met de bedrijfspraktijk? Grams converteren naar AMU
Grams converteren naar AMU
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

