
Wetenschap
Wat betekent het als een chemische of fysische eigenschap periodiek is?
De periodiciteit van chemische en fysische eigenschappen is een fundamenteel concept in de scheikunde, omdat wetenschappers hierdoor de eigenschappen van elementen kunnen voorspellen op basis van hun positie in het periodiek systeem. Enkele van de eigenschappen die periodiciteit vertonen, zijn onder meer:
1. Atoomstraal:De atoomstraal neemt over het algemeen af over een periode (van links naar rechts) en neemt toe in een groep (van boven naar beneden). Dit komt door de toenemende nucleaire lading over een bepaalde periode, waardoor de elektronen dichter bij de kern worden getrokken, en door de toevoeging van nieuwe elektronenschillen in een groep.
2. Ionisatie-energie:Ionisatie-energie, de energie die nodig is om een elektron uit een atoom te verwijderen, neemt over het algemeen toe over een periode en neemt af in een groep. Deze trend wordt voornamelijk beïnvloed door de toenemende nucleaire lading, waardoor het moeilijker wordt om elektronen over een bepaalde periode te verwijderen, en de extra elektronenschillen in een groep, waardoor het gemakkelijker wordt om elektronen te verwijderen.
3. Elektronegativiteit:Elektronegativiteit, het vermogen van een atoom om elektronen naar zichzelf toe te trekken, neemt over het algemeen over een bepaalde periode toe en neemt af in een groep. Dit komt omdat de toenemende nucleaire lading over een periode elektronen dichter bij de kern trekt, wat resulteert in een sterkere aantrekkingskracht voor elektronen, terwijl de extra elektronenschillen in een groep de effectieve nucleaire lading verminderen die door de valentie-elektronen wordt ervaren.
4. Reactiviteit:De reactiviteit van elementen neemt over het algemeen toe binnen een groep en neemt af over een periode. Deze trend houdt vaak verband met het gemak waarmee elektronen verloren of gewonnen kunnen worden. Metalen (aan de linkerkant van het periodiek systeem) zijn bijvoorbeeld doorgaans reactiever omdat ze gemakkelijk elektronen kunnen verliezen, terwijl niet-metalen (aan de rechterkant) doorgaans minder reactief zijn omdat ze een sterke aantrekkingskracht op elektronen hebben.
De periodiciteit van chemische en fysische eigenschappen biedt waardevolle inzichten in het gedrag van elementen en stelt wetenschappers in staat voorspellingen te doen over de eigenschappen van nieuw ontdekte elementen of elementen die nog niet zijn gesynthetiseerd.
 Katalytische koppelingen begrijpen:niet alle synergieën zijn eenvoudig
Katalytische koppelingen begrijpen:niet alle synergieën zijn eenvoudig Waarom geleiden moleculaire verbindingen geen elektriciteit?
Waarom geleiden moleculaire verbindingen geen elektriciteit?  Kan waterstof een elektron verliezen en een ion vormen?
Kan waterstof een elektron verliezen en een ion vormen?  Nieuwe methode helpt de omkeerbaarheid en onomkeerbaarheid van praktische Li-metaalbatterijen te kwantificeren
Nieuwe methode helpt de omkeerbaarheid en onomkeerbaarheid van praktische Li-metaalbatterijen te kwantificeren Waar worden metalen voor gebruikt en waarom?
Waar worden metalen voor gebruikt en waarom?
Hoofdlijnen
- Waar bestaat de cel uit?
- Twee Caribische vogelvangbomen vernoemd naar twee vrouwen met over het hoofd gezien botanische werken
- Welke groep organismen heeft volgens het fossielenbestand het langst bestaan:buikpotigen, koralen, zoogdieren of vaatplanten?
- Bioloog uit Syracuse onthult hoe walvissen kunnen 'zingen' voor hun avondeten
- Waarom mensen op politici stemmen waarvan ze weten dat het leugenaars zijn
- Welk voorbeeld betreft een celmembraan dat berichten ontvangt?
- Kleine eiwitten spelen grote rol in cellulaire energiebalans
- Hoe maak je een MRI van je draak:onderzoekers ontwikkelen de eerste hersenatlas van de baardagaam
- Nieuw model helpt verklaren hoe voorzieningen ziekten in het wild bevorderen of verminderen
- Efficiënte elektrokatalytische reductie van nitraat tot stikstof:veelbelovende manier om stikstof uit water te verwijderen

- Onderzoekers ontsluiten kankerverwekkend mechanisme van E. coli-toxine met synthetische biologie

- Nieuw systeem maakt snel, antibioticabehandelingen op maat mogelijk

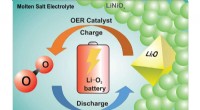
- Chemici maken doorbraak op weg naar het maken van een oplaadbare lithium-zuurstofbatterij
- Doorbraakmateriaal kan leiden tot goedkopere, meer wijdverbreide zonnepanelen en elektronica

 Onderzoekers demonstreren 3D optisch schijfgeheugen op nanoschaal met petabit-capaciteit
Onderzoekers demonstreren 3D optisch schijfgeheugen op nanoschaal met petabit-capaciteit  Veranderende ecosystemen in Beieren
Veranderende ecosystemen in Beieren De oude reuzen van Yosemite, onder een miljard sterren
De oude reuzen van Yosemite, onder een miljard sterren Onderzoeker vindt op gegevens gebaseerd bewijs over politiezorg tussen krijgers en voogden
Onderzoeker vindt op gegevens gebaseerd bewijs over politiezorg tussen krijgers en voogden Natuurkundigen ontrafelen mysterie van stabiele fullerenen
Natuurkundigen ontrafelen mysterie van stabiele fullerenen Onderzoekers synthetiseren hernieuwbare oliën voor gebruik in smeermiddelen
Onderzoekers synthetiseren hernieuwbare oliën voor gebruik in smeermiddelen Infrarood NASA-beelden tonen versterking van tropische storm Soulik
Infrarood NASA-beelden tonen versterking van tropische storm Soulik Tienden van een pond omrekenen naar Ounces
Tienden van een pond omrekenen naar Ounces
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

