
Wetenschap
Hoe bereken je de molariteit van kaliumjodaat bij redoxtitratie?
1. Standaardiseer de natriumthiosulfaatoplossing. Dit wordt gedaan door een bekende hoeveelheid kaliumjodaat te laten reageren met een bekende hoeveelheid natriumthiosulfaat. Het eindpunt van de reactie wordt bereikt wanneer de oplossing kleurloos wordt.
2. Bereken de molariteit van de natriumthiosulfaatoplossing. Gebruik de volgende formule:
```
Molariteit van natriumthiosulfaat =mol kaliumjodaat / liter natriumthiosulfaat
```
3. Reageer de kaliumjodaatoplossing met een bekende hoeveelheid natriumthiosulfaatoplossing. Het eindpunt van de reactie wordt bereikt wanneer de oplossing kleurloos wordt.
4. Bereken het aantal mol kaliumjodaat in de reactie. Gebruik de volgende formule:
```
Mol kaliumjodaat =liter natriumthiosulfaat * molariteit natriumthiosulfaat
```
5. Bereken de molariteit van de kaliumjodaatoplossing. Gebruik de volgende formule:
```
Molariteit van kaliumjodaat =mol kaliumjodaat / liter kaliumjodaat
```
Hier is een voorbeeld van hoe u de molariteit van kaliumjodaat bij redoxtitratie kunt berekenen:
1. Standaardiseer de natriumthiosulfaatoplossing:
- Los 0,1000 g kaliumjodaat op in 100 ml water.
- Voeg 50 ml 6 M zwavelzuur toe.
- Voeg 1 g kaliumjodide toe.
- Titreer de oplossing met 0,1 M natriumthiosulfaatoplossing totdat de oplossing kleurloos wordt. Het eindpunt van de reactie wordt bereikt nadat 15,00 ml natriumthiosulfaatoplossing is toegevoegd.
2. Bereken de molariteit van de natriumthiosulfaatoplossing:
```
Molariteit van natriumthiosulfaat =(0,1000 g / 214,01 g/mol) =0,0004612 M
```
3. Laat de kaliumjodaatoplossing reageren met een bekende hoeveelheid natriumthiosulfaatoplossing:
- Pipetteer 50 ml van de kaliumjodaatoplossing in een kolf.
- Voeg 50 ml 6 M zwavelzuur toe.
- Voeg 1 g kaliumjodide toe.
- Titreer de oplossing met 0,1 M natriumthiosulfaatoplossing totdat de oplossing kleurloos wordt. Het eindpunt van de reactie wordt bereikt nadat 25,00 ml natriumthiosulfaatoplossing is toegevoegd.
4. Bereken het aantal mol kaliumjodaat in de reactie:
```
Mol kaliumjodaat =25,00 ml * 0,0004612 M
=0,001153 mol
```
5. Bereken de molariteit van de kaliumjodaatoplossing:
```
Molariteit van kaliumjodaat =0,001153 mol/0,0500 L =0,02306 M
```
Daarom is de molariteit van de kaliumjodaatoplossing 0,02306 M.
 Is een zwak zuur vergelijkbaar met verdund zuur?
Is een zwak zuur vergelijkbaar met verdund zuur?  Experimenteel vaccin maakt de dodelijkste synthetische opioïden bot
Experimenteel vaccin maakt de dodelijkste synthetische opioïden bot Wat is het veranderen van een vloeistof in een gas aan de oppervlaktevloeistof?
Wat is het veranderen van een vloeistof in een gas aan de oppervlaktevloeistof?  Membraanloze protocellen kunnen aanwijzingen geven voor de vorming van het vroege leven
Membraanloze protocellen kunnen aanwijzingen geven voor de vorming van het vroege leven Een ongebruikelijke vorm van antibioticaresistentie bij pandemische cholera
Een ongebruikelijke vorm van antibioticaresistentie bij pandemische cholera
 Bedreigde planten in Maleisië
Bedreigde planten in Maleisië Vergelijkend onderzoek naar veerkrachtgerelateerd beleid en lokale praktijken in vijf steden wereldwijd
Vergelijkend onderzoek naar veerkrachtgerelateerd beleid en lokale praktijken in vijf steden wereldwijd  Kosten van klimaatrampen bereiken de helft van de Amerikaanse groei in tien jaar:rapport
Kosten van klimaatrampen bereiken de helft van de Amerikaanse groei in tien jaar:rapport Geavanceerde kennis en nieuwe technologieën in gashydraatonderzoek
Geavanceerde kennis en nieuwe technologieën in gashydraatonderzoek Wat is een goede wetenschappelijke zin voor biosfeer?
Wat is een goede wetenschappelijke zin voor biosfeer?
Hoofdlijnen
- Nieuwe beeldvormingsbenadering visualiseert hoe het uitoefenen van kracht op eiwitten complexe formaties verandert
- Wat is de fusie van twee gameten om een diploïde zygoot te vormen?
- Ezels hebben meer bescherming nodig tegen de winter dan paarden
- Onderzoekers laten voor het eerst bewuste processen zien in de hersenen van vogels
- Fenotype: definitie, types, voorbeelden
- Nieuwsgierige grote witte haai speelt met camera
- De hectische 24-uurs inspanning om een bedreigde, verweesde vleermuis
- Hoe u uw hersenen kunt stimuleren
- Genontdekking kan wereldwijde tarwe-epidemie stoppen
- Snel en furieus:nieuwe klasse van 2D-materialen slaat elektrische energie op
- Evolutie hacken, screeningstechniek kan het meest wijdverbreide enzym verbeteren

- Neurowetenschappers ontdekken nieuwe structuur van belangrijk eiwit in de hersenen
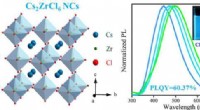
- Wetenschappers synthetiseren loodvrije op zirkonium gebaseerde vacature-geordende dubbele perovskiet nanokristallen
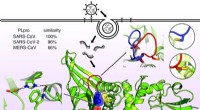
- Informatie over de moleculaire vorm van virussen die COVID-19 veroorzaken, SARS, en MERS onthult structurele overeenkomsten
 Nepnieuws maakt ziekte-uitbraken erger, uit onderzoek blijkt
Nepnieuws maakt ziekte-uitbraken erger, uit onderzoek blijkt Hoe controleren zwemmers hun borstcrawl-zwemsnelheid?
Hoe controleren zwemmers hun borstcrawl-zwemsnelheid? Geoptimaliseerde directionele polarisatiecamera helpt terrestrische ecosysteem koolstofmonitoring
Geoptimaliseerde directionele polarisatiecamera helpt terrestrische ecosysteem koolstofmonitoring TossingBot kan objecten pakken en in gespecificeerde bakken gooien
TossingBot kan objecten pakken en in gespecificeerde bakken gooien Wetenschappers vinden nieuwe conclusies over hoe sauropodeklauwen werden gebruikt
Wetenschappers vinden nieuwe conclusies over hoe sauropodeklauwen werden gebruikt  Effecten van een belangrijk medicijndoelwit gereguleerd door moleculaire codes
Effecten van een belangrijk medicijndoelwit gereguleerd door moleculaire codes Ondanks lagere zwavelemissies in de VS en West-Europa, luchtvervuiling daalt langzamer
Ondanks lagere zwavelemissies in de VS en West-Europa, luchtvervuiling daalt langzamer Afbeelding:NGC 6818 in het sterrenbeeld Boogschutter
Afbeelding:NGC 6818 in het sterrenbeeld Boogschutter
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

