
Wetenschap
Welke ionen ontstaan er als ammoniak oplost in water?
De ionisatie van ammoniak in water kan worden weergegeven door de volgende chemische vergelijking:
NH3 + H2O ⇌ NH4+ + OH-
Bij deze reactie accepteert een ammoniakmolecuul (NH3) een waterstofion (H+) van een watermolecuul (H2O), waardoor een ammoniumion (NH4+) wordt gevormd. Tegelijkertijd geeft het watermolecuul dat het waterstofion afstaat een hydroxide-ion (OH-) af.
De evenwichtsconstante (Kb) voor de ionisatie van ammoniak in water bij kamertemperatuur (25°C) is ongeveer 1,8 x 10-5. Dit geeft aan dat de ionisatie van ammoniak een relatief zwak proces is, wat betekent dat de meerderheid van de ammoniakmoleculen niet-geïoniseerd in oplossing blijft.
De aanwezigheid van ammonium- en hydroxide-ionen in de oplossing draagt bij aan de basiseigenschappen van waterige ammoniak. De hydroxide-ionen die tijdens ionisatie worden geproduceerd, kunnen reageren met andere zuren die in de oplossing aanwezig zijn, wat leidt tot een verhoging van de pH en een afname van de zuurgraad van de oplossing.
 Beruchte studie naar de ‘donkere kant’ van de mensheid zou wel eens kunnen aantonen hoe we deze op afstand kunnen houden
Beruchte studie naar de ‘donkere kant’ van de mensheid zou wel eens kunnen aantonen hoe we deze op afstand kunnen houden  Gletsjers geven aanwijzingen om woestijnvorming tegen te gaan
Gletsjers geven aanwijzingen om woestijnvorming tegen te gaan Nieuw boek over schimmelziekten van stadsbomen
Nieuw boek over schimmelziekten van stadsbomen Satelliet ziet tropische cycloon Luban naderen Oman
Satelliet ziet tropische cycloon Luban naderen Oman Over de Wasp Life Cycle
Over de Wasp Life Cycle
Hoofdlijnen
- Onderzoek onthult nieuwe aanwijzingen over hoe walvissen en dolfijnen echolocatie gingen gebruiken
- DNA-barcoding van parasitaire wormen:is het koosjer?
- Een betere pinda op je bord? Nieuwe bevindingen onthullen potentieel voor gewasverbetering
- Wat is beter voor uw hond:brokjes of rauw vlees? Onderzoek levert verrassende gezondheidsresultaten op
- Hoe duplicaten in twee rijen in OpenOffice te verwijderen
- Hoe slaapwandelen werkt
- Wetenschappers onthullen hoe SID-1 dsRNA herkent en systemische RNA-interferentie initieert
- Structuur van het hart Cell
- De functies van de linker temporale kwab
- Nieuw slim materiaal werkt beter onder druk
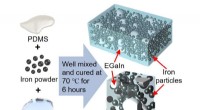
- Team vervaardigt magneten volledig van zeldzame aardmetalen uit de VS

- Omzetting van kooldioxide naar methanol
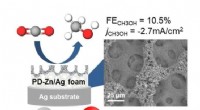
- Onderzoekers ontsluiten kankerverwekkend mechanisme van E. coli-toxine met synthetische biologie

- Nieuw elektrodemateriaal ontwikkeld om de laadcapaciteit van lithiumbatterijen te vergroten
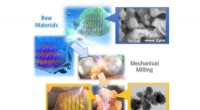
 Wat is de standaard enthalpieverandering voor een reactie die het verbreken van alle bindingen in gasvormig benzeen betekent?
Wat is de standaard enthalpieverandering voor een reactie die het verbreken van alle bindingen in gasvormig benzeen betekent?  Belangrijkste onderdeel om quantum computing op te schalen
Belangrijkste onderdeel om quantum computing op te schalen Tropische cycloon Alcides regenval waargenomen door GPM Satellite
Tropische cycloon Alcides regenval waargenomen door GPM Satellite Woordkeuze is belangrijk in weercommunicatie
Woordkeuze is belangrijk in weercommunicatie Vingertoppen blijken verschillend te reageren op verschillende oppervlakken
Vingertoppen blijken verschillend te reageren op verschillende oppervlakken Zonnebadend apparaat verandert water in oververhitte stoom
Zonnebadend apparaat verandert water in oververhitte stoom Waarom zijn ondiepe meren vatbaar voor eutrofiëring?
Waarom zijn ondiepe meren vatbaar voor eutrofiëring? Nieuwe hybride 3D-printtechniek voegt een vierde dimensie toe aan additive manufacturing
Nieuwe hybride 3D-printtechniek voegt een vierde dimensie toe aan additive manufacturing
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

