
Wetenschap
Eerste gedetailleerde blik op hoe moleculair reuzenrad protonen levert aan cellulaire fabrieken
Een team van wetenschappers heeft voor het eerst gedetailleerd gekeken hoe een moleculair reuzenrad protonen aan cellulaire fabrieken levert, wat nieuwe inzichten oplevert in hoe cellen energie opwekken.
Het onderzoek, gepubliceerd in het tijdschrift Nature, richt zich op een eiwitcomplex genaamd ATP-synthase, dat wordt aangetroffen in de binnenmembranen van mitochondriën, de krachtcentrales van cellen. ATP-synthase gebruikt de energie van een protongradiënt om adenosinetrifosfaat (ATP) te genereren, de belangrijkste energievaluta van de cel.
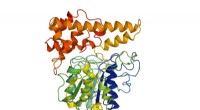
Het ATP-synthasecomplex bestaat uit twee roterende subeenheden, de F1- en F0-subeenheden. De F1-subeenheid bevat de katalytische plaats waar ATP wordt gesynthetiseerd, terwijl de F0-subeenheid verantwoordelijk is voor het genereren van de protongradiënt.
De nieuwe studie, geleid door wetenschappers van de Universiteit van Californië, Berkeley, onthult hoe de F0-subeenheid van ATP-synthase een reeks protonbindingsplaatsen gebruikt om protonen door het membraan te transporteren. De protonen zijn in een specifieke volgorde aan de locaties gebonden, en terwijl de F0-subeenheid roteert, worden de protonen van de ene site naar de volgende doorgegeven totdat ze de katalytische site in de F1-subeenheid bereiken.
Dit proces is vergelijkbaar met de manier waarop een reuzenrad mensen van de ene plaats naar de andere vervoert. De protonen zijn gebonden aan de protonbindende plaatsen zoals mensen gebonden zijn aan de zittingen van een reuzenrad. Terwijl het reuzenrad draait, worden de mensen naar de bovenkant van het reuzenrad getransporteerd, waar ze van boord kunnen gaan.
In het geval van ATP-synthase worden de protonen naar de katalytische plaats getransporteerd, waar ze worden gebruikt om ATP te genereren. Dit proces is essentieel voor het voortbestaan van de cel, omdat ATP nodig is voor een verscheidenheid aan cellulaire functies, waaronder celgroei, beweging en metabolisme.
De nieuwe studie geeft een gedetailleerd inzicht in hoe ATP-synthase werkt, en zou kunnen leiden tot de ontwikkeling van nieuwe medicijnen die zich op dit complex richten. Dergelijke medicijnen kunnen worden gebruikt om een verscheidenheid aan ziekten te behandelen, waaronder kanker en hartziekten.
"Dit onderzoek is een belangrijke doorbraak in ons begrip van hoe cellen energie opwekken", zegt senior auteur van het onderzoek Dr. John Walker, hoogleraar moleculaire biologie aan de Universiteit van Californië, Berkeley. "De inzichten uit deze studie kunnen leiden tot de ontwikkeling van nieuwe behandelingen voor een verscheidenheid aan ziekten."
 Het vriespunt berekenen
Het vriespunt berekenen Zelfherstellende katalysatoren maken het gemakkelijker om zonne-energie op te slaan met water
Zelfherstellende katalysatoren maken het gemakkelijker om zonne-energie op te slaan met water De beste groeicondities voor kristallen
De beste groeicondities voor kristallen  Voordelen en nadelen van steenkoolvergassing
Voordelen en nadelen van steenkoolvergassing  Palladium nanoclusterkatalysator ondersteunt zeer efficiënte en regioselectieve hydrogenering van epoxiden
Palladium nanoclusterkatalysator ondersteunt zeer efficiënte en regioselectieve hydrogenering van epoxiden
 De meeste EU-landen hebben vorig jaar de CO2-uitstoot verminderd:schattingen
De meeste EU-landen hebben vorig jaar de CO2-uitstoot verminderd:schattingen Maritiem continent verzwakt Aziatische tropische moessonregen door Australische stromen over de evenaar
Maritiem continent verzwakt Aziatische tropische moessonregen door Australische stromen over de evenaar Geologische vingerafdrukken van vulkanische as
Geologische vingerafdrukken van vulkanische as Een 3D-blik op de 2015 El Nino
Een 3D-blik op de 2015 El Nino Wereldwijde de-oxygenatie van de oceaan gekwantificeerd
Wereldwijde de-oxygenatie van de oceaan gekwantificeerd
Hoofdlijnen
- Wat veroorzaakt psychische aandoeningen?
- Nieuwe forensische methode heeft tot doel te voorspellen hoe een persoon eruit ziet op basis van een DNA-monster
- Studie suggereert nieuwe doelen voor het verbeteren van het sojaoliegehalte
- Grote katten in Groot-Brittannië - stedelijke mythe of wetenschappelijk feit?
- Hoe kan een mutatie in DNA invloed hebben op eiwitsynthese?
- Genetisch verhogen van de voedingswaarde van maïs kan miljoenen ten goede komen
- Hoe een biologisch diagram te tekenen
- Onderzoekers ontdekken dat de celcortex wordt geactiveerd door duizenden kortlevende eiwitcondensaten
- Hoe cellulaire vingertoppen cellen kunnen helpen met elkaar te ‘praten’
- Biofysici verhelderen de mechanismen van neutrale dragers van opgeloste stoffen

- Wetenschappers ontdekken bindend geheim achter eiwitsuperlijm
- Computer herontwerpt enzym

- Isolerende stenen met microscopisch kleine belletjes

- Klein worden om te bepalen waar nucleair materiaal vandaan komt en hoe het is gemaakt

 Geleidende ferro-elektriciteit kan de sleutel zijn tot nieuw elektronisch geheugen
Geleidende ferro-elektriciteit kan de sleutel zijn tot nieuw elektronisch geheugen Onderzoek bevestigt fecale bacteriën vervuild oppervlaktewater na orkaan Harvey
Onderzoek bevestigt fecale bacteriën vervuild oppervlaktewater na orkaan Harvey Principes voor het modelleren van aardoppervlaksystemen en hun eco-omgevingscomponenten
Principes voor het modelleren van aardoppervlaksystemen en hun eco-omgevingscomponenten Nanopore-technologie zorgt voor een doorbraak in de detectie van eiwitvarianten
Nanopore-technologie zorgt voor een doorbraak in de detectie van eiwitvarianten  Zeeniveau is een verrassend variabele parameter
Zeeniveau is een verrassend variabele parameter Wat is de verticale lijntest?
Wat is de verticale lijntest?  Langetermijnstudie van gelijmde stalen wapeningen op een betonnen balk gaat 50e jaar in
Langetermijnstudie van gelijmde stalen wapeningen op een betonnen balk gaat 50e jaar in Renault boekt recordverkopen als opvolger van Ghosn gezocht
Renault boekt recordverkopen als opvolger van Ghosn gezocht
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

