
Wetenschap
Wetenschappers identificeren een klasse van bindende moleculen die kunnen worden gebruikt voor gerichte eiwitafbraak
In de strijd tegen kanker en andere ziekten ontwikkelen wetenschappers moleculaire wapens die kunnen worden gebruikt om de oncontroleerbare celgroei te stoppen.
Een team van wetenschappers van Harvard en het Massachusetts General Hospital heeft ontdekt dat 'cyclimiden', een klasse van bindende moleculen die bekend staan als liganden, een veelbelovende en efficiënte aanpak bieden voor het verwijderen van ziekteveroorzakende of slecht functionerende eiwitten. Hun specifieke eigenschappen stellen wetenschappers in staat dwalende eiwitten aan te vallen bij hun moleculaire wortels.
"Al meer dan een jaar hebben we de vraag aangepakt wat de natuurlijke liganden zijn die worden herkend door cereblon, een eiwit dat cruciaal is voor gerichte afbraak", zegt senior co-auteur Christina Woo, Morris Kahn universitair hoofddocent scheikunde en chemische biologie. "Deze studie karakteriseert deze liganden uitgebreid om nieuwe inzichten te verschaffen in de biologie van de hersenen en hoe deze te kapen."
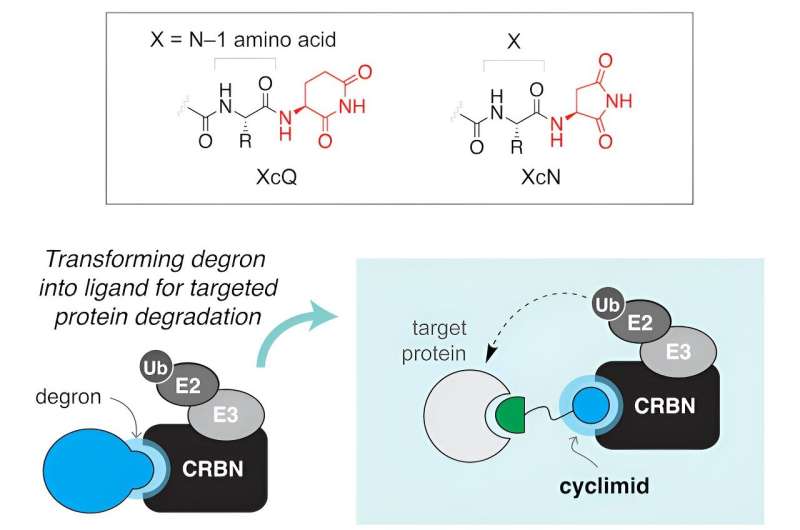
De afgelopen jaren hebben wetenschappers kleine moleculen ontwikkeld die zich specifiek richten op eiwitten die verband houden met ziekten. Deze moleculen hebben twee rollen:ze hechten zich aan het doeleiwit dat moet worden verwijderd, en hun ‘kernkop’ werkt samen met een deel van het cellulaire schoonmaaksysteem, waarbij ze zich vaak binden aan een eiwit dat cereblon wordt genoemd. Samen vormen deze gespecialiseerde moleculen wat wetenschappers een ternair complex noemen. Zodra dit complex is gevestigd, wordt het doeleiwit effectief gemarkeerd voor verwijdering door het proteasoom van de cel, dat fungeert als een cellulair recyclingsysteem.
Het succes van dit proces – het verwijderen van specifieke eiwitten – is afhankelijk van het ontwerp en de efficiëntie van de moleculaire kernkop, waardoor ze cruciale elementen zijn in de ontwikkeling van therapieën voor verschillende ziekten, waaronder kanker.

In het artikel van de onderzoekers gepubliceerd in Cell Chemical Biology vonden ze dat kleine structurele veranderingen aan het cereblon-ligand de biologische activiteiten in cellen dramatisch kunnen veranderen. In samenwerking met het Mazitschek Lab, dat uitgebreid onderzoek heeft gedaan naar de identificatie van ziekterelevante moleculaire doelwitten, introduceerden de onderzoekers een systematische biochemische benadering voor het kwantificeren van de vorming van ternaire complexen. Met deze methode kunnen onderzoekers de cellulaire afbraakactiviteit van cyclimiden effectiever voorspellen, waardoor het ontwikkelingsproces wordt gestroomlijnd.
"Met onze methode hebben we de gemeenschap een krachtige en betaalbare microscoop gegeven", zegt Ralph Mazitschek, co-senior auteur. "We hebben een alomvattend, betrouwbaar, robuust en gevoelig profileringsplatform opgezet dat toepasbaar is op vrijwel al deze kleine molecuulafbrekers en moleculaire lijmafbrekers."
"Dit was een samenwerking in de ware zin van het woord", zegt Connor Payne, postdoctoraal onderzoeker in het laboratorium van Mazitschek. "We hadden verschillende expertises en verschillende technologieën die we ontwikkelden, dus de synergie daartussen was echt heel mooi om te zien tot bloei komen."
In de toekomst zijn Woo en Mazitschek optimistisch dat cyclimiden en hun screeningplatforms zullen worden opgenomen in eiwitafbraakstrategieën, die nuttig zouden kunnen zijn bij de ontwikkeling van medicijnen en de behandeling van kanker.
"Ik denk dat ons onderzoek uiteindelijk het profileren van veel meer moleculen tegen gewenste doelen zal vergemakkelijken en sneller tot selectievere en effectievere moleculen zal komen", aldus Woo. "Er zijn veel verschillende richtingen die dit ons zou kunnen geven."