Wetenschap
Gericht op ijzeropname om een nieuwe klasse antibiotica tegen urineweginfecties te creëren
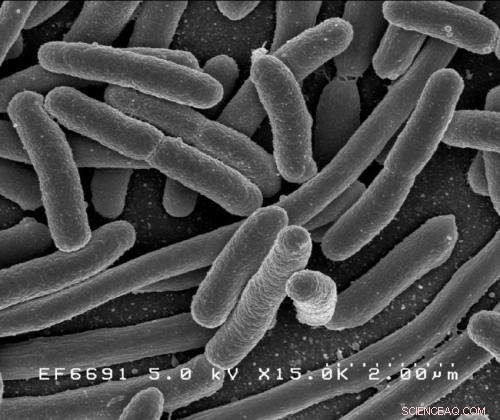
Escherichia coli. Krediet:Rocky Mountain-laboratoria, NIAID, NIH
Bij 11 miljoen gevallen per jaar, urineweginfecties (UTI's) zijn de meest voorkomende poliklinische infecties in de VS, volgens het Amerikaanse ministerie van Volksgezondheid en Human Services. Minstens de helft van alle vrouwen krijgt tijdens hun leven een urineweginfectie, en veel van de infecties - die steeds meer resistent zijn geworden tegen een breed scala aan antibiotica - komen terug. Nutsvoorzieningen, onderzoekers rapporteren vroege vooruitgang in de richting van de ontwikkeling van een nieuwe klasse antibiotica die deze infecties zouden bestrijden door de veroorzakende bacteriën van ijzer uit te hongeren.
De onderzoekers presenteren hun resultaten vandaag op de American Chemical Society (ACS) Fall 2020 Virtual Meeting &Expo.
"Je kunt niet voorkomen dat bacteriën zich ontwikkelen en resistentie ontwikkelen tegen antibiotica, " zegt Mary Rose Ronquillo, een student die werkt in het lab van Scott C. Eagon, doctoraat "Het doel van ons onderzoek is om een medicijn te ontwikkelen dat op een andere manier werkt dan de huidige medicijnen - door de bacteriën ijzer te ontnemen, een belangrijke voedingsstof die essentieel is voor hun overleving."
Momenteel, de meeste geneesmiddelen die UTI's behandelen die worden veroorzaakt door uropathogeen E coli (UPEC) ofwel de synthese van de bacteriële celwand verstoren of de bacteriële DNA-replicatie verstoren. Omdat de urinewegen een omgeving met een ijzertekort zijn, UPEC heeft verschillende manieren ontwikkeld om ijzer te verkrijgen, zoals door moleculen te produceren die sideroforen worden genoemd en die ijzer opzuigen dat is gebonden aan gastheereiwitten.
De onderzoekers, die aan de California Polytechnic State University zijn, hebben aan dit project samengewerkt met andere wetenschappers van de University of Michigan School of Medicine. De medewerkers toonden eerder aan dat het ijzerverwervingsproces een doelwit kan zijn voor kleine moleculen voor een mogelijke UTI-behandeling. In die studie, ze screenden bijna 150, 000 verbindingen en identificeerde er 16 die voorkomen dat deze bacteriën groeien onder ijzerbeperkende omstandigheden. Van deze 16 twee verbindingen waren gekoppeld aan verstoring van het bacteriële TonB-systeem, die bestaat uit drie transmembraaneiwitten die UPEC helpen ijzer op te nemen. De groep van Eagon concentreert zich op deze twee verbindingen voor verder onderzoek.
"We hebben een van deze verbindingen geselecteerd als een scaffold om te wijzigen in potentiële kleine molecuulremmers van het TonB-systeem, " M. Cole Detels, een student in het lab van Eagon, verklaart. Het molecuul heet 2-{[(3-chloor-4-methoxyfenyl)amino]methyl}chinoline-8-ol, of eenvoudiger, de "hydroxychinoline-steiger."
Nadat ze het steigermolecuul hadden gemaakt, Detels en Ronquillo maakten vijf variaties, en nog eens drie bevinden zich nu in de zuiveringsfase. "Hoewel de synthese van de potentiële medicijnen relatief eenvoudig is, het was een uitdaging om ze te zuiveren van de soep van andere chemicaliën die bij hun bereiding werden gebruikt, ', zegt Detels.
Het team zegt dat het doel is om een bibliotheek van remmers voor te bereiden waarin de hydroxychinoline-steiger wordt gemodificeerd met verschillende functionele groepen. "Met deze bibliotheek in de hand, we zullen samenwerken met onze medewerkers om ze te screenen tegen UPEC en menselijke cellijnen om te zoeken naar brede toxiciteit, "zegt Eagon. "Daarna, de verbindingen zullen worden getest in diermodellen om te zien of ze de bacteriën in vivo doden." Zodra het team van Eagon klaar is met het voorbereiden van de volledige hydroxyquinoline-bibliotheek, ze zijn van plan variaties te maken op het tweede scaffoldmolecuul.
Omdat ze gericht zijn op ijzeropname, deze nieuwe klasse geneesmiddelen zal naar verwachting geen effect hebben op heilzame E coli spanningen in andere delen van het lichaam. IJzer is overvloedig aanwezig in het lichaam op niet-urineweglocaties, dus het belemmeren van de ijzeropname zou geen probleem moeten zijn voor deze bacteriën. De meeste huidige antibiotica, echter, veeg alle stammen uit, inclusief gunstige darmflora. En omdat er geen TonB-homoloog is gevonden bij mensen, de mogelijkheid van toxische bijwerkingen zou ook worden verminderd in vergelijking met andere antibiotica.
 Wat is de chemische MDI?
Wat is de chemische MDI?  3D-geprinte koralen kunnen bio-energie verbeteren en koraalriffen helpen
3D-geprinte koralen kunnen bio-energie verbeteren en koraalriffen helpen Ingenieurs ontwikkelen drijvende boorinstallatie voor zonne-energie voor elektrolyse van zeewater
Ingenieurs ontwikkelen drijvende boorinstallatie voor zonne-energie voor elektrolyse van zeewater Wat doet een katalysator in een chemische reactie?
Wat doet een katalysator in een chemische reactie?  De code van colibactines kraken:onderzoek onderzoekt hoe verbinding DNA beschadigd om het verband met kanker te begrijpen
De code van colibactines kraken:onderzoek onderzoekt hoe verbinding DNA beschadigd om het verband met kanker te begrijpen
Hoofdlijnen
- Squash-variëteit waarvan ooit werd gedacht dat ze uitgestorven was, gedijt goed op biologische boerderij
- Wat is Ashwagandha?
- Ideeën voor het maken van een 3-D DNA-standaard voor middelbare school
- Kwam Eiwit, DNA of RNA als eerste?
- Dissectie van één molecuul van ontwikkelingsgencontrole
- Microbioomtransplantaties bieden ziekteresistentie in ernstig bedreigde Hawaiiaanse plant
- Studie beschrijft hoe de driedimensionale architectuur van het genoom verandert tijdens de celcyclus
- De ontdekking van een mijlpaal verandert de evolutiemarathon in een sprint
- Burgerwetenschappers ontdekken zes nieuwe soorten kevers in Borneo
 Tiny ASTERIA-satelliet behaalt primeur voor CubeSats
Tiny ASTERIA-satelliet behaalt primeur voor CubeSats Sterkere regens in een warmer klimaat kunnen de schade door hitte aan gewassen verminderen, zegt studie
Sterkere regens in een warmer klimaat kunnen de schade door hitte aan gewassen verminderen, zegt studie Hoe zijn fytoplankton reproductie?
Hoe zijn fytoplankton reproductie?  Nanosponzen kunnen infectie met SARS-CoV-2 coronavirus onderscheppen
Nanosponzen kunnen infectie met SARS-CoV-2 coronavirus onderscheppen Wat als uw auto u bespioneert?
Wat als uw auto u bespioneert? Draagbare chemiekit maakt het mogelijk om de zoetheid van bushfood ter plaatse te testen
Draagbare chemiekit maakt het mogelijk om de zoetheid van bushfood ter plaatse te testen Harvey brengt verborgen capaciteit naar voren in het maatschappelijk middenveld om te reageren, zegt veerkrachtexpert
Harvey brengt verborgen capaciteit naar voren in het maatschappelijk middenveld om te reageren, zegt veerkrachtexpert NASA observeert de vorming van tropische storm Miriams
NASA observeert de vorming van tropische storm Miriams
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com