
Wetenschap
Gemodificeerd kankermedicijn effectief tegen multiresistente bacteriën
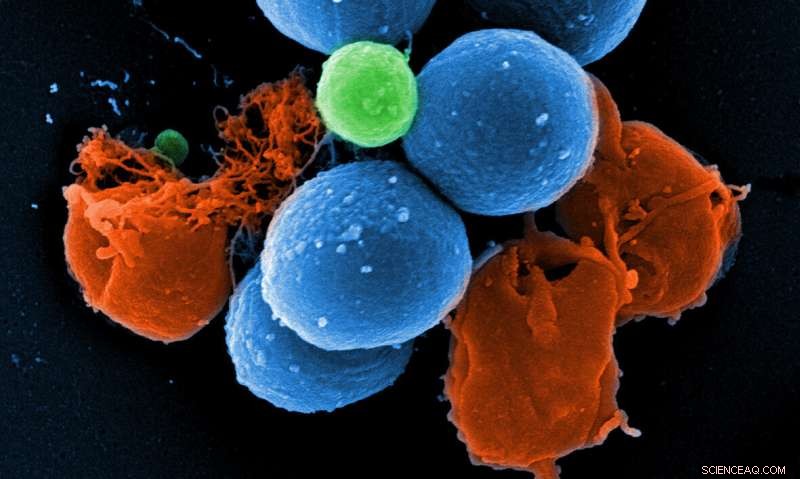
Scanning-elektronenmicrofoto van intacte MRSA (blauw), PK150-geïnduceerde blaasjesvorming (groen), en MRSA vernietigd door PK150 (rood). Krediet:Manfred Rohde / HZI
Antibioticaresistente bacteriën zijn in toenemende mate de bron van dodelijke infecties. Een team van wetenschappers van de Technische Universiteit van München (TUM) en het Helmholtz Center for Infection Research (HZI) in Braunschweig hebben nu een goedgekeurd kankermedicijn aangepast om een actief middel te ontwikkelen tegen multiresistente pathogenen.
De methicilline-resistente Staphylococcus aureus (MRSA) is de bron van ernstige en aanhoudende infecties. Sommige stammen zijn zelfs resistent tegen meerdere antibiotica. Er is dan ook een dringende behoefte aan nieuwe geneesmiddelen die effectief zijn tegen MRSA-infecties.
"De industriële ontwikkeling van nieuwe antibiotica stagneert en houdt geen gelijke tred met de verspreiding van antibioticaresistentie. We hebben dringend innovatieve benaderingen nodig om te voldoen aan de behoefte aan nieuwe infectietherapieën die niet direct tot hernieuwde resistentie leiden, " zegt prof. Eva Medina, directeur van de HZI Onderzoeksgroep Infectieimmunologie.
Nieuwe strategieën voor de ontwikkeling van antibiotica
Een veelbelovende strategie is om het potentiële effect van goedgekeurde medicijnen op bacteriën te testen. "Onze focus lag op een klasse van menselijke eiwitten die kinasen worden genoemd, die om te beginnen veel remmers hebben, " legt studieleider Stephan Sieber uit, hoogleraar organische chemie aan de TUM.
In deze geest, de onderzoekers hebben de werkzame stof sorafenib chemisch gewijzigd, een kankermedicijn dat effectief is tegen MRSA, om een sterker antibiotisch effect te bereiken. Dit leidde tot de ontwikkeling van PK150, een molecuul dat 10 keer effectiever is tegen MRSA dan de oorspronkelijke stof.

Wetenschappers onder leiding van prof. Stephan Sieber van de Technische Universiteit van München en prof. Eva Medina van het Helmholtz Center for Infection Research hebben een goedgekeurd kankermedicijn aangepast om een actief middel te ontwikkelen tegen multiresistente pathogenen. Op de foto is te zien hoe auteur Robert Macsics een agarplaat bekijkt waarop kolonies Staphylococcus aureus zijn gegroeid. Krediet:Andreas Heddergott / TUM
Meerdere aanvallen voorkomen de ontwikkeling van resistentie
Het krachtige nieuwe middel richt zich op verschillende onconventionele structuren in de bacteriën. Twee doelen werden nader onderzocht:PK150 remt een essentieel eiwit dat betrokken is bij het bacteriële energiemetabolisme. Voor een ander, het werkt op de celwand.
In tegenstelling tot eerder bekende antibiotica zoals penicilline en methicilline, die interfereren met celwandvorming, PK150 werkt indirect. Het slaat de eiwitproductie in bacteriën uit balans. Als resultaat, de bacteriën geven meer eiwitten af die de celwanddikte naar buiten sturen, waardoor de cellen barsten.
In muizen, PK150 is in verschillende weefsels effectief gebleken tegen MRSA. Terwijl stafylokokken snel resistentie ontwikkelen tegen andere antibiotica, de onderzoekers zagen geen ontwikkeling van enige resistentie tegen PK150.

Wetenschappers onder leiding van prof. Stephan Sieber van de Technische Universiteit van München en prof. Eva Medina van het Helmholtz Center for Infection Research hebben een goedgekeurd kankermedicijn aangepast om een actief middel te ontwikkelen tegen multiresistente pathogenen. De foto toont auteur Robert Macsics in het laboratorium van de groep van Prof. Sieber aan de steriele werkbank. Krediet:Andreas Heddergott / TUM
Effectiviteit tegen biofilms en persisters
Eva Medina en Dr. Katharina Rox, een farmacoloog van de afdeling Chemische Biologie van de HZI, toonde aan dat PK150 gunstige farmacologische eigenschappen heeft. Het kan als tablet worden toegediend, bijvoorbeeld, en blijft enkele uren stabiel in het lichaam. "Als gevolg van de chemische veranderingen in het molecuul, PK150 bindt niet langer aan menselijke kinasen, maar werkt heel specifiek tegen bacteriële doelwitten, ' zegt Sieber.
En PK 150 heeft nog een ander voordeel:"MRSA-infecties zijn vaak chronisch, omdat de bacteriën inactief kunnen worden. PK150 doodt deze zelfs, evenals ziektekiemen beschermd in biofilms, " zegt prof. Dietmar Pieper, hoofd van de HZI onderzoeksgroep "Microbial Interactions and Processes."
In het kader van het aBACTER-project, Het team van prof. Sieber is nu bezig met het verder optimaliseren van PK150 om de klinische ontwikkelingsfase in te gaan.
De studie is gepubliceerd in Natuurchemie .
 Bomen planten is geen wondermiddel voor klimaatverandering, ecoloog schrijft in Science-commentaar
Bomen planten is geen wondermiddel voor klimaatverandering, ecoloog schrijft in Science-commentaar Wetenschappers krijgen als eerste inzicht in oorzaak van aardbevingen in slow motion
Wetenschappers krijgen als eerste inzicht in oorzaak van aardbevingen in slow motion UITLEG:Waarom Haïti vatbaar is voor verwoestende aardbevingen
UITLEG:Waarom Haïti vatbaar is voor verwoestende aardbevingen Feds kondigen historische waterbezuinigingen aan:wat betekent dit?
Feds kondigen historische waterbezuinigingen aan:wat betekent dit? 5 mythes over hernieuwbare energie
5 mythes over hernieuwbare energie
Hoofdlijnen
- Het verschil tussen rode en witte bloedcellen
- Kenmerken van Twins
- Nieuwe studie voorspelt wereldwijde verandering in ondiepe rifecosystemen als het water warmer wordt
- Twee fasen van fotosynthese
- Lake Michigan watervogels botulisme sterfgevallen in verband met warm water, algen
- De handel in neushoornhoorn legaliseren - reken niet blindelings aan
- Hoe overleef je een massale uitsterving?
- Nieuwe zoomtechniek onthult voor het eerst een elektrisch circuit van cellen
- Hoe is mitose van invloed op het leven?
- Filmen op hoge snelheid onthult eiwitveranderingen tijdens fotosynthese

- Noem die whisky:colorimetrische herkenning van aldehyden en ketonen
- Ontbrekende atomen in een vergeten kristal brengen luminescentie

- Verslaving behandelen:Cryo-EM-technologie maakt het onmogelijke mogelijk
- Onderzoekers melden nieuw begrip van thermo-elektrische materialen

 Wat inheemse overlevenden van seksueel misbruik van kinderen aan onderzoekers vertelden die ze nodig hebben
Wat inheemse overlevenden van seksueel misbruik van kinderen aan onderzoekers vertelden die ze nodig hebben Keniaanse boeren proosten op groeiende vraag Europese vraag naar avocado's
Keniaanse boeren proosten op groeiende vraag Europese vraag naar avocado's Ongekende rook in bosbrandseizoenen was verantwoordelijk voor meer dan 400 doden
Ongekende rook in bosbrandseizoenen was verantwoordelijk voor meer dan 400 doden Nieuw beschreven soorten giraffen kunnen helpen bij het traceren van de evolutie van voorouders van giraffen
Nieuw beschreven soorten giraffen kunnen helpen bij het traceren van de evolutie van voorouders van giraffen Post-Tropical Storm Teddy in nachtelijk zicht op NASA Newfoundland
Post-Tropical Storm Teddy in nachtelijk zicht op NASA Newfoundland Hubble onthult een gigantische kosmische Bat Shadow
Hubble onthult een gigantische kosmische Bat Shadow Wetenschappers distilleren koemelk tot nanocapsules voor medicijnafgifte
Wetenschappers distilleren koemelk tot nanocapsules voor medicijnafgifte Hoe een autocorrelatiecoëfficiënt te berekenen
Hoe een autocorrelatiecoëfficiënt te berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

