
Wetenschap
Buurtreactie:een radicale strategie om drie organische groepen met elkaar te verbinden
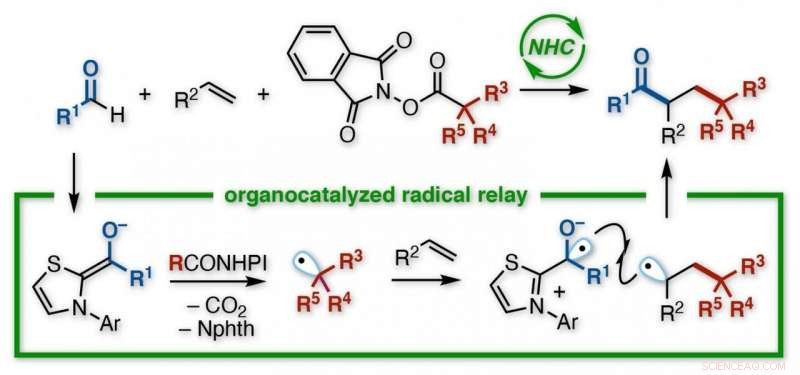
Een Japans onderzoeksteam aan de Kanazawa University ontwikkelde een reactie voor het maken van gefunctionaliseerde ketonen. Met behulp van een N-heterocyclische carbeen (NHC) organokatalysator, zonder behoefte aan metalen of lichte bestraling, een acyl- en een alkylgroep worden toegevoegd over de dubbele binding van een alkeen. De NHC geeft regioselectieve controle over een relaisproces waarbij elektronenoverdracht betrokken is, gevolgd door opeenvolgende toevoeging van twee radicalen aan het alkeen. De diverse producten zijn nuttige bouwstenen voor verdere syntheses. Krediet:Universiteit van Kanazawa
Organische chemici zijn moleculaire architecten, het ontwerpen van geavanceerde constructies. Naarmate de moleculen die in de wetenschap en de geneeskunde worden gebruikt, steeds complexer worden, er zijn nieuwe tools nodig om de bouwstenen samen te voegen. Nutsvoorzieningen, een Japans team van Kanazawa University heeft een reactie ontwikkeld die drie componenten tegelijk met elkaar verbindt met behulp van vrije radicalen.
Dubbele koolstof-koolstofbindingen, bekend als alkenen, zijn reactiever dan enkele bindingen. Dit maakt ze bruikbaar voor het verbinden van verschillende groepen:als de dubbele binding wordt verbroken, aan beide uiteinden kunnen twee nieuwe moleculen worden toegevoegd, overbrugd door het nu enkelvoudig gebonden voormalige alkeen.
Het Kanazawa-team heeft gekeken naar manieren om deze transformatie te bereiken met behulp van aldehyden, die een dubbele binding tussen zuurstof en koolstof bevatten, als een van de twee moleculen geënt op een alkeen. Zoals gemeld in de Tijdschrift van de American Chemical Society , het doel was om zeer gefunctionaliseerde ketonen te creëren, een belangrijke familie van verbindingen in de organische synthese.
Hun gekozen methode was een bekende reactie, suggestief genoeg, als een radicaal relais. Met een ongepaard elektron, en dus een halflege orbitaal, radicalen (of vrije radicalen) hebben de neiging vraatzuchtig reactief te zijn. Zo reactief, inderdaad, dat ze niet kunnen worden opgeslagen, maar moet in-situ worden gegenereerd door ergens tijdens een reactie een elektron af te slaan, een cascade van verbreken en maken van bindingen op gang brengen.
Chemici kunnen op verschillende manieren radicalen maken, maar het Kanazawa-team wilde een oraganokatalysator testen, een N-heterocyclisch carbeen (NHC) genoemd. Met een aldehyde als een reactant, en een gefunctionaliseerde redoxester als de andere, de NHC veroorzaakte hun transformatie in radicalen. Eerdere studies lieten doorschemeren dat beide radicalen sneller zouden reageren met een alkeen dan met elkaar.
"De uitdaging met radicalen is dat, zo onstabiel zijn, ze reageren vaak met zichzelf, ", zegt co-auteur Kazunori Nagao. "Dan krijg je ofwel je startmateriaal terug, of een bijproduct, in plaats van het doel. We hebben dit hier geminimaliseerd. In feite, de reactie verliep als een relais - eerst de alkylradicaal toegevoegd aan één koolstofatoom van het alkeen, en dan de acylradicaal toegevoegd aan de andere."
De resulterende verbinding had een keton en een van ester afgeleide groep gebonden aan twee aangrenzende koolstofatomen, in een zogenaamde buurtopstelling. Hoewel er ook een directe reactie tussen de verschillende radicalen optrad, wat een ongewenst tweecomponentenproduct opleverde, in plaats van het met alkeen overbrugde driecomponentendoel - het was klein. Verder, een breed scala aan uitgangsmaterialen was compatibel met het proces.
"Twee cruciale punten zijn het vermelden waard, " zegt Hirohisa Ohmiya, corresponderende auteur van de studie. "Eerst, in tegenstelling tot sommige reacties, de onze is vrij van metaalkatalysatoren en heeft geen lichtbron nodig om radicalen te produceren, waardoor het groen en veelzijdig is. Tweede, de NHC regelt nauwkeurig het relais, zodat we selectief kunnen zijn in de posities van functionele groepen. We werken nu aan een asymmetrische versie voor chirale producten."
 Een nieuwe gelelektroforesetechniek voor snelle biomarkerdiagnose via massaspectrometrie
Een nieuwe gelelektroforesetechniek voor snelle biomarkerdiagnose via massaspectrometrie Alternatief cement met lage ecologische voetafdruk ontwikkeld
Alternatief cement met lage ecologische voetafdruk ontwikkeld Welke faseveranderingen zijn exotherm en endotherm?
Welke faseveranderingen zijn exotherm en endotherm?  Een ongrijpbare ontbrekende schakel isoleren
Een ongrijpbare ontbrekende schakel isoleren Geavanceerde biomaterialen met zijde-fibroïne-bioactief glas om patiëntspecifieke 3D-bottransplantaten te ontwikkelen
Geavanceerde biomaterialen met zijde-fibroïne-bioactief glas om patiëntspecifieke 3D-bottransplantaten te ontwikkelen
Hoofdlijnen
- Wat is TA Cloning?
- E. Coli kweken in een petrischaal
- Edinburgh Zoo:panda Tian Tian zal dit jaar niet bevallen
- De drie manieren waarop een RNA-molecuul structureel verschilt van een DNA-molecule
- Centrosoom: definitie, structuur en functie (met diagram)
- Malariaparasiet verpakt genetisch materiaal voor reis van muggen naar mensen
- Nieuw onderzoek naar speurhonden kan levens redden
- Horror als Noorse goederentreinen meer dan 100 rendieren neermaaien
- Kluizenaar of niet? Wetenschappers gebruiken Twitter om spidervragen aan te pakken
- Microschaal thermoforese om hits van high-throughput screening te karakteriseren

- De grootste maan van Saturnus kan de sleutel zijn tot schonere motoren

- Chemici brengen gemengde gevouwen eiwitten tot leven

- Van een bijproduct van de biodieselindustrie tot duurzame productie van een waardevolle chemische stof
- Extreme omstandigheden in halfgeleiders

 Menselijke activiteiten verhogen het risico dat de zomer vroeg begint in Zuid-Korea
Menselijke activiteiten verhogen het risico dat de zomer vroeg begint in Zuid-Korea Racisme en discriminatie tegen homo's vergroten het risico op arrestatie en opsluiting
Racisme en discriminatie tegen homo's vergroten het risico op arrestatie en opsluiting Namen van de structurele componenten van het menselijk hart
Namen van de structurele componenten van het menselijk hart  Een 3D-model maken van de planeet Venus
Een 3D-model maken van de planeet Venus Pre-Kaikoura-enquête vond hiaten in het bewustzijn van de tsunami van Kiwi's
Pre-Kaikoura-enquête vond hiaten in het bewustzijn van de tsunami van Kiwi's NASA-NOAA-satelliet vindt een grote tropische cycloon Gaja
NASA-NOAA-satelliet vindt een grote tropische cycloon Gaja Wat hebben Mars en de aarde gemeen?
Wat hebben Mars en de aarde gemeen?  Bosbranden woeden bij Turkse resorts, drie doden
Bosbranden woeden bij Turkse resorts, drie doden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | Dutch | Danish | Norway | French | German |

-
Wetenschap © https://nl.scienceaq.com

