
Wetenschap
Genoommijnbouw onthult nieuwe productieroute voor veelbelovende malariabehandeling

Elisabeth Parkinson, links, Universitair Docent Scheikunde, Purdue University met G. William Arends hoogleraar moleculaire en cellulaire biologie William Metcalf, Rechtsaf. Krediet:Universiteit van Illinois in Urbana-Champaign
Microben staan bij biologen bekend als meester-ingenieurs van bruikbare kleine moleculen, en er zijn veel kneepjes van het vak. Toen onderzoekers van de Universiteit van Illinois nader bekeken hoe een bekende microbe een bekend zogenaamd natuurlijk product maakt, ze werden beloond met de ontdekking van een volledig onbekende biochemische truc.
G. William Arends hoogleraar Moleculaire en Cellulaire Biologie aan de Universiteit van Illinois William Metcalf leidde de studie met de toenmalige postdoctoraal onderzoeker Elizabeth (Betsy) Parkinson. Parkinson is nu een assistent-professor scheikunde aan de Purdue University. Metkalf, Parkinson en coauteurs rapporteerden over hun werk, die werd gesteund door de NIH, in Natuur Chemische Biologie .
Het werk begon met een verrassing:de onderzoekers gingen op zoek naar hoe hun microbe, Streptomyces lavendulae, creëert een chemische stof genaamd fosmidomycine. Het team was geïnteresseerd in hoe deze verbinding wordt gemaakt, deels omdat het een antimicrobieel middel is dat effectief is tegen malaria. een door muggen overgedragen ziekte waaraan jaarlijks honderdduizenden mensen overlijden. Zoals verwacht, S. lavendulae produceerde wel een stof die microben doodde, maar het was geen fosmidomycine.
"Het meest interessante dingenonderzoek is waar je een vraag stelt en je een totaal onverwacht antwoord krijgt, ' zei Metcalf. 'Iets blijkt zoals we hadden verwacht; dat is geweldig!"
Al snel volgden meer verrassingen. Het team herleidde de dodelijke krachten van de bacterie tot de productie van een nauw verwant molecuul, dehydrofosmidomycine, een bekend natuurproduct dat misschien zelfs iets beter is dan fosmidomycine voor de behandeling van malaria. Echter, de genen die S. lavendulae gebruikte om dehydrofosmidomycine te maken, waren totaal anders dan die bij andere microben.
"Het lijkt erg op een andere klasse moleculen waar we in het verleden aan hebben gewerkt, vrijwel identiek, chemisch en structureel, maar de biosyntheseroute en de genen zijn totaal verschillend, Metcalf zei. "Als je nadenkt over evolutie en hoe je daar bent gekomen, dat is fascinerend, dat deze moleculen zo goed zijn dat de natuur het meerdere keren onafhankelijk heeft ontdekt."
Microben ontwikkelen het vermogen om natuurlijke producten zoals fosmidomycine en dehydrofosmidomycine te maken om hen te helpen naburige microben te verslaan om ruimte en hulpbronnen. Elk natuurlijk product is chemisch vervaardigd door een reeks eiwitten die enzymen worden genoemd. die om de beurt het groeiende molecuul aanpassen door atomen toe te voegen of te verwijderen om de vorm en activiteit te veranderen. Microbiële genomen zijn verspreid met clusters van genen die coderen voor deze enzymen, met één cluster dat doorgaans alle genen bevat die nodig zijn voor het maken van één natuurlijk product.
Het laboratorium van Metcalf en andere onderzoekers van het Carl R. Woese Institute for Genomic Biology aan de Universiteit van Illinois willen de relatie onderzoeken tussen microbiële natuurlijke producten en de genclusters die hun productie mogelijk maken. Door te leren herkennen welke genen tot welk soort producten leiden, ze hopen genoomsequencing te gebruiken om de ontdekking van nieuwe natuurlijke producten te versnellen die, zoals fosmidomycine en verwante moleculen, kan belangrijke therapeutische eigenschappen hebben.
Metcalf was bijzonder opgewonden om te zien dat een bekend type molecuul werd gemaakt door een onbekend genencluster.
"De technische term is convergerende evolutie naar een chemisch product, "Zei Metcalf. "En dat zegt u . . . dat het een heel goed molecuul is. Het doet wat de natuur wil:het is antibacterieel en het doodt ook parasieten, zoals malaria en planten, zoals onkruid, het heeft echt veel toepassingen. Het is absoluut niet giftig voor mensen, wat fijn is."
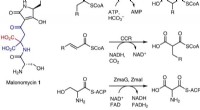
De onderzoekers gingen dieper in op de details van het nieuwe genencluster en de chemische reacties die mogelijk worden gemaakt door de enzymen. Ze reconstrueerden en bevestigden experimenteel een reeks stappen die leidden van de eerste "ingrediënten" tot het eindproduct.
"Dus waarom geef je om hoe moleculen zoals deze worden gemaakt? . . . het is de goedkoopste manier om iets te maken, Metcalf zei. "Dit biedt een andere route naar hetzelfde molecuul, wat misschien een efficiëntere route is, misschien een goedkopere route, dat moet nog worden onderzocht."
Het hoogtepunt van de nieuw ontdekte route was een enzym dat wordt gecodeerd door het gen dfmD. Zijn naam, doet denken aan een bibliotheeknummer en door de onderzoekers gekozen om zijn positie in het dehydrofosmidomycine-producerende gencluster aan te geven, logenstraft de nieuwigheid van de chemische reactie die het enzym faciliteert.
"Je verbreekt twee koolstof-stikstofbindingen, je hervormt één koolstof-koolstofbinding, en je oxideert nog een koolstof-koolstofbinding. En dat doe je allemaal in één stap, " zei Metcalf. Met andere woorden, het enzym breekt een stukje van het grotere molecuul af, draait het om, maakt het weer vast, en tweaks het resulterende product, allemaal in de enkele continue actie, analoog aan een persoon die van stoelconfiguratie verandert in een minibusreclame.
"In de eenvoudigste bewoordingen, wat dfmD doet, is een chemische reactie die niet gemakkelijk voor te stellen is, nummer een, gewoon gebaseerd op de eerste beginselen van de chemie; en nummer twee, dat is nog nooit eerder in de natuur waargenomen, "Zei Metcalf. "Omdat dit iets radicaal anders is, het draagt bij aan die hoeveelheid kennis, zodat wanneer we naar nieuwe wegen kijken, we kunnen nadenken over hoe ze zouden kunnen werken."
 Alternatieve cementrecepten - Een recept voor eco-beton
Alternatieve cementrecepten - Een recept voor eco-beton Patterning-methode kan de weg vrijmaken voor nieuwe op glasvezel gebaseerde apparaten, slim textiel
Patterning-methode kan de weg vrijmaken voor nieuwe op glasvezel gebaseerde apparaten, slim textiel Thermische oorkappen beschermen de batterijen van mobiele telefoons tegen extreme temperaturen
Thermische oorkappen beschermen de batterijen van mobiele telefoons tegen extreme temperaturen De crunch houden in vetarme chips
De crunch houden in vetarme chips Gemakkelijke manieren om koper te smelten
Gemakkelijke manieren om koper te smelten
 Veranderingen in de oceaantransportband voorspelden abrupte klimaatveranderingen met vier eeuwen
Veranderingen in de oceaantransportband voorspelden abrupte klimaatveranderingen met vier eeuwen Onderzoek toont aan dat beperkingen op houtverbranding in Utah de luchtkwaliteit drastisch verbeteren
Onderzoek toont aan dat beperkingen op houtverbranding in Utah de luchtkwaliteit drastisch verbeteren Duurzame pelletproductie redt levens
Duurzame pelletproductie redt levens Vegetatie bestand tegen berging van houtkap na hevige natuurbrand
Vegetatie bestand tegen berging van houtkap na hevige natuurbrand Wat is Griffonia Simplicifolia?
Wat is Griffonia Simplicifolia?
Hoofdlijnen
- Uitgebreide quota voor blauwvintonijn kunnen het herstel ongedaan maken:wetenschappers
- Kamgelei mogelijk eerste afstamming van evolutionaire boom
- Animatie ontmoet biologie - werpt nieuw licht op het gedrag van dieren
- In de mangoestenmaatschappij immigranten zijn een bonus - als ze tijd krijgen om zich te vestigen
- Klimaatverandering, bevolkingsgroei kan leiden tot aquacultuur in open oceaan
- De internationale Human Cell Atlas publiceert strategische blauwdruk, kondigt gegevens aan van de eerste miljoen cellen
- Hoe een 3D-model voor celbiologieprojecten te bouwen Mitochondria & Chloroplast
- Wat is het oudste levende wezen op aarde?
- Critici slaan VS over import van olifantentrofeeën
- Wetenschappers ontdekken nieuwe route naar antibiotica met behulp van genbewerking
- Computationele studie laat zien hoe Ebola nucleocapside stabiliseert

- Vloeibare kristallen kunnen laserpointeraanvallen op vliegtuigen helpen afweren

- Nieuwe methode voor nauwkeurigere bepaling van het tijdstip van overlijden op plaats delict

- Hoe RNA werd gevormd bij de oorsprong van het leven
 Snelle HIV-detectiemethode kan vroege ziekte diagnosticeren
Snelle HIV-detectiemethode kan vroege ziekte diagnosticeren Consumenten:online restaurantrecensies zijn niet allemaal gelijk
Consumenten:online restaurantrecensies zijn niet allemaal gelijk Internationale SWOT-satelliet om 's werelds water te onderzoeken
Internationale SWOT-satelliet om 's werelds water te onderzoeken Een konijn ontleden
Een konijn ontleden  Laserlus koppelt kwantumsystemen over een afstand
Laserlus koppelt kwantumsystemen over een afstand Plastic rommel veroorzaakt ramp op onbewoond eiland in de Stille Oceaan
Plastic rommel veroorzaakt ramp op onbewoond eiland in de Stille Oceaan Moleculaire halfgeleiders kunnen de toekomst van elektronica zijn, en deze nieuwe techniek biedt een manier om ze massaal te produceren
Moleculaire halfgeleiders kunnen de toekomst van elektronica zijn, en deze nieuwe techniek biedt een manier om ze massaal te produceren Holografische beeldvorming kan worden gebruikt om tekenen van leven in de ruimte te detecteren
Holografische beeldvorming kan worden gebruikt om tekenen van leven in de ruimte te detecteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

