
Wetenschap
Nieuwe schaal voor elektronegativiteit herschrijft het leerboek scheikunde

Elektronegativiteit opnieuw gedefinieerd:een nieuwe schaal voor elektronegativiteit omvat de eerste 96 elementen, een duidelijke stijging ten opzichte van eerdere versies. Credit:Martin Rahm/Chalmers University of Technology
Elektronegativiteit is een van de meest bekende modellen om te verklaren waarom chemische reacties plaatsvinden. Nutsvoorzieningen, Martin Rahm van de Chalmers University of Technology, Zweden, heeft het concept opnieuw gedefinieerd met een nieuwe, uitgebreidere schaal. Zijn werk, samen met collega's, waaronder een Nobelprijswinnaar, is gepubliceerd in de Tijdschrift van de American Chemical Society .
De theorie van elektronegativiteit wordt gebruikt om te beschrijven hoe sterk verschillende atomen elektronen aantrekken. Door gebruik te maken van elektronegativiteitsschalen, men kan de geschatte ladingsverdeling in verschillende moleculen en materialen voorspellen, zonder toevlucht te hoeven nemen tot complexe kwantummechanische berekeningen of spectroscopische studies. Dit is essentieel voor het begrijpen van alle soorten materialen, evenals voor het ontwerpen van nieuwe. Dagelijks gebruikt door chemici en materiaalonderzoekers over de hele wereld, het concept is afkomstig van het onderzoek van de Zweedse scheikundige Jöns Jacob Berzelius in de 19e eeuw en wordt veel onderwezen op middelbare schoolniveau.
Nutsvoorzieningen, Martin Rahm, Universitair docent fysische chemie aan de Chalmers University of Technology, heeft een gloednieuwe schaal van elektronegativiteit ontwikkeld.
"De nieuwe definitie is de gemiddelde bindingsenergie van de buitenste en zwakste gebonden elektronen - algemeen bekend als de valentie-elektronen, " hij legt uit.
"We hebben deze waarden afgeleid door experimentele foto-ionisatiegegevens te combineren met kwantummechanische berekeningen. de meeste elementen verhouden zich op dezelfde manier tot elkaar als in eerdere schalen. Maar de nieuwe definitie heeft ook geleid tot enkele interessante veranderingen waarbij atomen van plaats zijn verwisseld in de volgorde van elektronegativiteit. Aanvullend, voor sommige elementen is dit de eerste keer dat hun elektronegativiteit is berekend."
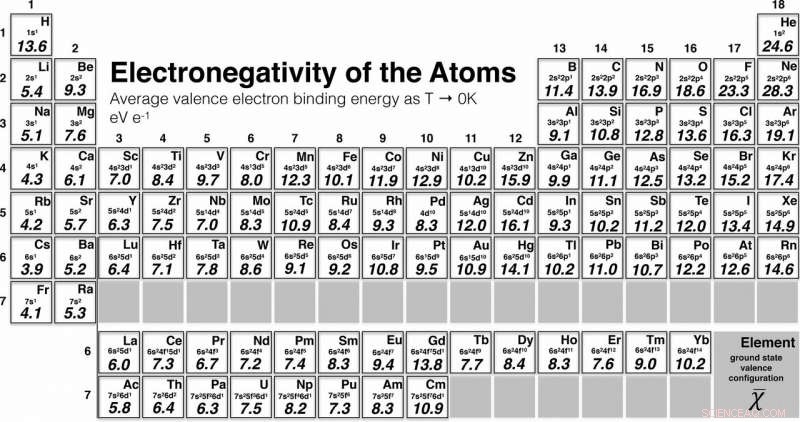
Periodiek systeem met de waarden van de eerste 96 elementen in de nieuwe schaal van elektronegativiteit, gepubliceerd in het artikel in de Tijdschrift van de American Chemical Society . Credit:Martin Rahm/Chalmers University of Technology
Bijvoorbeeld, vergeleken met eerdere schalen, zuurstof en chroom zijn beide opgeschoven in de rangschikking, ten opzichte van elementen die er het dichtst bij staan in het periodiek systeem. De nieuwe schaal omvat 96 elementen, een duidelijke stijging ten opzichte van eerdere versies. De schaal loopt nu vanaf het eerste element, waterstof, tot de zesennegentigste, curium.
Een motivatie voor de onderzoekers om de nieuwe schaal te ontwikkelen was dat, hoewel er verschillende definities van het concept bestaan, elk kan slechts delen van het periodiek systeem dekken. Een extra uitdaging voor chemici is hoe te verklaren waarom elektronegativiteit soms niet in staat is om chemische reactiviteit of de polariteit van chemische bindingen te voorspellen.
Een ander voordeel van de nieuwe definitie is hoe deze past in een breder kader dat kan helpen verklaren wat er gebeurt als chemische reacties niet worden gecontroleerd door elektronegativiteit. Bij deze reacties die moeilijk te begrijpen zijn met conventionele chemische modellen, complexe interacties tussen elektronen zijn aan het werk. Wat uiteindelijk de uitkomsten van de meeste chemische reacties bepaalt, is de verandering in totale energie. In de nieuwe krant de onderzoekers bieden een vergelijking waarbij de totale energie van een atoom kan worden beschreven als de som van twee waarden. Een daarvan is elektronegativiteit, en de tweede is de gemiddelde elektroneninteractie. De grootte en het karakter van deze waarden als ze tijdens een reactie veranderen, onthult het relatieve belang van elektronegativiteit bij het beïnvloeden van het chemische proces.
Er zijn eindeloze manieren om de atomen in het periodiek systeem te combineren om nieuwe materialen te creëren. Elektronegativiteit biedt een eerste belangrijke indicator van wat van deze combinaties kan worden verwacht.
"De schaal is groot, en ik hoop dat het onderzoek op het gebied van scheikunde en materiaalkunde grote gevolgen zal hebben. Elektronegativiteit wordt routinematig gebruikt in chemisch onderzoek en met onze nieuwe schaal kunnen een aantal ingewikkelde kwantummechanische berekeningen worden vermeden. De nieuwe definitie van elektronegativiteit kan ook nuttig zijn voor het analyseren van elektronische structuren die zijn berekend via de kwantummechanica, door dergelijke resultaten begrijpelijker te maken, ’ zegt Martin Rahm.
 Gemodelleerde wolken in de tropen krijgen een reality check
Gemodelleerde wolken in de tropen krijgen een reality check Kabul wordt geconfronteerd met watercrisis als droogte, populatie stam aanbod
Kabul wordt geconfronteerd met watercrisis als droogte, populatie stam aanbod Veranderingen in het post-Sovjet-voedselsysteem leidden tot reductie van broeikasgassen
Veranderingen in het post-Sovjet-voedselsysteem leidden tot reductie van broeikasgassen De cryosfeer van de aarde is van vitaal belang voor iedereen
De cryosfeer van de aarde is van vitaal belang voor iedereen Arctisch zee-ijsverlies in het verleden in verband met abrupte klimaatgebeurtenissen
Arctisch zee-ijsverlies in het verleden in verband met abrupte klimaatgebeurtenissen
Hoofdlijnen
- Arbusculaire mycorrhiza-schimmelgemeenschappen blootgesteld met nieuwe benadering van DNA-sequencing
- Wat zijn de functies van het septum in een regenworm?
- Menselijk genoom DNA-sequentietypen
- Menselijke anatomieprojecten
- Celstructuren en hun drie belangrijkste functies
- Twee doelen van mitose
- Nieuwe techniek doorzoekt het genoom op genen die ziekten bestrijden
- Lignine-afval aangepast voor industrieel gebruik van bio-olie
- Hoe Cytoplasma voor een celproject te maken
- Optisch pincet met aerosol verbetert het begrip van deeltjes in de lucht

- Chemici verkrijgen nieuw materiaal voor antibacteriële voedselcoatings
- Nieuwe methoden voorgesteld om polymere lamellaire kristallen te karakteriseren

- Realtime analyse van MOF-adsorptiegedrag
- Klein printen, zeer nauwkeurige objecten in een kwestie van seconden

 Jetstream wordt niet golvender ondanks de opwarming van het noordpoolgebied
Jetstream wordt niet golvender ondanks de opwarming van het noordpoolgebied Zeer efficiënte koeling met behulp van een nieuwe nanoporeuze vaste stof
Zeer efficiënte koeling met behulp van een nieuwe nanoporeuze vaste stof Een duw voor een verschuiving in het waardesysteem dat impact en succes definieert
Een duw voor een verschuiving in het waardesysteem dat impact en succes definieert Beroemd economisch experiment dat duizenden keren is gereproduceerd
Beroemd economisch experiment dat duizenden keren is gereproduceerd Microsoft houdt bod op Pentagon te midden van ethische bezwaren
Microsoft houdt bod op Pentagon te midden van ethische bezwaren India beoordeelt technisch probleem dat maanmissie afbrak
India beoordeelt technisch probleem dat maanmissie afbrak Nanoblasten van door laser geactiveerde nanodeeltjes verplaatsen moleculen, eiwitten en DNA in cellen
Nanoblasten van door laser geactiveerde nanodeeltjes verplaatsen moleculen, eiwitten en DNA in cellen Auto's ruilen voor deelfietsen kan tot 73 doden per jaar voorkomen
Auto's ruilen voor deelfietsen kan tot 73 doden per jaar voorkomen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Swedish | German | Dutch | Danish | Norway | Italian | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

