
Wetenschap
De sleutelrol van enzymen in de embryonale ontwikkeling begrijpen

Christie Sze, een vijfdejaars promovendus in Feinberg's Driskill Graduate Program in Life Sciences, was de eerste auteur van de studie. Krediet:Jim Prisching
De katalytische activiteit van een enzym genaamd Set1A - een eiwit dat essentieel is voor de levensvatbaarheid van embryonale stamcellen (ESC's) - is niet vereist voor zelfvernieuwing van ESC, volgens een Northwestern Medicine-studie gepubliceerd in het tijdschrift Genen en ontwikkeling .
De bevindingen bieden belangrijke nieuwe inzichten in Set1A, een subeenheid van het COMPASS-eiwitcomplex dat betrokken is bij ontwikkelingsstoornissen en sommige kankers.
"Dit verraste iedereen in het lab, " zei Christie Sze, een vijfdejaars promovendus in Feinberg's Driskill Graduate Program in Life Sciences, en de eerste auteur van de studie. "Het is een onverwachte bevinding:hoewel dit eiwit absoluut belangrijk is voor embryonale stamcellen, de belangrijkste functie is dat niet."
De studie toonde ook aan dat de katalytische functie noodzakelijk is, echter, tijdens ESC-differentiatie, volgens senior auteur Ali Shilatifard, doctoraat, de Robert Francis Furchgott Professor en voorzitter van Biochemie en Moleculaire Genetica.
Set1A is een van de zes leden van de COMPASS-familie van enzymen bij mensen. Deze eiwitten, die voor het eerst werden geïdentificeerd door Shilatifard in 2001, sindsdien is aangetoond dat ze centraal staan in genexpressie door hun rol bij het implementeren van methylering op een histonlocatie genaamd H3K4.
Set1A blijkt bijzonder belangrijk te zijn; in tegenstelling tot andere COMPASS-leden, embryonale stamcellen zonder Set1A kunnen niet overleven. Verder, disfunctie van Set1A is eerder in verband gebracht met ontwikkelingsstoornissen, zoals schizofrenie, en bepaalde kankers.
Hoewel het duidelijk is dat het enzym zelf van cruciaal belang is bij de ontwikkeling, of dit te wijten was aan de belangrijkste methylase-activiteit van Set1A werd niet begrepen.
In de huidige studie, met behulp van een muis embryonaal stamcelmodel, Sze richtte zich specifiek op het SET-domein van Set1A - het deel van het eiwit dat verantwoordelijk is voor zijn katalytische activiteit - met de genbewerkingstool CRISPR.
De wetenschappers ontdekten dat na het verwijderen van het functionele domein van Set1A - waardoor het enzym niet in staat was om methylering te implementeren - de embryonale stamcellen nog steeds overleefden, zonder effect op proliferatie en zelfvernieuwing.
In het tweede deel van de studie, Sze onderzocht de mutante ESC's tijdens differentiatie, en toonde aan dat de katalytische activiteit van Set1A inderdaad vereist was voor normale ESC-differentiatie.
"Het zegt dat in embryonale stamcellen, H3K4-methylering door Set1A is niet belangrijk, maar in differentiatie is het, " zei Shilatifard, ook een professor in de kindergeneeskunde en een lid van het Robert H. Lurie Comprehensive Cancer Center van de Northwestern University. "Dit roept de vraag op:wat is er speciaal aan histon H3K4-methylatie tijdens differentiatie? En wat is de functie van het hele Set1A-eiwit dat onafhankelijk is van zijn katalytische functie?"
Vooruit gaan, het Shilatifard-lab zal andere aspecten van Set1A onderzoeken, om te ontdekken waarom het enzym zelf van cruciaal belang is voor embryonale stamcellen, als het niet zijn katalytische functie is. De bevindingen kunnen helpen om meer inzicht te krijgen in de ontwikkeling van kanker.
"De COMPASS-familie is sterk gemuteerd bij kanker. Hoewel deze studie van een ontwikkelingsaspect is, om kanker te begrijpen, je moet de normale functies van het eiwit begrijpen, " zei Sze. "Ons laboratorium leert steeds meer over elk van deze familieleden, en hoe ze een rol spelen bij ziekte."
In een aanvullende bevinding gegevens uit de studie suggereren ook dat Set1A verantwoordelijk is voor het activeren van bivalente genen - belangrijk voor het reguleren van belangrijke ontwikkelingsprocessen - tijdens differentiatie. Het lab had eerder aangetoond dat een ander COMPASS-enzym, genaamd MLL2, is belangrijk voor deze activering in de zelfvernieuwende staat; de huidige studie suggereert dat er een wisseling van verantwoordelijkheden is tussen de twee enzymen tijdens de verschillende stadia.
 Rekbare supercondensatoren om de draagbare apparaten van morgen van stroom te voorzien
Rekbare supercondensatoren om de draagbare apparaten van morgen van stroom te voorzien Wetenschappers lossen de gouden puzzel van calaveriet op
Wetenschappers lossen de gouden puzzel van calaveriet op De uitkomst van de wapenwedloop tussen mens en bacterie voorspellen
De uitkomst van de wapenwedloop tussen mens en bacterie voorspellen Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels
Studie onthult unieke fysieke, chemische eigenschappen van cicadevleugels Onderzoekers ontdekken een nieuwe fase in blokcopolymeren
Onderzoekers ontdekken een nieuwe fase in blokcopolymeren
 Opinie:waarom demonstranten 12 jaar op hun hoede moeten zijn voor retoriek over de afbraak van het klimaat
Opinie:waarom demonstranten 12 jaar op hun hoede moeten zijn voor retoriek over de afbraak van het klimaat Langst bekende ononderbroken registratie van het Paleozoïcum ontdekt in de wildernis van Yukon
Langst bekende ononderbroken registratie van het Paleozoïcum ontdekt in de wildernis van Yukon Boomringen tonen ongekende stijging van extreem weer in Zuid-Amerika
Boomringen tonen ongekende stijging van extreem weer in Zuid-Amerika Milieuschade door mistreductie is waarneembaar vanuit de ruimte, vind hydrologen
Milieuschade door mistreductie is waarneembaar vanuit de ruimte, vind hydrologen Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde
Studie:gletsjers in Azië worden geconfronteerd met enorme smelting door de opwarming van de aarde
Hoofdlijnen
- Welke moleculen kunnen zonder hulp door het plasmamembraan gaan?
- Namen van DNA-strengen
- CRISPR-octrooioorlogen benadrukken het probleem van het verlenen van brede intellectuele eigendomsrechten voor technologie die publieke voordelen biedt
- rRNA: Wat is het?
- Lokale elektrische reacties in bladeren maken fotosynthese hittetolerant
- 10 misvattingen over de griep
- Nieuw onderzoek lost een van de meest verhitte geschillen over evolutionaire biologie op robuuste wijze op
- Hoe een cel te splitsen in Two
- Projectideeën om het menselijke spijsverteringsstelsel te laten zien op de middelbare school voor studenten
- Indonesische smokkelaars stopten exotische vogels in pijpen:politie

- Ver van harpoenen, walvissen schitteren in de boom van ecotoerisme in IJsland

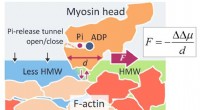
- Nieuwe intermoleculaire oppervlaktekracht onthult actomyosine-aandrijfmechanisme
- Noordelijke blootstelling:fossielen van een zuidelijke walvis voor het eerst gevonden in het noorden

- Celmodel onthult dynamische aard van segmentatieklok die de vorming van wervels stimuleert

 Röntgenstralen, computersimulaties onthullen kristalgroei
Röntgenstralen, computersimulaties onthullen kristalgroei Canadese groep redt Britse muziekretailer HMV
Canadese groep redt Britse muziekretailer HMV Al het zout is niet hetzelfde
Al het zout is niet hetzelfde  Californië kan 600 krijgen, 000 acres nieuwe federaal beschermde wildernis
Californië kan 600 krijgen, 000 acres nieuwe federaal beschermde wildernis Graphenes piëzo-elektrische belofte
Graphenes piëzo-elektrische belofte Het internet der dingen mogelijk maken met een nieuw soort memristors
Het internet der dingen mogelijk maken met een nieuw soort memristors Rapport richt zich op onbenutte arbeidskrachten voor Israëls groeiende hightechsector
Rapport richt zich op onbenutte arbeidskrachten voor Israëls groeiende hightechsector Eenvoudige eenstaps N-terminale modificatie van eiwitten
Eenvoudige eenstaps N-terminale modificatie van eiwitten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

