
Wetenschap
Kunstmatig enzym kan een gen-switch activeren
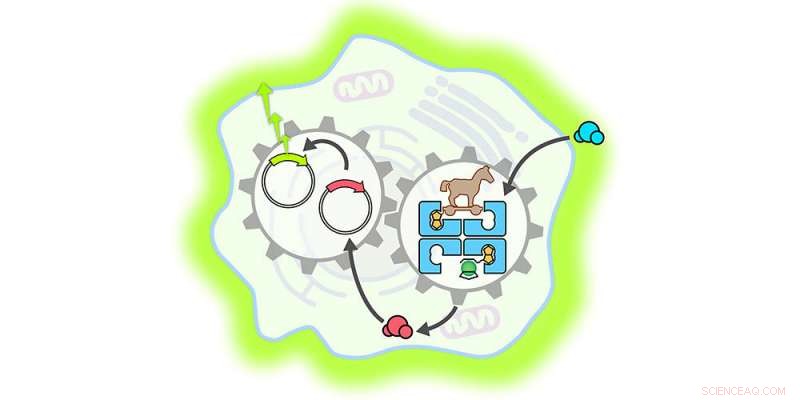
Laat er licht zijn:een kunstmatig metallo-enzym (blauw) dringt een zoogdiercel binnen, waar het de afgifte van een hormoon versnelt (blauwe tot rode bolletjes). Dit activeert een genenschakelaar (cirkels met pijlpunten), wat vervolgens leidt tot de productie van een fluorescerend indicatoreiwit (lichtgroene gloed rond de cel). Krediet:Universiteit van Bazel, Yasunori Okamoto
Complexe reactiecascades kunnen worden geactiveerd in kunstmatige moleculaire systemen:Zwitserse wetenschappers hebben een enzym geconstrueerd dat een zoogdiercel kan binnendringen en de afgifte van een hormoon kan versnellen. Dit activeert vervolgens een genschakelaar die de aanmaak van een fluorescerend eiwit activeert. De bevindingen werden gerapporteerd door onderzoekers van de NCCR Molecular Systems Engineering, geleid door de Universiteit van Basel en ETH Zürich.
De natuur vertrouwt op enzymen om energie-intensieve biochemische reacties te versnellen die nodig zijn voor het behoud van leven. Echter, natuurlijke enzymen zijn niet allemaal even geschikt voor alle reactietypes. Kunstmatig gecreëerde katalysatoren zijn veel veelzijdiger, omdat ze veel meer chemische syntheseprocessen kunnen bevorderen.
Er is dus een groot potentieel in het introduceren van kunstmatige katalysatoren in levende cellen en organen om celfuncties op genetisch niveau te wijzigen of om een medicijn te maken van een onschadelijke voorloper in de cel zelf. Echter, dergelijke katalysatoren werken vaak alleen onder strikt gecontroleerde omstandigheden die in levende cellen bijna onmogelijk te bereiken zijn.
Cascade van kunstmatige componenten
Om deze beperking te overwinnen, onderzoekers van de universiteiten van Basel (professor Thomas Ward) en Genève (professor Stefan Matile) en van ETH Zürich (professor Martin Fussenegger) ontwikkelden een katalysator met kleine moleculen die een gen-switch kan aansturen. Als deze schakelaar is geactiveerd, de gewenste celfunctie wordt geactiveerd.
Voor het huidige onderzoek de onderzoekers maakten een metallo-enzym, een biocompatibel eiwit waarin een katalytisch actief metaalfragment (in dit geval ruthenium) is verwerkt. Met deze methode, ze slaagden er voor het eerst in een kunstmatig metallo-enzym te ontwikkelen dat een zoogdiercel kon binnendringen.
Eenmaal in de cel, het metallo-enzym zette – net als een paard van Troje – zijn katalytische functie in en versnelde de productie van een bepaald schildklierhormoon. Dit hormoon activeerde vervolgens een synthetische genschakelaar die leidde tot de aanmaak van een fluorescerend eiwit dat luciferase wordt genoemd.
Een nieuw soort chemie in levende organismen
De studie, gepubliceerd in Natuurcommunicatie , bewijst de haalbaarheid van een innovatieve aanpak die gericht is op de ontwikkeling van celfuncties en als aanvulling op traditionele biochemische processen. Het werk is een goed voorbeeld van de mogelijkheden die de combinatie van synthetische biologie en organometaalchemie biedt voor de beheersing van celfuncties in levende organismen.
 Top 5 energiezuinige computers
Top 5 energiezuinige computers  Onderzoek toont aan dat de uitstoot van verboden ozonafbrekende stoffen weer afneemt
Onderzoek toont aan dat de uitstoot van verboden ozonafbrekende stoffen weer afneemt Sleutelgewassen zijn de focus van landbouwonderzoek
Sleutelgewassen zijn de focus van landbouwonderzoek Noordelijke oceanen hebben ooit CO2 de atmosfeer in gepompt
Noordelijke oceanen hebben ooit CO2 de atmosfeer in gepompt Machine learning voorspelt nieuwe details van geothermische warmtestroom onder de Groenlandse ijskap
Machine learning voorspelt nieuwe details van geothermische warmtestroom onder de Groenlandse ijskap
Hoofdlijnen
- Muggen dragen bij warm weer vaker het denguevirus over
- Oplossen van hoe een complexe ziekte eiken bedreigt
- Namen van de Enzymen in de Mond & Esophagus
- Sterfgevallen chimpansees in Oeganda toegeschreven aan menselijk verkoudheidsvirus
- De verschillen tussen Mendelian & Polygenic Traits
- Interferentie berekenen
- Het ontrafelen van de mechanismen die de celgroei en -grootte regelen
- Diffusie: wat is het? & Hoe gebeurt het?
- Hoe maak je een 3D-celmembraamodel
- Om vervuiling door voertuigen te verminderen, een enkel atoom kan het werk van meerdere doen

- De geur van pure chocolade, gedemystificeerd
- Wetenschappers vinden een manier om langlevende, snelladende batterijen
- Een stap dichter bij ontwerp-on-demand steigers voor weefselregeneratie

- Zout smelt geen ijs - zo maakt het de winterse straten echt veilig

 Hoe lang duurt het voordat een orkaan door het land reist?
Hoe lang duurt het voordat een orkaan door het land reist?  Grensmuren maken ons niet veiliger of sterker, zegt politicoloog
Grensmuren maken ons niet veiliger of sterker, zegt politicoloog Bento-browser maakt het zoeken op mobiele apparaten gemakkelijker
Bento-browser maakt het zoeken op mobiele apparaten gemakkelijker VS nodigt luchtvaartregelgevers ter wereld uit voor bijeenkomst over Boeings 737 MAX
VS nodigt luchtvaartregelgevers ter wereld uit voor bijeenkomst over Boeings 737 MAX Wetenschappers ontwikkelen nieuwe primaire methode voor het meten van druk
Wetenschappers ontwikkelen nieuwe primaire methode voor het meten van druk Nieuw systeem ontworpen om de waterkwaliteit van rivieren te bewaken
Nieuw systeem ontworpen om de waterkwaliteit van rivieren te bewaken Een sessiele druppel optillen van een superamfifoob oppervlak met behulp van een inslaande druppel
Een sessiele druppel optillen van een superamfifoob oppervlak met behulp van een inslaande druppel Radicale heroverweging nodig om obesitas aan te pakken, honger, klimaat:rapport
Radicale heroverweging nodig om obesitas aan te pakken, honger, klimaat:rapport
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Norway | Portuguese |

-
Wetenschap © https://nl.scienceaq.com

