
Wetenschap
Neutronenstudie van glaucoommedicijnen biedt aanwijzingen over enzymdoelen voor agressieve kankers
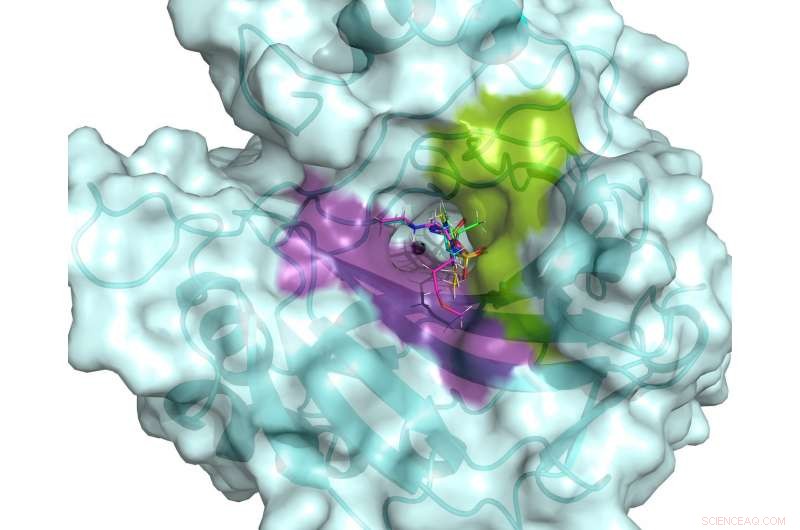
De actieve plaats van hCA II. De actieve plaats wordt geflankeerd door hydrofiele (paarse) en hydrofobe (groene) bindingsholtes die kunnen worden gebruikt om specifieke geneesmiddelen te ontwerpen die zich richten op met kanker geassocieerde hCA's. Vijf klinische geneesmiddelen worden gesuperponeerd getoond in de actieve plaats van hCA II, gebaseerd op neutronenstructuren bij kamertemperatuur. Krediet:ORNL/Andrey Kovalevsky
Nieuwe inzichten uit neutronenanalyse van glaucoommedicijnen en hun enzymdoelwit kunnen wetenschappers helpen bij het ontwerpen van medicijnen die effectiever gericht zijn op agressieve kankers.
Een team van onderzoekers onder leiding van het Oak Ridge National Laboratory van het Department of Energy gebruikte neutronen-macromoleculaire kristallografie om de verschillende toestanden van drie glaucoommedicijnen te onderzoeken terwijl ze interageren met het beoogde enzym, humaan koolzuuranhydrase II (hCA II).
"Ons doel was om verschillen waar te nemen in de presentatie van drie klinisch gebruikte glaucoommedicijnen terwijl ze gebonden zijn aan het hCA II-enzym, " zei Andrey Kovalevsky, een instrumentwetenschapper bij ORNL en een senior co-auteur van de studie. "Door te kijken hoe goed deze medicijnen zich richten op hCA II in geprotoneerde, neutrale en gedeprotoneerde staten, we hoopten inzichten te verkrijgen die het mogelijk zouden maken om deze medicijnen te verbeteren, zodat ze zich beter kunnen richten op enzymen die verband houden met kanker."
Protonering verwijst naar de aanwezigheid, toevoeging of verlies van een proton, waardoor het medicijn een neutrale, positieve of negatieve lading, respectievelijk. Het veranderen van de lading van een medicijn kan zijn vermogen om het doeleiwit te herkennen en eraan te binden veranderen en bijgevolg, zijn effectiviteit.
De studie, gepubliceerd in het tijdschrift Structuur , vond die temperatuur, pH, en de elektrische lading van de drie DrDeramus-geneesmiddelen beïnvloedde hun vermogen om zich te richten op en te binden aan het hCA II-enzym.
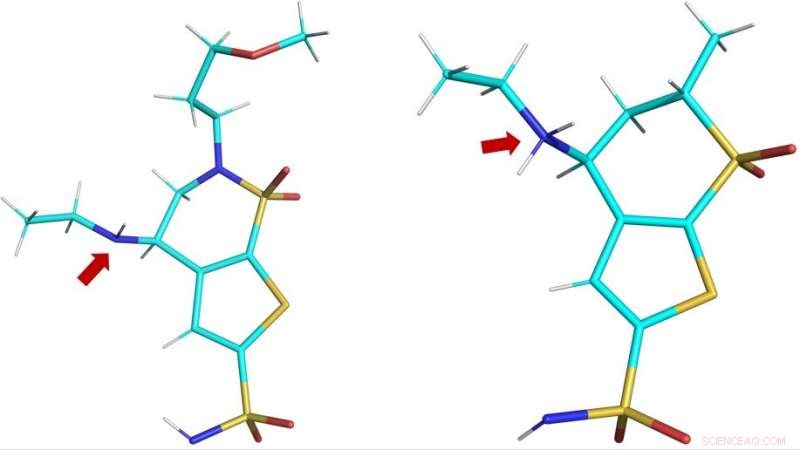
Driedimensionale structuren van de klinische geneesmiddelen brinzolamide (BZM, links) endorzolamide (DZM, rechts) zoals waargenomen in de actieve plaats van hCA II. De rode pijl toont de aminogroepen van de medicijnen:in BZM, het stikstofatoom (in blauw) is niet geprotoneerd en dus niet geladen; in DZM, het stikstofatoom heeft een extra proton opgenomen en is dus positief geladen. Krediet:ORNL/Andrey Kovalevsky
"Deze ontdekking was echt een proof of principle voor ons, " zei Robert McKenna, een professor aan de Universiteit van Florida en een senior co-auteur van de studie. "Het opende onze ogen voor hoe veranderingen in temperatuur en pH de protoneringstoestand van het medicijn kunnen beïnvloeden, wat het op zijn beurt min of meer effectief maakt."
Nieuwe informatie over de waterstofbindingsnetwerken die de actieve plaats van hCA II vormen, kan andere wetenschappers helpen nieuwe en betere geneesmiddelen voor de behandeling van kanker te ontwikkelen. De familie van hCA-enzymen bevat vergelijkbare eiwitten, zoals hCA IX en XII, die geassocieerd zijn met agressieve borstkankers, zoals triple negatieve borstkanker.
"We willen het verschil in verantwoordelijkheid benutten, pH en temperatuur om te zien of we medicijnen kunnen ontwerpen die effectiever zijn in het aanpakken van deze enzymen, " zei Kovalevsky. "Als we binding op atomair niveau kunnen begrijpen, we kunnen medicijnen herontwerpen en ze veranderen in sterkere en selectievere 'magneten' die worden aangetrokken door met kanker geassocieerde enzymen. Dergelijke medicijnen zouden veel effectiever zijn in het doden van kankercellen terwijl gezonde cellen ongedeerd blijven, wat de bijwerkingen voor patiënten aanzienlijk vermindert."
Veel wetenschappers hebben röntgenkristallografie gebruikt om de structuren van hCA-enzymen te analyseren, maar deze studies missen volledige atomaire informatie over medicijnbinding vanwege het onvermogen van röntgenstralen om waterstofatomen te visualiseren die overvloedig aanwezig zijn in eiwitten en enzymen.
Neutronen zijn gevoelig voor lichtere elementen, ze geven dus veel meer gedetailleerde informatie over de locatie van waterstofatomen. Het zien van waterstof is van cruciaal belang voor het bestuderen van protoneringstoestanden van een enzym en ligand - een molecuul dat bindt aan een biologisch macromolecuul - en voor het analyseren van de architectuur van waterstofbindingsnetwerken. Neutronen bieden ook andere experimentele voordelen.
"Als je neutronendiffractie gebruikt, heb je geen stralingsschade, zodat je je studie bij kamertemperatuur kunt doen, "zei McKenna. "Bovendien, bevriezingskristallen kunnen het medicijn en het enzym veranderen, het introduceren van een verkeerd beeld in de studie, terwijl studies bij kamertemperatuur meer lijken op de omgeving waarin het medicijn zal worden gebruikt."
 Herhalingssleutel tot zelfgenezing, flexibele medische hulpmiddelen
Herhalingssleutel tot zelfgenezing, flexibele medische hulpmiddelen Onderzoekers produceren goedkope handdesinfecterende middelen uit afval
Onderzoekers produceren goedkope handdesinfecterende middelen uit afval Nieuw voedsel invriesconcept verbetert kwaliteit, verhoogt de veiligheid, vermindert energieverbruik
Nieuw voedsel invriesconcept verbetert kwaliteit, verhoogt de veiligheid, vermindert energieverbruik Op koolstof gebaseerde katalysatoren die worden gebruikt voor Fischer-Tropsch-synthese
Op koolstof gebaseerde katalysatoren die worden gebruikt voor Fischer-Tropsch-synthese Wat is een coëfficiënt in een chemische formule?
Wat is een coëfficiënt in een chemische formule?
 Lichtere bestrating maakt steden echt cool als het goed wordt gedaan
Lichtere bestrating maakt steden echt cool als het goed wordt gedaan Tot 35 doden als tyfoon Hagibis Japan teistert (update)
Tot 35 doden als tyfoon Hagibis Japan teistert (update) Gemeenschappelijke spinnen in Massachusetts
Gemeenschappelijke spinnen in Massachusetts  IceBridge lanceert twee sets antarctische vluchten
IceBridge lanceert twee sets antarctische vluchten Voorjaar 2020 Arctisch ozongat waarschijnlijk veroorzaakt door recordhoge oppervlaktetemperaturen in het noorden van de Stille Oceaan
Voorjaar 2020 Arctisch ozongat waarschijnlijk veroorzaakt door recordhoge oppervlaktetemperaturen in het noorden van de Stille Oceaan
Hoofdlijnen
- Thailand neemt grote slagtanden van olifanten in beslag ter waarde van meer dan $ 450, 000
- Procedures voor elektroforese van gel
- Slimme app gebruikt smartphonecamera om plantensoorten te identificeren
- Waar bevinden zich lipiden in het lichaam?
- Studie kijkt naar de invloed van woonwerven op voedselwebben
- Voelen planten pijn?
- De allereerste tagging van Amazone-dolfijnen om de inspanningen voor natuurbehoud te stimuleren
- Hoe de cellen van planten, dieren en eencellige organismen te vergelijken
- Projectideeën voor biotechnologie
- Wiskundige modellering laat zien hoe chitinase, een moleculaire monorail, gehoorzaamt aan eenrichtingsverkeer
- Een solvatatieproces stap voor stap volgen

- Softwarebibliotheek voor snellere verwerking van chemische reacties

- Wetenschappers rekruteren nieuwe atoomzwaargewichten in gerichte strijd tegen kanker

- Wetenschappers ontwikkelen zeer gevoelige moleculaire optische druksensor

 Wat zijn de toepassingen van discrete wiskunde?
Wat zijn de toepassingen van discrete wiskunde?  Van het kwantumniveau tot de auto-accu
Van het kwantumniveau tot de auto-accu Nieuwe peiling onthult publieke ontkoppeling over voedsel en klimaatverandering
Nieuwe peiling onthult publieke ontkoppeling over voedsel en klimaatverandering Afhaalmaaltijden - de milieukosten van het verpakken van onze favoriete fastfood
Afhaalmaaltijden - de milieukosten van het verpakken van onze favoriete fastfood Nieuwe oproep om oude verhalen te onderzoeken:studie naar modellering van infectieziekten doet twijfel rijzen over de impact van Justinianic Plagues
Nieuwe oproep om oude verhalen te onderzoeken:studie naar modellering van infectieziekten doet twijfel rijzen over de impact van Justinianic Plagues Marcheren voor verandering:Womens March 2017 kreeg overwegend positieve online steun
Marcheren voor verandering:Womens March 2017 kreeg overwegend positieve online steun Nieuwe klassen van topologische kristallijne isolatoren met anomalie van oppervlakterotatie
Nieuwe klassen van topologische kristallijne isolatoren met anomalie van oppervlakterotatie UFO-hoaxes
UFO-hoaxes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

