
Wetenschap
Onderzoekers ontdekken sleutelfuncties van therapeutisch veelbelovende jumbovirussen
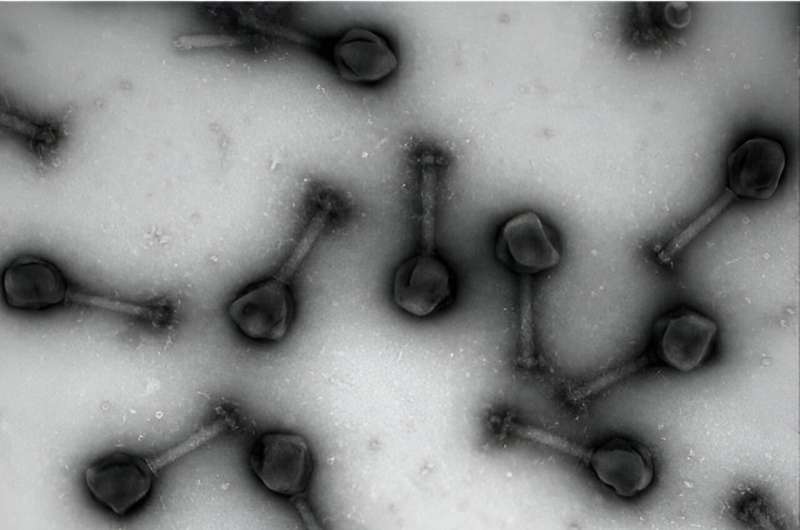
Antibiotische medicijnen werden in het begin van de 20e eeuw een populaire behandeling voor bacteriële infecties en ontpopten zich als een transformerend hulpmiddel in de menselijke gezondheid. Halverwege de eeuw werden er regelmatig nieuwe antibiotica ontwikkeld in de gouden eeuw van het medicijn.
Maar toen ontwikkelden zich bacteriën. Ze vonden nieuwe manieren om antibioticabehandelingen te omzeilen, waardoor veel behandelingen nutteloos werden. Terwijl nieuwe bronnen van antibiotica opdroogden, escaleerden bacteriële infecties tot de huidige mondiale gezondheidscrisis van antibioticaresistentie.
Wetenschappers kijken nu naar een ongewone bondgenoot, virussen, om deze toenemende dreiging het hoofd te bieden. Onlangs hebben onderzoekers zich geconcentreerd op virussen die bekend staan als bacteriofagen als een nieuw hulpmiddel om antibioticaresistente bacteriën te behandelen en te ontwapenen. Er is speciale aandacht besteed aan 'jumbo'-fagen – virussen waarvan onlangs is ontdekt dat ze over extreem grote genomen beschikken – die kunnen worden gebruikt als speciale toedieningsmiddelen die niet alleen bacteriën kunnen doden, maar ook kunnen worden ontwikkeld om antibiotica rechtstreeks aan de infectiebron af te geven. P>
Maar om nieuwe therapieën via fagen te kunnen leveren, moeten wetenschappers eerst de buitengewone biologische samenstelling en mechanismen in deze mysterieuze virussen begrijpen.
Onderzoekers van de University of California San Diego School of Biological Sciences en hun collega's van het Innovative Genomics Institute van UC Berkeley en de Chulalongkorn Universiteit in Bangkok hebben een substantiële stap voorwaarts gezet in het ontcijferen van verschillende sleutelfuncties binnen jumbofagen.
"Deze jumbofagen hebben grote genomen die in theorie zouden kunnen worden gemanipuleerd om ladingen te vervoeren die bacteriën effectiever doden", zegt Joe Pogliano, professor aan de UC San Diego aan de School of Biological Sciences en senior auteur van een nieuw artikel gepubliceerd in de Proceedings van de Nationale Academie van Wetenschappen . "Het probleem is dat hun genoom ingesloten is en dus niet gemakkelijk toegankelijk is. Maar nu hebben we enkele van de belangrijkste elementen ervan ontdekt."
Zoals beschreven in het artikel concentreerde het onderzoek onder leiding van afgestudeerde student Chase Morgan van de School of Biological Sciences zich op jumbo Chimalliviridae-fagen waarvan werd vastgesteld dat ze zich in bacteriën repliceerden door een compartiment te vormen dat lijkt op de kern in de cellen van mensen en andere levende organismen. Het kernachtige compartiment van de Chimalliviridae scheidt en importeert selectief bepaalde eiwitten waardoor het zich kan vermenigvuldigen in de gastheerbacterie. Maar hoe dit proces zich ontvouwt was een raadselachtig onderdeel van het proces.
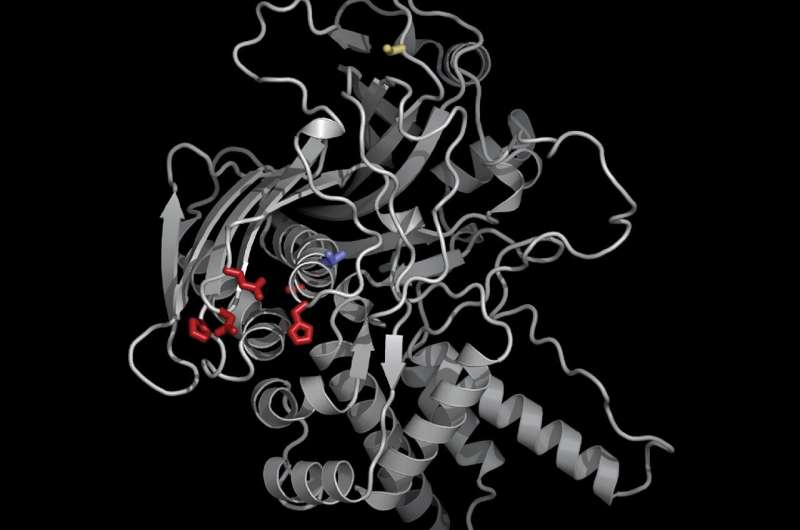
Met behulp van nieuwe genetische en celbiologische hulpmiddelen identificeerden Morgan en zijn collega's een sleuteleiwit, dat ze 'eiwitimporteur van Chimallivirussen A' of PicA noemden, dat fungeert als een soort uitsmijter in nachtclubs, die selectief eiwitten verhandelt door toegang te verlenen tot de kern voor sommige, maar weigeren de toegang voor anderen. Ze ontdekten dat PicA de transport van vrachteiwitten door de beschermende schil van de faagkern coördineert.
“Alleen al het feit dat dit virus in staat is om deze ongelooflijk complexe structuur en transportsysteem op te zetten is echt verbazingwekkend en zoiets hebben we nog niet eerder gezien”, aldus Morgan. ‘Wat wij beschouwen als complexe biologie is meestal gereserveerd voor hogere levensvormen bij mensen en onze tienduizenden genen, maar hier zien we functioneel analoge processen in een relatief klein viraal genoom van slechts ongeveer 300 genen. Het is waarschijnlijk de eenvoudigste selectieve biologie. transportsysteem dat wij kennen."
Met behulp van CRISPRi-ART, een programmeerbaar RNA-hulpmiddel voor het bestuderen van genomen, konden de onderzoekers aantonen dat PicA een essentieel onderdeel is van het ontwikkeling- en replicatieproces van de Chimalliviridae-kern.
"Zonder de eenvoud en veelzijdigheid van op RNA gerichte CRISPR-technologieën zou het direct stellen en beantwoorden van deze vragen vrijwel onmogelijk zijn. We zijn erg enthousiast om te zien hoe deze hulpmiddelen de mysteries ontrafelen die worden gecodeerd door faaggenomen", zegt co-auteur Ben Adler, een van de onderzoekers. postdoctoraal onderzoeker onder leiding van Nobelprijswinnaar CRISPR-pionier Jennifer Doudna.
Bacteriën en virussen zijn al miljarden jaren verwikkeld in een soort wapenwedloop, waarbij ze allemaal evolueren om de aanpassingen van de ander tegen te gaan. De onderzoekers zeggen dat het geavanceerde PicA-transportsysteem het resultaat is van die intense, voortdurende evolutionaire concurrentie. Het systeem is geëvolueerd om zowel zeer flexibel als zeer selectief te zijn, waardoor alleen de belangrijkste nuttige elementen in de kern mogelijk zijn. Zonder het PicA-systeem zouden de verdedigingseiwitten van de bacterie zich een weg naar binnen banen en het replicatieproces van het virus saboteren.
Dergelijke informatie is van vitaal belang omdat wetenschappers van het Emerging Pathogens Initiative en het Center for Innovative Phage Applications and Therapeutics van UC San Diego ernaar streven de basis te leggen om fagen uiteindelijk genetisch te programmeren om een verscheidenheid aan dodelijke ziekten te behandelen.
"We hadden echt geen idee hoe het eiwitimportsysteem werkte of welke eiwitten er eerder bij betrokken waren, dus dit onderzoek is de eerste stap in het begrijpen van een sleutelproces dat cruciaal is voor het succesvol repliceren van deze fagen", aldus de School of Biological Sciences. afgestudeerde studente Emily Armbruster, co-auteur van een paper. "Hoe meer we deze essentiële systemen begrijpen, hoe beter we fagen kunnen ontwikkelen voor therapeutisch gebruik."
Toekomstige doelwitten voor dergelijke genetisch geprogrammeerde virussen zijn onder meer de Pseudomonas aeruginosa-bacteriën, waarvan bekend is dat ze potentieel dodelijke infecties veroorzaken en risico's met zich meebrengen voor patiënten in ziekenhuizen. Andere veelbelovende doelwitten zijn onder meer E. coli en Klebsiella, die chronische en terugkerende infecties kunnen veroorzaken en in sommige gevallen in de bloedbaan terecht kunnen komen, wat levensbedreigend kan zijn.