
Wetenschap
Hoe E. coli de kracht krijgt om urineweginfecties te veroorzaken
Door hun anatomie zijn vrouwen bijzonder gevoelig voor urineweginfecties, waarbij bijna de helft er ooit in hun leven mee te maken krijgt.
Wetenschappers proberen al tientallen jaren uit te vinden hoe bacteriën voet aan de grond krijgen bij verder gezonde mensen, waarbij ze alles onderzoeken, van hoe de microben naar binnen bewegen en zich aan de binnenkant van de blaas hechten, tot hoe ze hun gifstoffen inzetten om ongemakkelijke en vaak pijnlijke symptomen te veroorzaken.
Onderzoek gepubliceerd in PNAS onderzoekt hoe de bacterie Escherichia coli, of E. coli, verantwoordelijk voor de meeste urineweginfecties, in staat is de voedingsstoffen van de gastheer te gebruiken om zich tijdens infectie in een buitengewoon snel tempo voort te planten, ondanks de vrijwel steriele omgeving van verse urine.
Onderzoekers die in het laboratorium van Harry Mobley, Ph.D., aan de University of Michigan Medical School werkten, begonnen met het kijken naar mutante stammen die niet zo goed waren in het repliceren in muismodellen om bacteriële genen te identificeren die belangrijk kunnen zijn voor het vaststellen van infecties.
Daarbij identificeerden ze een groep genen die transportsystemen controleren als cruciaal.
"Als bacteriën iets nodig hebben om te groeien, bijvoorbeeld een aminozuur, kunnen ze dat op twee manieren verkrijgen", legt Mobley uit, de Frederick G. Novy Distinguishes Professor in Microbiologie en Immunologie.
"Ze kunnen het zelf maken, of ze kunnen het van hun gastheer stelen met behulp van wat wij een transportsysteem noemen."
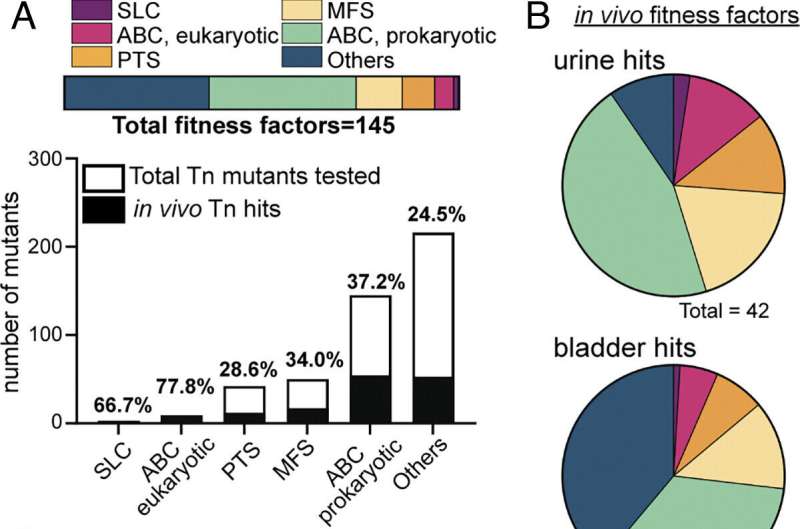
Uit hun eerdere screening van genexpressie bleek dat bijna 25% van de bacteriële genen bestemd was voor replicatietactieken, waaronder transportsystemen voor specifieke aminozuren, die E. coli gebruikt om duizenden moleculen per seconde binnen te brengen, aldus Mobley.
Eerste auteur Allyson Shea, Ph.D., een voormalig lid van Mobley's laboratorium en nu assistent-professor in de microbiologie en immunologie aan de Universiteit van South Alabama, verwees naar een bibliotheek met transporteiwitten van E. coli met andere soorten UTI-pathogenen om kijk welke belangrijk waren voor infectie. Ze ontdekte dat een type transporter genaamd ABC-transporters (voor ATP-bindende cassette) van cruciaal belang bleek te zijn.
Vervolgens bevestigde ze met behulp van orgaanagar gemaakt uit de urinewegen van muizen dat ABC-transporters essentieel waren voor infectie. Veel bacteriestammen die deze importsystemen voor voedingsstoffen misten, waren defect voor de groei op blaas- en nierorgaan-agar.
"Het lijkt erop dat bacteriën investeren in deze energie-dure ATP-transportsystemen om een hogere affiniteit te hebben voor de energiebronnen waarin ze geïnteresseerd zijn", zegt Shea.
"Deze systemen zijn heel erg goed in het binnenkrijgen van voedingsstoffen in de cel."
De bevindingen, zo merkt Mobley op, openen wegen voor de ontwikkeling van nieuwe therapieën – wat vooral belangrijk is in een tijdperk van toenemende antibioticaresistentie.
"Als je deze transportsystemen remt, kun je misschien de snelle groei van deze bacteriën remmen", zei hij.
Dat zal niet eenvoudig zijn, merkt Shea op, omdat bacteriën meerdere back-upsystemen hebben ontwikkeld voor deze belangrijke klasse transporteurs.
"Het mooie van deze ATP-bindende familie is dat ze allemaal een ATP-bindende subeenheid hebben die het transportsysteem de energie geeft die het nodig heeft om voedingsstoffen door het celmembraan te krijgen."
Deze subeenheid zou potentieel een doelwit kunnen zijn om de hele familie van transporters disfunctioneel te maken.
Hoewel dit niet noodzakelijkerwijs antibiotica zou vervangen, zegt ze, zou het de groei kunnen vertragen, zodat antibiotica en het immuunsysteem van de gastheer de insecten beter zouden kunnen stoppen.
Andere auteurs zijn onder meer Valerie S. Forsyth, Jolie A. Stocki, Taylor J. Mitchell, Arwen E. Frick-Cheng, Sara N. Smith en Sicilië L. Hardy.