
Wetenschap
Hoe de zebravis een gebroken hart repareert
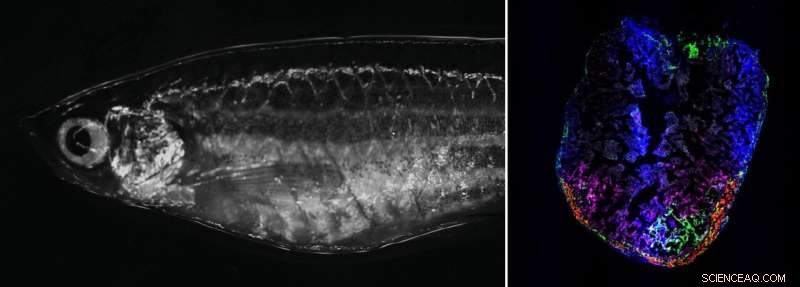
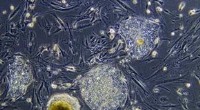
Rechts:Volwassen zebravis in de helderveldmicroscoop. Links:Zebravishart 7 dagen na cryoletsel. Tijdelijk geactiveerde fibroblasten lokaliseren naar het letselgebied. Krediet:Panáková Lab, MDC
Een MDC-onderzoeksteam onder leiding van Jan Philipp Junker en Daniela Panáková heeft ontdekt dat zebravissen hartweefsel kunnen regenereren na een verwonding. Bindweefselcellen spelen een belangrijke rol in het proces door tijdelijk in een geactiveerde toestand te komen, zoals het team meldt in Nature Genetics .
Wanneer een persoon een hartaanval krijgt en niet snel genoeg wordt behandeld, worden hartspiercellen (cardiomyocyten) beschadigd door een gebrek aan zuurstof en beginnen ze af te sterven. Er vormt zich dan littekenweefsel en omdat we geen nieuwe hartspiercellen kunnen aanmaken, kan het hart niet meer zo goed pompen als zou moeten. De dingen zijn heel anders bij lagere gewervelde dieren zoals de zebravis, die organen kan regenereren, inclusief het hart.
"We wilden weten hoe deze kleine vis dat doet en of we ervan kunnen leren", zegt professor Jan Philipp Junker, hoofd van het Quantitative Developmental Biology Lab van het Berlin Institute for Medical Systems Biology (BIMSB), onderdeel van de Max Delbrück Centrum voor Moleculaire Geneeskunde in de Helmholtz Association (MDC) in Berlijn. In samenwerking met Dr. Daniela Panáková, die het Electrochemical Signaling in Development and Disease Lab bij het MDC leidt, simuleerden de onderzoekers myocardinfarctverwondingen in de harten van hun zebravis. Met behulp van eencellige analyses en boomstambomen volgden ze de regeneratie van de cardiomyocyten. Ze hebben hun observaties nu gepubliceerd in het tijdschrift Nature Genetics .
Mensenharten stoppen kort voor regeneratie
De onderzoekers begonnen door een koude naald een paar seconden onder een microscoop tegen het hart van een millimeter van de zebravis te houden. De naald doodt elk weefsel dat het aanraakt. Net als bij mensen met een hartaanval veroorzaakt dit een ontstekingsreactie, die wordt gevolgd door littekens van bindweefselcellen die bekend staan als fibroblasten. "Verrassend genoeg lijkt de onmiddellijke reactie op de verwonding erg op elkaar. Maar terwijl het proces bij mensen op dat moment stopt, gaat het door in de vissen. Ze vormen nieuwe cardiomyocyten, die kunnen samentrekken", zegt Junker.
"We wilden de signalen identificeren die van andere cellen komen en de regeneratie helpen stimuleren", vervolgt hij. Het team van Junker gebruikte eencellige genomica om in het gewonde hart te zoeken naar cellen die niet voorkomen in een gezond zebravishart. Ze vonden drie nieuwe soorten fibroblasten die tijdelijk in een geactiveerde toestand komen. Hoewel ze uiterlijk identiek zijn aan de andere fibroblasten, kunnen deze geactiveerde cellen een hele reeks extra genen lezen die verantwoordelijk zijn voor de vorming van eiwitten, zoals bindweefselfactoren zoals collageen 12.
Fibroblasten geven het signaal voor regeneratie
Bij mensen wordt littekenvorming (of fibrose) gezien als een obstakel voor het regenereren van het hart. Maar de fibroblasten blijken belangrijk te zijn voor het proces zodra ze in hun tijdelijk geactiveerde toestand komen. Hoe belangrijk ze zijn, werd duidelijk toen Panáková een genetische truc gebruikte om de collageen 12 tot expressie brengende fibroblasten in de zebravis uit te schakelen. Het resultaat:geen regeneratie. Junker vindt het logisch dat fibroblasten verantwoordelijk zijn voor het geven van herstelsignalen:"Ze vormen zich tenslotte precies op de plaats van de verwonding", zegt hij.
Om de bron van deze geactiveerde fibroblasten te identificeren, produceerde het team van Junker celstambomen met behulp van een techniek genaamd LINNAEUS, die zijn laboratorium in 2018 ontwikkelde. LINNAEUS werkt met genetische littekens die gezamenlijk fungeren als een streepjescode voor de oorsprong van elke cel. "We maken deze streepjescode met behulp van een genetische schaar van CRISPR-Cas9. Als twee cellen na een verwonding dezelfde streepjescodevolgorde hebben, betekent dit dat ze verwant zijn", legt Junker uit. De onderzoekers identificeerden twee bronnen van tijdelijk geactiveerde fibroblasten:de buitenste laag van het hart (epicardium) en de binnenste laag (endocardium). Cellen die collageen 12 produceren, werden uitsluitend in het epicardium gevonden.
Verschillende disciplines werkten nauw samen aan het onderzoek
Meerdere MDC-onderzoekers werkten gedurende het hele onderzoek samen - van de experimenten met de vissen tot de genetische analyses tot de bio-informatische interpretatie van de resultaten. "Voor mij was het meest opwindende om te zien hoe goed onze disciplines elkaar aanvullen en hoe we de resultaten van bio-informatica op een levend dier konden verifiëren", zegt Sara Lelek, hoofdauteur van het onderzoek en verantwoordelijk voor het dier. testen. "Het was een groot project waardoor we allemaal onze expertise konden bijdragen. Ik denk dat dat de reden is waarom de studie zo uitgebreid en zo nuttig is voor veel onderzoekers."
Dr. Bastiaan Spanjaard, ook hoofdauteur, is het ermee eens:"Omdat we zulke verschillende expertisegebieden hadden, moesten we onze experimenten en analyses vaak aan elkaar uitleggen. Hartregeneratie is een complex proces dat door veel verschillende dingen wordt beïnvloed. De experimenten produceerden enorme hoeveelheden data. Het was een enorme uitdaging om de juiste biologische signalen eruit te filteren."
Het is nog steeds onduidelijk of beschadigde harten bij zoogdieren zoals mensen en muizen de nodige signalen missen of het vermogen om de signalen te lezen. Als de signalen ontbreken, kan op termijn medicatie worden ontwikkeld om ze te simuleren. Maar, zegt Junker, het zou veel moeilijker zijn om een manier te vinden om signaalinterpretatie na te bootsen.
Fibroblasten helpen ook om nieuwe bloedvaten te vormen
De onderzoekers willen nu nader kijken naar de genen die de tijdelijk geactiveerde fibroblasten vooral vaak lezen. Ze weten dat veel van de genen in kwestie belangrijk zijn voor het vrijgeven van eiwitten in de omgeving. En dit kunnen factoren zijn die ook cardiomyocyten beïnvloeden. En het eerste bewijs suggereert dat de geactiveerde fibroblasten niet alleen de regeneratie van het hart bevorderen; ze helpen ook om nieuwe bloedvaten te vormen die het hart van zuurstof voorzien.
 Een topjaar voor farma
Een topjaar voor farma Onderzoekers onthullen op oxygenaat gebaseerde routes bij de omzetting van syngas via bifunctionele oxide-zeolietkatalysatoren
Onderzoekers onthullen op oxygenaat gebaseerde routes bij de omzetting van syngas via bifunctionele oxide-zeolietkatalysatoren Verbeterde afvalscheiding door superstabiele magnetische vloeistof
Verbeterde afvalscheiding door superstabiele magnetische vloeistof Wanneer FRETing over kankerbiomarkers niet zal werken, focus in plaats daarvan op knipperen
Wanneer FRETing over kankerbiomarkers niet zal werken, focus in plaats daarvan op knipperen Hoge precisie, on-site analyse van edele metalen in metallurgische afvallozingen
Hoge precisie, on-site analyse van edele metalen in metallurgische afvallozingen
 Natuurbeschermers botsen over de weg vooruit ondanks het delen van kerndoelen, studie vondsten
Natuurbeschermers botsen over de weg vooruit ondanks het delen van kerndoelen, studie vondsten Orkaan Oscar op satellietbeelden:een eenogig klein monster met een staart
Orkaan Oscar op satellietbeelden:een eenogig klein monster met een staart Tornado-waarschuwingen geven een pad om voorspellingen te verbeteren
Tornado-waarschuwingen geven een pad om voorspellingen te verbeteren Branden die Brits-Columbia overweldigen; rook verstikt de lucht
Branden die Brits-Columbia overweldigen; rook verstikt de lucht Nieuw onderzoek vindt dat tornado's van de grond af worden gevormd, in tegenstelling tot de populaire gedachte
Nieuw onderzoek vindt dat tornado's van de grond af worden gevormd, in tegenstelling tot de populaire gedachte
Hoofdlijnen
- Burn-out eist zware financiële tol van diergeneeskunde
- Welke vormen over het midden van een cel nabij het einde van Telophase?
- Burgerwetenschappers helpen bij het vastleggen van wilde zoogdieren op camera
- Stappen van DNA-transcriptie
- Een nieuwe rol voor insuline als vitale factor bij het in stand houden van stamcellen
- Onderzoek toont aan dat menselijke activiteit het gedrag van bobcat beïnvloedt
- Wat is Ashwagandha?
- Ouderleeftijd kan een belangrijke factor zijn om volbloedpaarden als eerste voorbij de post te helpen
- Antibioticaresistente infecties bij huisdieren
- Beoordeling van Vaccinium-veredelingsonderzoek en vooruitzichten voor de toekomstige richtingen
- Hoe toxoplasmose immuuncellen uitbuit om de hersenen te bereiken?
- Het bestuderen van roofzuchtig gedrag in het bacterierijk
- Aanwijzingen voor de aangeboren resistentie tegen geneesmiddelen van een cacaofermenterende ziekteverwekker

- Waarom zouden wetenschappers een hybride mens-koe-embryo willen creëren?
 Wat is 5 Pence waard?
Wat is 5 Pence waard?  Planeten ter grootte van de aarde met statistisch veel water rond rode dwergen
Planeten ter grootte van de aarde met statistisch veel water rond rode dwergen Blauwe wijn? Een vintage met thee? Startup Spanje schudt de boel wakker
Blauwe wijn? Een vintage met thee? Startup Spanje schudt de boel wakker Kunnen zuurneutraliserende levensvormen bewoonbare holten maken in Venuswolken?
Kunnen zuurneutraliserende levensvormen bewoonbare holten maken in Venuswolken? Kunnen olie en water mengen?
Kunnen olie en water mengen? Supermaterialen uit de magnetron
Supermaterialen uit de magnetron Transparante coatings voor alledaagse toepassingen
Transparante coatings voor alledaagse toepassingen Energieopwekkende doek kan batterijen in draagbare apparaten vervangen
Energieopwekkende doek kan batterijen in draagbare apparaten vervangen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

