Wetenschap
Wanneer FRETing over kankerbiomarkers niet zal werken, focus in plaats daarvan op knipperen
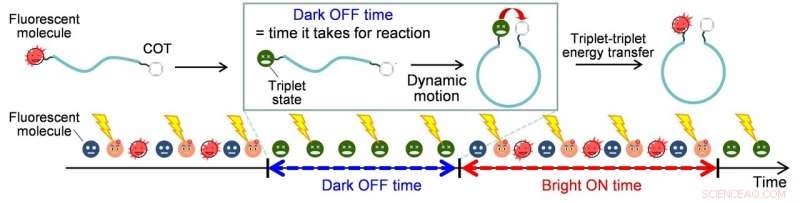
Schematische weergave van het knipperen van de fluorescentie gecontroleerd door tripletvorming en triplet-triplet energieoverdracht. Krediet:Universiteit van Osaka
Fluorescentiespectroscopie is onmisbaar in de biomedische diagnostiek. Je kunt fluorescentie aanzetten als een zaklamp in een donkere kamer. Een diagnostische test kan worden ontworpen om te labelen, bijvoorbeeld, een specifiek molecuul DNA met een fluorescerende sonde. Als dat specifieke DNA-molecuul aanwezig is, je ziet fluorescentie of een verandering in de fluorescentie.
Soms stopt een anders fluorescerend molecuul voor een korte tijd met het uitstralen van licht. Dit wordt fluorescentie knipperen genoemd, wat het moeilijk kan maken om biomoleculen te detecteren in de ultralage concentraties die nodig zijn voor ziektediagnostiek. Een manier om tegelijkertijd het knipperen voor diagnostiek te verminderen en bruikbare biochemische informatie uit het knipperen te halen voor basisonderzoek zou het beste van twee werelden zijn.
In een recent gepubliceerd onderzoek in Angewandte Chemie , onderzoekers van de Universiteit van Osaka gebruikten een bekend molecuul, afgekort als COT - een fotostabilisator - om het knipperen van de fluorescentie in biochemische tests te moduleren. De onderzoekers gebruikten COT om de architectuur van DNA-moleculen te onderzoeken en om een kanker-RNA-biomarker te detecteren bij ultralage concentraties.
"COT onderdrukt het knipperen van de fluorescentie, en zo de fluorescentie verhoogt, door in fysiek contact te komen met de fluorofoor, " legt Jie Xu uit, hoofdauteur. "In tegenstelling tot, het moduleren van emissie door een veelgebruikte techniek die bekend staat als fluorescentieresonantie-energieoverdracht, TOBBEN, werkt alleen over veel langere afstanden - in het gebied van 1 tot 10 nanometer - en alleen op een nanoseconde tijdschaal."
De onderzoekers testten hun opstelling eerst op dubbelstrengs DNA met daarin een interne spacer. Toen COT aan het ene uiteinde van de spacer zat en de fluorofoor aan het andere uiteinde, er was meer fluorescentie dan wanneer COT niet aanwezig was. Echter, fluorescentie knipperen was niet volledig geëlimineerd. De onderzoekers maakten hiervan misbruik door te testen hoe de chemische architectuur van de spacer het knipperen moduleert.
"Toenemende lengte van de spacer en toenemende pi-stapelinteracties - niet-covalente interacties tussen aromatische ringen - in de spacer verhoogde de tijd van de fluorofoor in de 'uit'-toestand, " zegt Kiyohiko Kawai, senior auteur. "FRET kan geen informatie geven over biomoleculaire dynamiek over deze subnanometerafstanden."
De onderzoekers ontdekten vervolgens ultrakleine concentraties van een RNA-molecuul dat een biomarker is voor veel kankers. Ze bevestigden eerst een fluorescerende sonde met COT op een glasplaatje. De sonde was zodanig ontworpen dat binding aan de RNA-biomarker de fluorescentie van de sonde zou verhogen.
"Binding aan het doel-RNA verminderde de tijd van de sonde in de uit-stand met de helft, " zegt Xu. "Dit biedt een duidelijk middel om een kankerbiomarker te detecteren."
Detectie van een ziektegerelateerd biomolecuul bij ultralage concentraties, mogelijk gemaakt met deze techniek, kan een manier zijn om een ziekte in een vroeg stadium te diagnosticeren en de behandeling te vergemakkelijken. Verder, veel fundamentele biochemische onderzoeksstudies zijn mogelijk nu onderzoekers moleculaire bewegingen op subnanometerschaal en over brede tijdschalen kunnen onderzoeken.
 Handdesinfecterend middel opnieuw ontwerpen en doneren 7, 000 gallons om COVID-19 te bestrijden
Handdesinfecterend middel opnieuw ontwerpen en doneren 7, 000 gallons om COVID-19 te bestrijden Polymeerkristallen vormen de sleutel tot recordbrekend energietransport
Polymeerkristallen vormen de sleutel tot recordbrekend energietransport Een duurzame nieuwe oplossing voor veroudering, corrosieve infrastructuur
Een duurzame nieuwe oplossing voor veroudering, corrosieve infrastructuur Onderzoek toont aan dat keramiek kan vervormen als metalen als het onder een elektrisch veld wordt gesinterd
Onderzoek toont aan dat keramiek kan vervormen als metalen als het onder een elektrisch veld wordt gesinterd Superdiamond koolstof-borium kooien kunnen verschillende eigenschappen opvangen en aanboren
Superdiamond koolstof-borium kooien kunnen verschillende eigenschappen opvangen en aanboren
 Nieuwe methode voor het meten van RNAi-bestrijdingsmiddel in de bodem
Nieuwe methode voor het meten van RNAi-bestrijdingsmiddel in de bodem Vrees voor lekkende giftige brandstof als zeedieren sterven in ecologische ramp in Rusland
Vrees voor lekkende giftige brandstof als zeedieren sterven in ecologische ramp in Rusland Wetenschappers vinden hoogste gehalte aan microplastics ooit op zeebodem
Wetenschappers vinden hoogste gehalte aan microplastics ooit op zeebodem Zeespiegelverandering in Zuidoost-Azië 6, 000 jaar geleden heeft gevolgen voor vandaag
Zeespiegelverandering in Zuidoost-Azië 6, 000 jaar geleden heeft gevolgen voor vandaag Voedselsystemen zijn voer voor het terugdringen van de milieueffecten van steden
Voedselsystemen zijn voer voor het terugdringen van de milieueffecten van steden
Hoofdlijnen
- Ideeën voor de dingen Kinderen kunnen met een microscoop bekijken
Kinderen zijn vaak nieuwsgierig naar de wereld om hen heen. Een manier om deze nieuwsgierigheid aan te moedigen, is om ze een manier te bieden om de natuur op een nieuwe en intensiev
- Nieuwe mierenvogelsoort ontdekt in Peru
- Onderzoekers ontwikkelen een gel voor het kweken van grote hoeveelheden neurale stamcellen
- Plasticity Cell Definition
- Verschil tussen plantaardige en dierlijke celdeling
- Het overdrachtspotentieel van vliegen kan groter zijn dan gedacht, onderzoekers zeggen:
- Nieuw inzicht in unieke plantchemicaliën kan toekomstige medicijnontwikkeling informeren
- Beperkingen Enzymen die worden gebruikt in DNA-vingerafdrukken
- Grazende paarden op betere weiden
 Berichten over toename corruptie in Nigeria na film- en tekstcampagne
Berichten over toename corruptie in Nigeria na film- en tekstcampagne Video:Europese robotarm klaar voor de ruimte
Video:Europese robotarm klaar voor de ruimte Enorme ongelijkheden in het onderwijs blootgelegd tijdens pandemie
Enorme ongelijkheden in het onderwijs blootgelegd tijdens pandemie IPad mini review:in een tijdperk van grotere iPhones, heeft Apples kleine tablet nog zin?
IPad mini review:in een tijdperk van grotere iPhones, heeft Apples kleine tablet nog zin? Natuurkundigen springen over versnellers met ultrahoge energetische kosmische straling
Natuurkundigen springen over versnellers met ultrahoge energetische kosmische straling Vaardigheden zoals het opsporen van onzin kunnen kinderen helpen cyberbeveiligingsuitdagingen het hoofd te bieden
Vaardigheden zoals het opsporen van onzin kunnen kinderen helpen cyberbeveiligingsuitdagingen het hoofd te bieden Stroomstoringen blijven voor miljoenen aanhouden terwijl een nieuwe ijzige storm opdoemt
Stroomstoringen blijven voor miljoenen aanhouden terwijl een nieuwe ijzige storm opdoemt Gehele getallen omzetten in percentages
Gehele getallen omzetten in percentages
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com