
Wetenschap
Oude scheikunde kan verklaren waarom levende wezens ATP gebruiken als de universele energievaluta
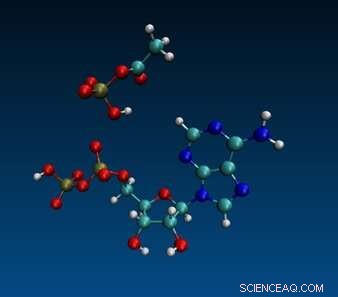
Moleculaire dynamische simulatie van ADP en acetylfosfaat. Krediet:Aaron Halpern, UCL (CC-BY 4.0, creativecommons.org/licenses/by/4.0/)
Volgens een nieuwe studie die op 4 oktober in het open access-tijdschrift PLOS Biology is gepubliceerd, kan een eenvoudige verbinding met twee koolstofatomen een cruciale speler zijn geweest in de evolutie van het metabolisme vóór de komst van cellen. , door Nick Lane en collega's van University College London, U.K. De bevinding werpt mogelijk licht op de vroegste stadia van prebiotische biochemie en suggereert hoe ATP de universele energiedrager van al het cellulaire leven vandaag de dag werd.
ATP, adenosinetrifosfaat, wordt door alle cellen gebruikt als energietussenproduct. Tijdens cellulaire ademhaling wordt energie opgevangen wanneer een fosfaat wordt toegevoegd aan ADP (adenosinedifosfaat) om ATP te genereren; splitsing van dat fosfaat maakt energie vrij om de meeste soorten cellulaire functies aan te drijven. Maar het helemaal opnieuw opbouwen van de complexe chemische structuur van ATP is energie-intensief en vereist zes afzonderlijke ATP-gestuurde stappen; hoewel overtuigende modellen prebiotische vorming van het ATP-skelet mogelijk maken zonder energie van reeds gevormd ATP, suggereren ze ook dat ATP waarschijnlijk vrij schaars was en dat een andere verbinding een centrale rol kan hebben gespeeld bij de omzetting van ADP naar ATP in dit stadium van evolutie.
De meest waarschijnlijke kandidaat, geloofden Lane en collega's, was de twee-koolstofverbinding acetylfosfaat (AcP), die tegenwoordig in zowel bacteriën als archaea fungeert als een metabool tussenproduct. Van AcP is aangetoond dat het ADP fosforyleert tot ATP in water in aanwezigheid van ijzerionen, maar na die demonstratie bleven er tal van vragen over, waaronder of andere kleine moleculen ook zouden kunnen werken, of AcP specifiek is voor ADP of in plaats daarvan net zo zou kunnen functioneren. goed samengaat met difosfaten van andere nucleosiden (zoals guanosine of cytosine), en of ijzer uniek is in zijn vermogen om ADP-fosforylering in water te katalyseren.
In hun nieuwe studie hebben de auteurs al deze vragen onderzocht. Op basis van gegevens en hypothesen over de chemische omstandigheden van de aarde voordat het leven ontstond, testten ze het vermogen van andere ionen en mineralen om ATP-vorming in water te katalyseren; geen enkele was bijna zo effectief als ijzer. Vervolgens testten ze een panel van andere kleine organische moleculen op hun vermogen om ADP te fosforyleren; geen enkele was zo effectief als AcP, en slechts één andere (carbamoylfosfaat) had enige significante activiteit. Ten slotte toonden ze aan dat geen van de andere nucleosidedifosfaten een fosfaat van AcP accepteerde.
Door deze resultaten te combineren met moleculair-dynamische modellering, stellen de auteurs een mechanistische verklaring voor voor de specificiteit van de ADP/AcP/ijzerreactie, waarbij ze veronderstellen dat de kleine diameter en hoge ladingsdichtheid van het ijzerion, gecombineerd met de conformatie van het tussenproduct gevormd wanneer de drie komen samen en bieden een "precies juiste" geometrie waarmee AcP's fosfaat van partner kan wisselen, waardoor ATP wordt gevormd.
"Onze resultaten suggereren dat AcP de meest plausibele voorloper is van ATP als biologische fosforylator," zegt Lane, "en dat de opkomst van ATP als de universele energievaluta van de cel niet het resultaat was van een 'bevroren ongeluk', maar ontstond van de unieke interacties van ADP en AcP. Na verloop van tijd, met de opkomst van geschikte katalysatoren, zou ATP uiteindelijk AcP als een alomtegenwoordige fosfaatdonor kunnen verdringen, en de polymerisatie van aminozuren en nucleotiden bevorderen om RNA, DNA en eiwitten te vormen."
Hoofdauteur Silvana Pinna voegt toe:"ATP speelt zo'n centrale rol in het metabolisme dat ik dacht dat het mogelijk zou zijn om het onder prebiotische omstandigheden uit ADP te vormen. Maar ik dacht ook dat verschillende fosforylerende middelen en metaalionkatalysatoren zouden werken, vooral diegene die in het leven behouden blijven. Het was zeer verrassend om te ontdekken dat de reactie zo selectief is - in het metaalion, de fosfaatdonor en het substraat - met moleculen die het leven nog steeds gebruikt. Het feit dat dit het beste gebeurt in water onder milde, levenscompatibele omstandigheden is echt heel belangrijk voor de oorsprong van het leven." + Verder verkennen
Zeewater had fosfor kunnen leveren dat nodig is voor opkomend leven
 Methaan-etende microben kunnen de uitstoot van gassen verminderen als de Antarctische ijskappen smelten
Methaan-etende microben kunnen de uitstoot van gassen verminderen als de Antarctische ijskappen smelten Hoe Nepal profiteert als vrouwen actief worden in waterbeheer
Hoe Nepal profiteert als vrouwen actief worden in waterbeheer Definitie van een Aquatisch Ecosysteem
Definitie van een Aquatisch Ecosysteem  Actie op stadsniveau is de juiste manier om emissies aan te pakken, studie toont
Actie op stadsniveau is de juiste manier om emissies aan te pakken, studie toont Florence zou genoeg regen kunnen dumpen om de Chesapeake Bay te vullen
Florence zou genoeg regen kunnen dumpen om de Chesapeake Bay te vullen
Hoofdlijnen
- Onderzoek toont aan dat menselijke activiteit het gedrag van bobcat beïnvloedt
- Hoe jaloezie werkt
- Een pittige oplossing voor het herstellen van oesterriffen
- Wat is een organel in een cel?
- Opnieuw geïntroduceerde buideldieren kunnen een nieuwe bedreiging vormen voor op de grond levende vogels
- Beoordeling van op SERS gebaseerde sensoren voor landbouwtoepassingen
- Cytoplasma: functie en feiten
- Vergeet uw huisdieren niet tijdens koud weer
- Een aap en een virus:een miljoen jaar samen
- Kunstmatige intelligentie gebruikt om bossen in Maines beter te monitoren

- Earth Microbiome Project:het microbioom van... alles in kaart brengen

- Van druppel tot ontdekking
- Wilde zwijnengif veldtesten in Texas, Alabama in 2018

- Campylobacter gebruikt andere organismen als Trojaans paard om nieuwe gastheren te infecteren
 Kometen instortende kliffen en stuiterende rotsblokken
Kometen instortende kliffen en stuiterende rotsblokken De majestueuze orchidee uit Singapore genoemd ter ere van koningin Elizabeth
De majestueuze orchidee uit Singapore genoemd ter ere van koningin Elizabeth Waarom doden we?
Waarom doden we?  Hoe we een congres voor 570 mensen organiseerden zonder plastic te gebruiken
Hoe we een congres voor 570 mensen organiseerden zonder plastic te gebruiken Lage snowpacks van 2014, 2015 kan steeds gebruikelijker worden met warmere omstandigheden
Lage snowpacks van 2014, 2015 kan steeds gebruikelijker worden met warmere omstandigheden Elektrische velden kunnen druppels van oppervlakken duwen
Elektrische velden kunnen druppels van oppervlakken duwen Kinderen op de basisschool kunnen evolutionaire concepten leren die volwassenen stompzinnig maken, nieuwe studie vondsten
Kinderen op de basisschool kunnen evolutionaire concepten leren die volwassenen stompzinnig maken, nieuwe studie vondsten Melkweg zou de thuisbasis kunnen zijn van 100 miljard mislukte sterren
Melkweg zou de thuisbasis kunnen zijn van 100 miljard mislukte sterren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

