
Wetenschap
Volledige structuur van mitochondriaal respiratoir supercomplex gedecodeerd
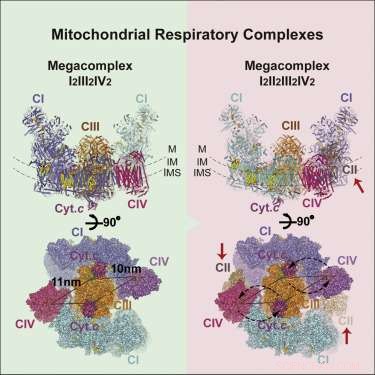
Respiratoire megacomplexe structuur. Credit: Cel (2017). DOI:10.1016/j.cell.2017.07.050
(Phys.org) — Stuk voor stuk, het schakelschema voor elektronentransport in de mitochondriën is bijna voltooid. Elke nieuwe structuur die voor een van de vijf ademhalingscomplexen wordt verkregen, beperkt de samengestelde puzzel verder. Eventueel, grote blokken zijn gerangschikt in hun definitieve plaatsingen. De exacte samenstelling van het grootste blok, het zogenaamde megacomplex, is onderzoekers lang ontgaan. Nutsvoorzieningen, na beeldvorming van 140 afzonderlijke subeenheden tot een resolutie van 3,9 anstrom, de Full Monty is blootgelegd. Onderzoekers beschrijven in Cel precies hoe het menselijke respiratoire megacomplex in elkaar zit en lijkt te functioneren.
Voorbij zijn de eenvoudige dagen. Geen ruwe diagrammen meer met complexen opgesteld in het membraan in een rij van één tot vijf met elektronen en hun mobiele dragers die opeenvolgend van links naar rechts reizen. Kom maar op met de stoichiometrie, en kom maar op met de 2-D. Stoichiometrie betekent dat in werkelijkheid, elk complex is in feite vertegenwoordigd in het megacomplex op een specifiek exemplaarnummer. Deze extra kopieën moeten ergens in een nauwkeurige weergave terechtkomen. Niet alleen dat, maar de kleinere elektronendragers hebben een ruimte nodig om rond te hangen. Ze moeten ook aanwezig zijn in kanalen die ofwel lokaal blijven voor het megacomplex of mogelijk naar anderen diffunderen. De uiteindelijke geometrie zal bepalen waar afzonderlijke elektronenpaden samensmelten of splitsen, en waar ze het meest waarschijnlijk achteruit rijden.
Het beeld van het megacomplex (MC) dat is ontstaan heeft de volgende stoichiometrie:MCI2II2III2IV2. Dit betekent dat complexen I, ik, III, &IV zijn elk in tweevoud aanwezig, terwijl complex V afwezig is. Het is in het membraan geconfigureerd in een cirkelvormige structuur met het dimere CIII in het midden en gevoed door perifere CI- en CIV-complexen. De CII-complexen zijn blijkbaar geen essentiële vereisten voor de kernstructuur, maar er wordt verondersteld dat ze zo nodig in openingen worden geklemd. De auteurs vonden ook bewijs voor een lichtgewicht vertolking van het megacomplex dat soms kan worden geassembleerd met slechts een enkel CI-complex.
De centrale positionering van het CIV-dimeer suggereert een zekere logica. CIV, of cytochroomoxidase, is de terminale rustplaats voor elektronen die de keten binnenkomen. Degenen die het zo ver hebben gehaald, zijn zo ver mogelijk naar beneden in de hiërarchie van het reductiepotentieel gedaald. Hier, ze zijn verzonken in wachtende zuurstofmoleculen, die vervolgens worden uitgeput als watermoleculen. Elektronen met een hoog potentieel, verpakt als NADH, komen het complex binnen aan de omtrek en worden naar het centrum geleid. De afwezigheid van C5-complexen is misschien niet zo ongewoon, gezien het feit dat ze meestal worden gevonden als rijen "V'-vormige dimeren die het membraan verwringen in gebieden met een hoge kromming bij bochten in de cristea.
Met de basisstructuur in de hand, de onderzoekers konden enkele basisprincipes van de werking suggereren. Hun opname en plaatsing van CII verklaart effectief omgekeerd elektronentransport van succinaat naar NADH. De voorgestelde geometrie creëert ook een afgesloten Q-pool (een in vet oplosbare elektronendrager) die toegankelijk is voor zowel CI als CII. De auteurs waren ook in staat om de identiteit en locaties vast te stellen van verschillende lipidemoleculen die het complex binnen het membraan beveiligen, specifiek, verschillende cruciale moleculen van fosfatidylethanolamine, fosfatidylcholine, en cardiolipine. Ze waren ook in staat om voorkeurs- of meest efficiënte elektronenoverdrachtsroutes te identificeren, die op hun beurt beperken hoeveel elektronen tegelijkertijd tussen actieve dragers kunnen worden overgedragen.
Een van de onmiddellijke voordelen van dit nieuwe werk is dat veel van de voorheen onvolledig begrepen pathogene mutaties in respiratoire eiwitten nu logisch zijn. Voorafgaand aan het hebben van een megacomplexe structuur, onderzoekers hadden geen andere keuze dan zich te concentreren op hoe mutaties de structuur of functie van individuele complexen beïnvloeden. Zoals het blijkt, de meeste van de geregistreerde mutaties in kernsubeenheden Ci en CIII-doelwit bevinden zich in residuen die betrokken zijn bij eiwit-eiwitinteractieplaatsen tussen complexen. (Bijvoorbeeld, ziekte-geassocieerde mutaties in subeenheden NDUFV1, NDUFS1, ND1, ND5, en ND6 in CI en subeenheid MT-CYB in CIII). Dit toont de zinloosheid aan om alleen naar afzonderlijke eiwitten en subeenheden te kijken in afwezigheid van het grotere geheel.
Er moet worden vermeld dat eerdere pogingen om stoichiometrie van het ademhalingscomplex te definiëren enigszins verschillende resultaten hebben opgeleverd, afhankelijk van de organen en soorten die werden bestudeerd. Aardappel, koe, schaap, en gist, die niet altijd een CI-complex hebben om van te spreken, zijn allemaal bestudeerd. Het is niet verwonderlijk dat verschillende omstandigheden verschillende stoichiometrie en vorm kunnen vereisen. Verschillende megacomplexe structuren zouden verschillende voordelen met zich meebrengen voor het kanaliseren van substraat, katalytische verbetering, sekwestratie van reactieve tussenproducten, of structurele stabilisatie. Een studie die specifiek naar hart-mitochondriën keek, stelde de verhouding voor oxidatieve fosforylatiecomplexen I:II:III:IV:V in op 1:1,5:3:6:3. In dit geval, de auteurs noemden hun complex het 'respirasoom'.
Met het respiratoire megacomplex nu vermoedelijk gebarsten, de volgende grote stap voorwaarts is om enkele van de andere superstructuren van het mitochondriale dubbele membraansysteem in modellen te laten vallen om te voorspellen waarom cristea eruitziet zoals ze doen. De enorme TIM-TOM-importcomplexen omspannen beide membranen en zijn nauw verbonden met de mitoribosomen die mitochondriale eiwitten vertalen. De mitoribosomen, beurtelings, zijn gelokaliseerd in onderliggende membraan-geassocieerde nucleoïden die kopieën van het mtDNA bevatten. Naar analogie met de nucleolus van de kern, deze samengestelde nucleoïde-ribosoomstructuur wordt de 'mitochondriolus' genoemd. Andere cruciale importcomplexen bevinden zich in de mix van spelers die strijden om kritisch membraanvastgoed. De malaat-aspartaat-shuttle, bijvoorbeeld, is de belangrijkste shuttle in de hersenen en brengt de belangrijkste metabolieten tussen mitochondriën en cytosol in evenwicht. Ook de citraat-pyruvaat-shuttle voor vetzuursynthese en de glycerolfosfaat-shuttle (althans voor bruin vet en insectenvliegspier) moeten een thuis vinden waar ze goed kunnen opschieten met de directe buren.
De endemische organisatie van eiwitten in deze megastructuren suggereert dat mitochondriën meer op een hard kristal kunnen lijken dan op een vloeibaar protoplasma. Maar op de een of andere manier, ze lijken opmerkelijk soepel als het gaat om fusie en splijting. Wat gebeurt er met hun membraanstructuur bij dit soort veranderingen? Worden de complexen tijdelijk gedemonteerd en opgelost zoals de primaire cilium en centriol van reguliere cellen tijdens mitose? Een fascinerende nieuwe aanwijzing komt naar voren uit werk dat aantoont dat mitochondriën met elkaar in verbinding staan via 'nanotunnels' van hun eigen constructie. Deze nanotunnels zijn compleet anders (voor zover we weten) van het met cytoskelet doordrenkte merk van 'tunnelling nanobuisjes' die cellen zelf gebruiken om hele mitochondriën naar elkaar over te brengen.
Een recente recensie van Martin Picard en zijn collega's in Trends in celbiologie suggereert een manier waarop deze nanotunnels kunnen worden gevormd wanneer mitochondriën aan het cytoskelet zijn bevestigd. Als motoreiwitten zoals kinesine een stukje gefixeerde mitochondriën te pakken krijgen, het zou een dunne nanotunnel kunnen uittrekken als de kinesine motoren tegen een andere microtubule. Het stijve lichaam van de mitochondriën en de membraanstructuur zouden vermoedelijk intact blijven. Deze projectie kan dan een andere mitochondria tegenkomen waaraan het gehecht raakt.
Picard toonde eerder aan dat ongeveer de helft van de mitochondriën in de hartspier intermitochondriale knooppunten (IMJ's) en cristae heeft die in regelmatige patronen op één lijn liggen die zich uitstrekken over mitochondriale netwerken. Het is onwaarschijnlijk dat deze griezelige netwerkuitlijning voortkomt uit recente splijtingsgebeurtenissen omdat hartmitochondriën op hun plaats zijn gefixeerd en minimale splijting / fusie-dynamiek vertonen. Van de IMJ's is onlangs aangetoond dat ze de contractiliteit beheersen door snel ontkoppelde mitochondriën wanneer hun eigen membranen worden gedepolariseerd. Een ding dat van onmiddellijk belang zou zijn, hier, is om de stoichiometrie van de respiratoire subeenheid in mitochondriën van het menselijk hart opnieuw te onderzoeken om de hier gerapporteerde resultaten voor menselijke embryonale niercellen aan te vullen.
© 2017 Fys.org
 MBL-team fotografeert de bacteriële lifters op plastic afval in de oceaan
MBL-team fotografeert de bacteriële lifters op plastic afval in de oceaan Klimaatverandering verslechtert extreem weer in Australië:wetenschappers
Klimaatverandering verslechtert extreem weer in Australië:wetenschappers Welke dieren leven in aquatische habitats?
Welke dieren leven in aquatische habitats?  Soorten kikkers, geboren in Pennsylvania
Soorten kikkers, geboren in Pennsylvania Onderzoekers gebruiken genomische gegevens om refugia in kaart te brengen waar Noord-Amerikaanse bomen de ijstijd hebben overleefd
Onderzoekers gebruiken genomische gegevens om refugia in kaart te brengen waar Noord-Amerikaanse bomen de ijstijd hebben overleefd
Hoofdlijnen
- Amazoneboeren ontdekten het geheim van het domesticeren van wilde rijst 4, 000 jaar geleden
- Basiscelfuncties
- De betekenis van Penta E
- De definitie van abiotische en biotische factoren
- Nieuwe online database brengt het genoom in beeld met behulp van moleculaire structuur
- Bloed afnemen met de push-pull-methode levert nauwkeurige resultaten op met minder porren
- Onderzoek biedt inzichten voor de bestrijding van verwoestende amfibieënziekte
- De nadelen van Western Blotting
- Een klassieke darwinistische ecologische hypothese houdt stand - met een twist
- Vier klassen Macromoleculen die belangrijk zijn voor levende wezens

- Studie analyseert de eigenaardige schedelanatomie van brulapen
- Waarom creëren Britse wetenschappers een hybride mens-varken?

- Ontdekt? Nieuw maar uitgestorven menselijk familielid uit Melanesië

- Wetenschappers afluisteren onbekende spitssnuitdolfijnen af om te zien hoe diep ze duiken

 Waterdruppels worden hydrobots door magnetische kralen toe te voegen
Waterdruppels worden hydrobots door magnetische kralen toe te voegen Zeeanemonen krijgen plastic microvezels binnen
Zeeanemonen krijgen plastic microvezels binnen Afbeelding:CubeSat micro-gepulseerde plasma-thruster
Afbeelding:CubeSat micro-gepulseerde plasma-thruster Wetenschappers bestuderen hoe grootschalige milieuverstoringen oude samenlevingen beïnvloedden
Wetenschappers bestuderen hoe grootschalige milieuverstoringen oude samenlevingen beïnvloedden Wetenschappers identificeren overgangsmetaal voor zeer efficiënte kooldioxide-activering
Wetenschappers identificeren overgangsmetaal voor zeer efficiënte kooldioxide-activering Afname uitstoot lockdown heeft geen effect op klimaat
Afname uitstoot lockdown heeft geen effect op klimaat Hoe afbeeldingen op een grafische rekenmachine te tekenen
Hoe afbeeldingen op een grafische rekenmachine te tekenen  Hoe orkanen werken
Hoe orkanen werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Danish | Portuguese | Norway |

-
Wetenschap © https://nl.scienceaq.com

