
Wetenschap
Nanogeneeskunde dringt de hersenen binnen, roeit terugkerende hersenkanker bij muizen uit

Een elektronenmicroscoopbeeld van de nanodeeltjes. De schaalbalk is één micrometer, of 0,001 millimeter. Krediet:Jason Gregory, Lahann-lab, Universiteit van Michigan
Een nieuw synthetisch eiwit-nanodeeltje dat in staat is om langs de bijna ondoordringbare bloed-hersenbarrière te glippen, kan kankerdodende medicijnen rechtstreeks afleveren aan kwaadaardige hersentumoren, blijkt uit nieuw onderzoek van de Universiteit van Michigan.
De studie is de eerste die een intraveneuze medicatie aantoont die de bloed-hersenbarrière kan passeren.
De vondst, aangetoond bij muizen, nieuwe klinische therapieën mogelijk maken voor de behandeling van glioblastoom, de meest voorkomende en agressieve vorm van hersenkanker bij volwassenen, en een waarvan de incidentie in veel landen stijgt. De mediane overleving van vandaag voor patiënten met glioblastoom is ongeveer 18 maanden; de gemiddelde 5-jaarsoverleving is minder dan 5%.
In combinatie met straling, de intraveneus geïnjecteerde therapie van het UM-team leidde tot overleving op lange termijn bij zeven van de acht muizen. Toen die zeven muizen een herhaling van glioblastoom ervoeren, hun immuunreacties kwamen in werking om de hergroei van de kanker te voorkomen - zonder aanvullende therapeutische medicijnen of andere klinische behandelingen.
"Het is nog steeds een beetje een wonder voor ons, " zei Joerg Lahann, de Wolfgang Pauli Collegiate Professor of Chemical Engineering en een co-senior auteur op het papier, die verschijnt in Natuurcommunicatie . "Waar we enige niveaus van tumorgroei zouden verwachten, ze vormden zich gewoon niet toen we de muizen opnieuw uitdaagden. Ik werk al meer dan 10 jaar in dit veld en heb nog nooit zoiets gezien."
De bevindingen suggereren dat de combinatie van therapeutische medicijnen en toedieningsmethoden van nanodeeltjes door het UM-team niet alleen de primaire tumor heeft uitgeroeid, maar resulteerde in een immunologisch geheugen, of het vermogen om resterende kwaadaardige kankercellen sneller te herkennen en aan te vallen.

Het proces van het maken van deeltjes begint met een oplossing die het geneesmiddel tegen kanker bevat (in het paarse molecuul), tumor-homing molecuul (ring van regenboogstippen), het eiwit voor het passeren van de bloed-hersenbarrière (groene en rode linten), en de linkermoleculen (groene vijfhoeken) die helpen het geheel bij elkaar te houden. De oplossing loopt door een injectienaald en in een elektrisch veld dat het in een kegel comprimeert. Vanaf de punt van die kegel, kleine druppeltjes spuiten eruit. De vloeistof verdampt, en de deeltjes smelten samen. Eindelijk, een week uitharden op lichaamstemperatuur voltooit de koppeling, en de deeltjes zijn klaar om te gaan. Krediet:Jason Gregory, Lahann-lab, Universiteit van Michigan
"Dit is een enorme stap in de richting van klinische implementatie, " zei Maria G. Castro, de R. C. Schneider Collegiate Professor of Neurosurgery en een co-senior auteur op het papier. "Dit is de eerste studie die het vermogen aantoont om therapeutische geneesmiddelen systemisch af te leveren, of intraveneus, dat kan ook de bloed-hersenbarrière passeren om tumoren te bereiken."
Vijf jaar geleden, Castro wist hoe ze glioblastoom wilde aanpakken. Ze wilde een signaal stoppen dat kankercellen uitzenden, bekend als STAT3, om immuuncellen te misleiden om ze een veilige doorgang in de hersenen te geven. Als ze dat pad kon afsluiten met een remmer, de kankercellen zouden worden blootgesteld en het immuunsysteem zou ze kunnen elimineren. Maar ze had geen manier om door de bloed-hersenbarrière te komen.
Ze volgde een workshop aan het Biointerfaces Institute, die Lahann leidt, en de twee bespraken het probleem. Het team van Lahann begon te werken aan een nanodeeltje dat een STAT3-remmer langs de bloed-hersenbarrière zou kunnen brengen.
Een eiwit dat humaan serumalbumine wordt genoemd, die in het bloed aanwezig is, is een van de weinige moleculen die de bloed-hersenbarrière kan passeren, daarom gebruikte het team van Lahann het als de structurele bouwsteen voor hun nanodeeltjes. Ze gebruikten synthetische moleculen om deze eiwitten aan elkaar te koppelen en bevestigden vervolgens de STAT3-remmer en een peptide genaamd iRGD, die dient als een tumor-homing-apparaat.
In de loop van drie weken, een cohort muizen kreeg meerdere doses van het nieuwe nanomedicijn, de mediane overleving van muizen verlengen tot 41 dagen, vanaf 28 dagen voor degenen die niet worden behandeld. Na dat succes, het team voerde een tweede muisstudie uit met het medicijn naast de huidige zorgstandaard:gerichte radiotherapie. Zeven van de acht muizen bereikten een langetermijnoverleving en leken volledig tumorvrij, zonder tekenen van kwaadaardigheid, invasieve tumorcellen.
De onderzoekers zeggen dat hun synthetische eiwit-nanodeeltjes kunnen worden geadopteerd, na verdere ontwikkeling en preklinische testen, om andere medicijnen en therapieën met kleine moleculen af te leveren aan momenteel "niet-geneeskrachtige" op vaste stoffen gebaseerde tumoren.
De krant, "Systemische hersentumorafgifte van synthetische eiwitnanodeeltjes voor glioblastoomtherapie, " verschijnt in Natuurcommunicatie .
 Hoe maken we waterstof uit steenkool, en is het echt een schone brandstof?
Hoe maken we waterstof uit steenkool, en is het echt een schone brandstof? Kooldioxidemineralisatie in geologisch veel voorkomende gesteenten voor koolstofopslag
Kooldioxidemineralisatie in geologisch veel voorkomende gesteenten voor koolstofopslag Welke elementen reageren met zoutzuur?
Welke elementen reageren met zoutzuur?  Wat zijn de polymeren van lipiden?
Wat zijn de polymeren van lipiden?  Supramoleculaire complexvorming - antraceen macrocyclus en C60 fullereen
Supramoleculaire complexvorming - antraceen macrocyclus en C60 fullereen
 Lijst met onderzeese oceaanplanten
Lijst met onderzeese oceaanplanten  Arctische planten bieden mogelijk geen voorspeld koolstofvastleggingspotentieel
Arctische planten bieden mogelijk geen voorspeld koolstofvastleggingspotentieel Verschuivingen in diepe geologische structuur hebben mogelijk de grote tsunami in Japan in 2011 vergroot
Verschuivingen in diepe geologische structuur hebben mogelijk de grote tsunami in Japan in 2011 vergroot Oude overstromingen gevormd, achtergelaten rotsblokken in Wildcat Ridge
Oude overstromingen gevormd, achtergelaten rotsblokken in Wildcat Ridge De effecten van niet recycleren
De effecten van niet recycleren
Hoofdlijnen
- Hoe kan een babyrobotzeehond een medisch hulpmiddel zijn?
- Wat zijn Agar Slants?
- Kwam Eiwit, DNA of RNA als eerste?
- Belofte van nieuwe antibiotica ligt in het aanhaken van kleine giftige tetherballs aan bacteriën
- Horzels lokken:wetenschappers ontsluiten seksferomoon van berucht honingbij-roofdier
- Diversiteit van grote dieren speelt een belangrijke rol in koolstofcyclus
- Het voordeel van het hebben van veel replicatie-origines in een eukaryotisch chromosoom
- Wat is de relatie tussen stikstofbasen en de genetische code?
- Wat zijn de chemische namen van de vier macromoleculen?
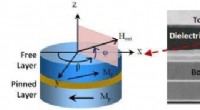
- Team ontwikkelt 's werelds krachtigste microgolfoscillatoren op nanoschaal
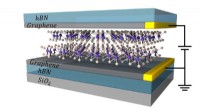
- Atomair dun magnetisch apparaat kan leiden tot nieuwe geheugentechnologieën
- Nanomaterialen:pijlers van de montage

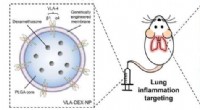
- Genetisch gemanipuleerde nanodeeltjes leveren dexamethason rechtstreeks aan ontstoken longen
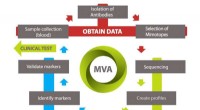
- Risicobeoordeling op nanoschaalniveau:de mimotoopvariatie-analyse nader bekeken
 Oude luizenachtige insecten gevonden om zich te voeden met dinosaurusveren
Oude luizenachtige insecten gevonden om zich te voeden met dinosaurusveren Google neemt het op tegen Apple Arcade met mobiele gameservice
Google neemt het op tegen Apple Arcade met mobiele gameservice Onderzoekers leveren open-source simulator voor cyberfysieke systemen
Onderzoekers leveren open-source simulator voor cyberfysieke systemen 99 procent van de groene zeeschildpadden van het Great Barrier Reef komen uit een vrouwtje
99 procent van de groene zeeschildpadden van het Great Barrier Reef komen uit een vrouwtje  Na een reset, Сuriositeit werkt normaal
Na een reset, Сuriositeit werkt normaal Aanzienlijke vooruitgang geboekt op het gebied van inverse fotogeleiding
Aanzienlijke vooruitgang geboekt op het gebied van inverse fotogeleiding Identificatie van biomolecuulfragmenten in ioniserende straling
Identificatie van biomolecuulfragmenten in ioniserende straling Effecten van koolstofvoetafdruk
Effecten van koolstofvoetafdruk
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

