
Wetenschap
Kooldioxidemineralisatie in geologisch veel voorkomende gesteenten voor koolstofopslag
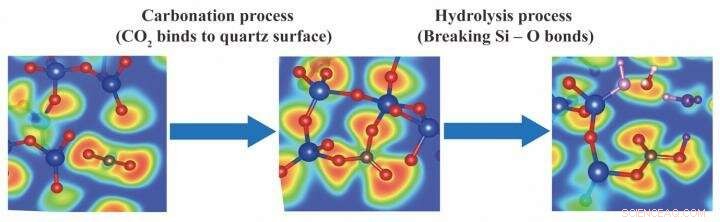
De rode kleur geeft aan dat de kans op het optreden van valentie-elektronen 100 procent is, de blauwe kleur betekent dat er geen elektronen in het gebied bestaan, en de groene kleur betekent vrij elektrongas dat de grens van covalente bindingen aangeeft. Rood, blauwe en bruine ballen vertegenwoordigen zuurstof, silicium- en koolstofatomen, respectievelijk. Credit:Internationaal Instituut voor koolstofneutraal energieonderzoek (I²CNER), Kyushu-universiteit
De mensheid moet verbeteren als het gaat om het verminderen van de CO2-uitstoot om de ergste effecten van klimaatverandering te voorkomen. Als de wereld wil voldoen aan de minimumdoelstelling van het IPCC om de wereldwijde temperatuurstijgingen onder de 1,5 °C te houden, alle mogelijke wegen voor CO 2 sanering moet worden onderzocht.
Geologische trapping kan hierbij een grote rol spelen. De ondergrondse rotsen en sedimenten van onze planeet bieden een enorme potentiële ruimte voor koolstofopslag op de lange termijn. Om dit te ondersteunen, een recente computationele studie van een door Japan geleide internationale groep aan de Kyushu University laat zien hoe ingesloten koolstofdioxide kan worden omgezet in onschadelijke mineralen.
De rotsen onder het aardoppervlak zijn zeer poreus, en trapping omvat het injecteren van CO 2 in de poriën na het verzamelen van de emissiebron. hoewel CO 2 wordt meestal als te stabiel beschouwd om chemisch met gesteente te reageren, het kan stevig aan het oppervlak binden door fysieke adsorptie. Uiteindelijk lost het op in water, koolzuur vormen, die kunnen reageren met waterige metalen om carbonaatmineralen te vormen.
"Mineralisatie is de meest stabiele methode van CO . op lange termijn 2 opslag, vergrendeling CO 2 in een volledig veilige vorm die niet opnieuw kan worden verzonden, " legt Jihui Jia van het International Institute for Carbon-Neutral Energy Research (I 2 CNER), Kyushu-universiteit, eerste auteur van de studie. "Eens werd gedacht dat dit duizenden jaren zou duren, maar dat beeld verandert snel. De chemische reacties worden niet volledig begrepen omdat ze zo moeilijk te reproduceren zijn in het laboratorium. Dit is waar modellenwerk om de hoek komt kijken."
Zoals gemeld in The Journal of Physical Chemistry C , aanvankelijk werden simulaties uitgevoerd om te voorspellen wat er gebeurt als koolstofdioxide botst met een gespleten kwartsoppervlak-kwarts (SiO 2 ) overvloedig aanwezig in de aardkorst. Toen de simulatietrajecten werden afgespeeld, de CO 2 moleculen werden gezien buigen van hun lineaire O=C=O vorm om trigonale CO . te vormen 3 eenheden gebonden met het kwarts.
In een tweede simulatieronde H 2 O-moleculen werden toegevoegd om het "formatiewater" na te bootsen dat vaak aanwezig is onder olie- en gasboorlocaties. Intrigerend, de H 2 O-moleculen vielen spontaan de reactieve CO . aan 3 structuren, het verbreken van de Si-O-bindingen om carbonaationen te produceren. Net als koolzuur, carbonaationen kunnen reageren met opgeloste metaalkationen (zoals Mg 2 + , Ca 2 + , en Fe 2 + ) om koolstof permanent in minerale vorm te binden.
Samen, de simulaties laten zien dat beide stappen van CO 2 mineralisatie - carbonatatie (binding aan gesteente) en hydrolyse (reageren met water) - zijn gunstig. Bovendien, vrije carbonaationen kunnen worden gemaakt door hydrolyse, niet alleen door dissociatie van koolzuur zoals ooit werd aangenomen. Deze inzichten waren gebaseerd op een geavanceerde vorm van moleculaire dynamica die niet alleen de fysieke botsingen tussen atomen modelleert, maar elektronenoverdracht, de essentie van de chemie.
"Onze resultaten suggereren enkele manieren om geologische vangst te verbeteren, ", zegt hoofdauteur Takeshi Tsuji van de studie. "Voor kwarts om CO . op te vangen 2 , het moet een gekloofd oppervlak zijn, dus de silicium- en zuurstofatomen hebben reactieve 'bungelende' bindingen. In het echte leven, echter, het oppervlak kan worden beschermd door waterstofbruggen en kationen, die mineralisatie zou voorkomen. We hebben een manier nodig om die kationen te verwijderen of het oppervlak te dehydrogeneren."
Er komen steeds meer aanwijzingen dat CO . wordt afgevangen 2 kan veel sneller mineraliseren dan eerder werd gedacht. Hoewel dit spannend is, de Kyushu-paper onderstreept hoe complex en delicaat de chemie kan zijn. Voor nu, de groep beveelt verdere studies aan over andere overvloedige rotsen, zoals basalt, om de rol in kaart te brengen die geochemische trapping kan spelen in de grootste technische uitdaging waarmee de beschaving wordt geconfronteerd.
 Risico's van natriumcarbonaat
Risico's van natriumcarbonaat Onderzoekers krijgen inzicht in hoe oplosmiddelmoleculen door licht gestuurde reacties beïnvloeden
Onderzoekers krijgen inzicht in hoe oplosmiddelmoleculen door licht gestuurde reacties beïnvloeden Nieuwe techniek voor in-cell afstandsbepaling
Nieuwe techniek voor in-cell afstandsbepaling Onderzoeksteam ontdekt verloren afbeeldingen uit de 19e eeuw
Onderzoeksteam ontdekt verloren afbeeldingen uit de 19e eeuw Bevindingen bevestigen het vermogen van beeldvormende technieken om gezond weefsel te onderscheiden na neoadjuvante chemotherapie
Bevindingen bevestigen het vermogen van beeldvormende technieken om gezond weefsel te onderscheiden na neoadjuvante chemotherapie
 Hoe stranden en kustlijnen te redden van rampen door klimaatverandering
Hoe stranden en kustlijnen te redden van rampen door klimaatverandering NASA volgt post-tropische cycloon Barry naar Indiana
NASA volgt post-tropische cycloon Barry naar Indiana Feiten over baby Giraffen
Feiten over baby Giraffen Oude mijnen werpen een lange schaduw over hun omgeving
Oude mijnen werpen een lange schaduw over hun omgeving Wereld moet tegen 2020 actie ondernemen om op hol geslagen klimaatverandering te voorkomen:VN-chef
Wereld moet tegen 2020 actie ondernemen om op hol geslagen klimaatverandering te voorkomen:VN-chef
Hoofdlijnen
- Zijn gelukkige mensen aardiger?
- Studie onthult hoe de adelborst zijn paar uur lang in stand houdt
- Gemengde organisatie van darmbacteriën wordt onthuld door microbioombeeldvormingstechnologie
- Wat is de structuur van stamcellen?
- Hoe schimmels hebben bijgedragen aan het ontstaan van het leven zoals wij dat kennen
- Ontdekking van gewasgenen raakt de wortel van voedselzekerheid
- Rollen van celorganellen in mitose
- Soorten berekenen Evenness
- Het Bohr-model:snel vervangen maar nooit vergeten
- Giftige chemicaliën uit water verwijderen:nieuwe milieuvriendelijke methode

- Op Mars of de aarde, biohybride kan koolstofdioxide omzetten in nieuwe producten

- Licht gebruiken om de reikwijdte van carbonyleringsreacties uit te breiden

- Nieuw flexibel materiaal verandert zijn poreuze aard bij blootstelling aan licht
- Oorbeschermers meten het alcoholgehalte in het bloed via de huid
 Intensivering van extreme regenval verschilt van regio tot regio, studie toont
Intensivering van extreme regenval verschilt van regio tot regio, studie toont Meer dan 100 brandwetenschappers dringen er bij het westen van de VS op aan:sla het vuurwerk over op deze recorddroge Fourth of July
Meer dan 100 brandwetenschappers dringen er bij het westen van de VS op aan:sla het vuurwerk over op deze recorddroge Fourth of July Team wil nieuwe NASA-telescoop gebruiken om licht te vangen van de eerste sterren die in het universum worden geboren
Team wil nieuwe NASA-telescoop gebruiken om licht te vangen van de eerste sterren die in het universum worden geboren Dode planeten kunnen tot een miljard jaar uitzenden
Dode planeten kunnen tot een miljard jaar uitzenden Hoe maak je een Bug Zapper
Hoe maak je een Bug Zapper  De natuur is de sleutel tot het koesteren van groene waterzuiveringsinstallaties
De natuur is de sleutel tot het koesteren van groene waterzuiveringsinstallaties Bonuswetenschap ontdekken met NASA's Magnetospheric Multiscale Spacecraft
Bonuswetenschap ontdekken met NASA's Magnetospheric Multiscale Spacecraft Wat is een niet-vluchtige opgeloste stof?
Wat is een niet-vluchtige opgeloste stof?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

