Wetenschap
Genetisch gemanipuleerde nanodeeltjes leveren dexamethason rechtstreeks aan ontstoken longen
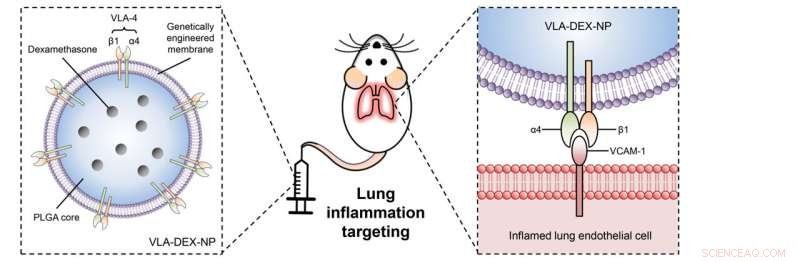
Schema van genetisch gemanipuleerde celmembraan-gecoate nanodeeltjes voor medicijnafgifte aan ontstoken longen. Krediet:Zhang Lab
Nano-ingenieurs aan de Universiteit van Californië in San Diego hebben nanodeeltjes ontwikkeld die op immuuncellen lijken en die zich richten op ontstekingen in de longen en medicijnen afleveren waar ze nodig zijn. Als proof-of-concept, de onderzoekers vulden de nanodeeltjes met het medicijn dexamethason en dienden ze toe aan muizen met ontstoken longweefsel. Ontsteking werd volledig behandeld bij muizen gezien de nanodeeltjes, bij een geneesmiddelconcentratie waar standaard toedieningsmethoden geen enkele werkzaamheid hadden.
De onderzoekers rapporteerden hun bevindingen in wetenschappelijke vooruitgang op 16 juni.
Het bijzondere aan deze nanodeeltjes is dat ze zijn gecoat in een celmembraan dat genetisch is gemanipuleerd om te zoeken naar en te binden aan ontstoken longcellen. Ze zijn de nieuwste in de lijn van zogenaamde celmembraan-gecoate nanodeeltjes die zijn ontwikkeld door het laboratorium van UC San Diego nanoengineering professor Liangfang Zhang. Zijn laboratorium heeft eerder met celmembraan gecoate nanodeeltjes gebruikt om toxines geproduceerd door MRSA te absorberen; sepsis behandelen; en train het immuunsysteem om kanker te bestrijden. Maar terwijl deze vorige celmembranen van nature afkomstig waren van lichaamscellen, de celmembranen die werden gebruikt om dit met dexamethason gevulde nanodeeltje te coaten, waren dat niet.
"In deze krant, we gebruikten een genetische manipulatiebenadering om de oppervlakte-eiwitten op de cellen te bewerken voordat we de membranen verzamelden. Dit heeft onze technologie aanzienlijk verbeterd door ons in staat te stellen bepaalde functionele eiwitten op de membranen nauwkeurig tot overexpressie te brengen of sommige ongewenste eiwitten uit te schakelen. " zei Zhang, wie is een senior auteur van het papier.
Joon Ho Park, een afgestudeerde student in het laboratorium van Zhang en eerste auteur van het artikel, zeiden de onderzoekers dat wanneer endotheelcellen ontstoken raken, ze brengen een eiwit genaamd VCAM1 tot overexpressie, waarvan het doel is om immuuncellen naar de plaats van ontsteking te lokken. In antwoord, de immuuncellen brengen een eiwit tot expressie dat VLA4 wordt genoemd, die zoekt naar en bindt aan VCAM1.
"We hebben celmembranen ontworpen om de volledige versie van VLA4 altijd tot uitdrukking te brengen, " zei Park. "Deze membranen brengen VLA4 constant tot overexpressie om VCAM1 en de plaats van ontsteking te zoeken. Deze gemanipuleerde celmembranen zorgen ervoor dat het nanodeeltje de ontstoken plaatsen kan vinden, en laat dan het medicijn vrij dat zich in het nanodeeltje bevindt om het specifieke ontstekingsgebied te behandelen."
Hoewel het nanodeeltje de werkzaamheid van het medicijn niet direct zal verbeteren - in dit geval dexamethason - kan het concentreren op de plaats van belang betekenen dat een lagere dosering nodig is. Deze studie toonde aan dat dexamethason zich in hogere concentraties ophoopte op de plaats van belang, en sneller, dan standaard benaderingen voor medicijnafgifte.
"We leveren exact hetzelfde medicijn dat in de kliniek wordt gebruikt, maar het verschil is dat we de drugs concentreren op het punt van belang, " zei Park. "Door deze nanodeeltjes zich op de ontstekingsplaats te richten, het betekent dat een groter deel van het medicijn terecht komt waar het nodig is, en niet door het lichaam worden opgeruimd voordat het zich kan ophopen en effectief kan zijn."
De onderzoekers merken op dat deze genetisch gemanipuleerde celmembraanbenadering een platformtechnologie is die in theorie kan worden gebruikt om niet alleen ontstekingen in andere delen van het lichaam aan te pakken - VCAM1 is een universeel signaal van ontsteking - maar ook veel bredere gebruiksscenario's.
"Dit is een veelzijdig platform, niet alleen voor longontsteking, maar voor elk type ontsteking dat VCAM1 opreguleert, " zei Park. "Deze technologie kan worden veralgemeend; dit gemanipuleerde celmembraan-gecoate nanodeeltje hoeft VLA4 niet tot overexpressie te brengen, het kan worden uitgewisseld met een ander eiwit dat zich op andere delen van het lichaam kan richten of andere doelen kan bereiken."
Om de celmembranen te manipuleren om het VLA4-eiwit tot overexpressie te brengen, Park en het team beginnen met het verpakken van VLA4-genen in een virale vector. Vervolgens brengen ze deze opnieuw geprogrammeerde virale vector in in in het laboratorium gekweekte gastheercellen die zijn afgeleid van muizen. De cellen nemen de genen op die de virale vector met zich meedraagt in hun eigen genoom en als resultaat produceren membranen die voortdurend VLA4 tot overexpressie brengen.
De volgende stap van de onderzoekers is om het proces te bestuderen met behulp van menselijke celmembranen, in plaats van celmembranen van muizen, die zijn ontworpen om de menselijke versie van VLA4 uit te drukken. Er zijn nog veel stappen nodig voordat de technologie kan worden getest in klinische proeven bij mensen, maar de onderzoekers zeggen dat deze vroege resultaten van de platformtechnologie bemoedigend zijn.
"Door gebruik te maken van de gevestigde technieken voor het bewerken van genen, deze studie brengt de met celmembraan gecoate nanodeeltjes naar een nieuw niveau en opent nieuwe mogelijkheden voor gerichte medicijnafgifte en andere medische toepassingen", gesloten door Zhang.
 Nieuwe aanpak maakt het gemakkelijker om nieuwe medicijnen te vinden
Nieuwe aanpak maakt het gemakkelijker om nieuwe medicijnen te vinden Waarom veranderen hydraten van kleur wanneer ze worden verwarmd?
Waarom veranderen hydraten van kleur wanneer ze worden verwarmd?  De pH verhogen met zuiveringszout in water
De pH verhogen met zuiveringszout in water  Doorstroomelektroden maken waterstof 50 keer sneller
Doorstroomelektroden maken waterstof 50 keer sneller Elektronenmicroscopie biedt nieuwe kijk op klein virus met therapeutisch potentieel
Elektronenmicroscopie biedt nieuwe kijk op klein virus met therapeutisch potentieel
Hoofdlijnen
- Olifantenstroperij in Afrika neemt af, maar ivoorvangsten nemen toe:studie
- Wat is de subeenheid van DNA genaamd?
- Garnalenvisserij in New England voor minstens een jaar gesloten
- Hoe bijen hun weg naar huis vinden
- Zeldzame vliegende vossen neergeschoten bij gruwelijke aanval in Australië
- Hinderlaag in een petrischaal
- Duiven kunnen zowel ruimte als tijd onderscheiden
- Beschrijving van gen-splitsing als een DNA-techniek
- Staan we op een kantelpunt met onkruidbestrijding?
 Kuststeden stellen tot 75% van de zeebodem bloot aan schadelijke lichtvervuiling
Kuststeden stellen tot 75% van de zeebodem bloot aan schadelijke lichtvervuiling Hoe kunstbloed werkt
Hoe kunstbloed werkt  Student lost een 100 jaar oud natuurkundig raadsel op
Student lost een 100 jaar oud natuurkundig raadsel op Enzymen geschikt maken voor industriële toepassingen
Enzymen geschikt maken voor industriële toepassingen Wat als je echt 50 eieren hebt gegeten zoals in Cool Hand Luke?
Wat als je echt 50 eieren hebt gegeten zoals in Cool Hand Luke?  Winst Nokia Q4 stijgt doordat operators overstappen op 5G-netwerken
Winst Nokia Q4 stijgt doordat operators overstappen op 5G-netwerken Hoe gebruik je een Bushnell Reflector Telescope
Hoe gebruik je een Bushnell Reflector Telescope Onderzoek:Tesla Autopilot misleidend, meer overschat dan vergelijkbare technologie
Onderzoek:Tesla Autopilot misleidend, meer overschat dan vergelijkbare technologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com