
Wetenschap
Gerichte nanodeeltjes die beeldvorming combineren met twee verschillende therapieën kunnen kanker aanvallen, andere condities
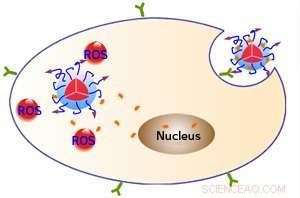
Oppervlaktepeptiden (paarse pijlen) zorgen ervoor dat fluorescerende nanodeeltjes binden aan een eiwit (groen) op de doelcellen en in de cellen worden opgenomen. Blootstelling aan licht zorgt ervoor dat de nanodeeltjes reactieve zuurstofsoorten (ROS) genereren, doodt de cellen, en maakt ook het medicijn doxorubicine (oranje) vrij, die vervolgens de celkern kunnen binnendringen. Krediet:WILEY-VCH Verlag GmbH &Co. KGaA, Weinheim
Nanosystemen die 'theranostisch' zijn - ze combineren zowel therapeutische als diagnostische functies - bieden een opwindende nieuwe mogelijkheid voor het afleveren van medicijnen aan specifieke cellen en het identificeren van ziekteplaatsen. Bin Liu van het A*STAR Institute of Materials Research and Engineering, en collega's van de Nationale Universiteit van Singapore, nanodeeltjes hebben gecreëerd met twee verschillende antikankerfuncties en een beeldvormende functie, allemaal op verzoek gestimuleerd door een enkele lichtbron. De nanodeeltjes bevatten ook de celgerichte eigenschap die essentieel is voor behandeling en beeldvorming op de juiste locaties.
Het systeem is opgebouwd rond een polymeer op basis van polyethyleenglycol dat een kleine peptidecomponent bevat waardoor het zich bij voorkeur aan specifieke celtypes kan binden. Het polymeer zelf dient als een fotosensibilisator die door licht kan worden gestimuleerd om reactieve zuurstofsoorten (ROS) vrij te maken. Het draagt ook het chemotherapiedrug doxorubicine in de vorm van een prodrug.
De natuurlijke fluorescentie van het polymeer helpt bij de diagnose en monitoring van de therapie, omdat het laat zien waar nanodeeltjes zich hebben opgehoopt. De ROS gegenereerd door lichtstimulatie hebben een directe 'fotodynamische' therapeutische activiteit, die de beoogde cellen vernietigt. De ROS verbreken bovendien de link tussen het polymeer en de doxorubicine. Dus, kankercellen kunnen worden onderworpen aan een tweeledige aanval van de ROS-therapie en het chemotherapie-medicijn dat erin vrijkomt (zie afbeelding).
"Dit is het eerste nanoplatform dat on-demand en beeldgestuurde fotodynamische therapie en chemotherapie kan bieden met geactiveerde medicijnafgifte via één lichtschakelaar, " legt Liu uit, benadrukt het belang van het systeem.
De onderzoekers demonstreerden de kracht van hun platform door het toe te passen op een mengsel van gekweekte kankercellen, waarvan sommige een oppervlakte-eiwit tot overexpressie brachten dat zou kunnen binden aan het targeting-peptide op de nanodeeltjes. Fluorescentiebeeldvorming gaf aan dat de nanodeeltjes werden opgenomen door de doelcellen en dat ROS en doxorubicine in deze cellen werden afgegeven - allemaal op significant hogere niveaus dan in cellen die als controles werden gebruikt. Het doxorubicine dat vrijkwam in het celcytoplasma ging gemakkelijk de kern binnen - de plaats van activiteit. Cruciaal, de gecombineerde therapie had een groter cytotoxisch effect dan enige therapie alleen.
"Het witte licht dat in dit werk wordt gebruikt, dringt niet voldoende door in het weefsel voor in vivo toepassingen, "Lou legt uit, "maar we proberen nu bijna-infrarood laserlicht te gebruiken om de weefselpenetratie te verbeteren en op weg te gaan naar on-demand kankertherapie." Ze stelt ook voor dat met een paar aanpassingen, het systeem kan geschikt zijn voor de diagnose en behandeling van andere pathologische processen, waaronder ontsteking en HIV-infectie.
 DNA-suikers gekenmerkt in ongekende resolutie, atoom voor atoom
DNA-suikers gekenmerkt in ongekende resolutie, atoom voor atoom De moleculaire afbuiging van lichtstraling door middel van diamantaan
De moleculaire afbuiging van lichtstraling door middel van diamantaan De rol van coöperativiteit in hydrofobe interacties onthuld in realtime monitoring
De rol van coöperativiteit in hydrofobe interacties onthuld in realtime monitoring Studie vindt bewijs voor bestaan van ongrijpbare metabolon
Studie vindt bewijs voor bestaan van ongrijpbare metabolon Een multidimensionaal beeld van SARS-CoV-2
Een multidimensionaal beeld van SARS-CoV-2
 ASA's Aqua-satelliet vindt een extra-tropische cycloon Cimaron
ASA's Aqua-satelliet vindt een extra-tropische cycloon Cimaron Waarom verschuift de Japanse Olympische marathon van steden om de hitte te vermijden? Een sportfysioloog legt uit:
Waarom verschuift de Japanse Olympische marathon van steden om de hitte te vermijden? Een sportfysioloog legt uit: De complexe relatie tussen ontbossing en voedingsdiversiteit in de Amazone
De complexe relatie tussen ontbossing en voedingsdiversiteit in de Amazone Klimaatverandering kan de vitale tropische regenband verkleinen
Klimaatverandering kan de vitale tropische regenband verkleinen 2018 was een van de warmste jaren ooit en dit jaar zou nog heter kunnen worden
2018 was een van de warmste jaren ooit en dit jaar zou nog heter kunnen worden
Hoofdlijnen
- Bacteriën als pacemaker voor de darm
- Somatische en genetische schade veroorzaakt door straling
- Hoe zijn fotosynthese en cellulaire ademhaling gerelateerd
- We kregen te maken met misbruik omdat we mensen vroegen om wespen te doden voor de wetenschap - hier is waarom het de moeite waard was
- Namen van DNA-strengen
- Wat gebeurt er met een diercel wanneer deze zich in een hypotone oplossing bevindt?
- Warmteminnende Australische mieren geloven in diversiteit, hint 74 soorten nieuw voor de wetenschap
- Wat zijn enkele kenmerken van proteïne?
- Revolutionaire beeldvormingstechniek maakt gebruik van CRISPR om DNA-mutaties in kaart te brengen
- Nano-software biedt verbeterde bescherming voor zowel werknemers als de industrie

- Hoogtepunt:superparamagnetische gouden nanoshells met afstembare optische eigenschappen
- Natuurkundigen kweken micromachines uit koolstof

- Rekbare lithium-ionbatterij op basis van nieuwe microhoningraatstructuur

- Lanthanide-nanokristallen verhelderen moleculaire triplet-excitons
 Lang verloren gewaand Vlaams meesterwerk ontdekt in Brusselse wijkzaal
Lang verloren gewaand Vlaams meesterwerk ontdekt in Brusselse wijkzaal Is zoutzuur hetzelfde als zoutzuur?
Is zoutzuur hetzelfde als zoutzuur?  VS heeft de natste 12 maanden ooit - opnieuw
VS heeft de natste 12 maanden ooit - opnieuw Kunstmatige zoetstoffen in grondwater duiden op verontreiniging door septische systemen
Kunstmatige zoetstoffen in grondwater duiden op verontreiniging door septische systemen Mannelijke promovendi verdienen meer, meer kans op een vaste baan dan vrouwelijke collega's
Mannelijke promovendi verdienen meer, meer kans op een vaste baan dan vrouwelijke collega's Team ontwikkelt nieuw mechanisme om materialen te versterken
Team ontwikkelt nieuw mechanisme om materialen te versterken Wat is de levensduur van een honingbij?
Wat is de levensduur van een honingbij?  Hoe de Japanse Olympische Spelen op basis van hernieuwbare energie het begin kunnen zijn van een wereldwijde race voor schone energie
Hoe de Japanse Olympische Spelen op basis van hernieuwbare energie het begin kunnen zijn van een wereldwijde race voor schone energie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

