
Wetenschap
Onverwachte oxidatieactiviteit van goud:de rol van water in nanokatalyse van goud decoderen
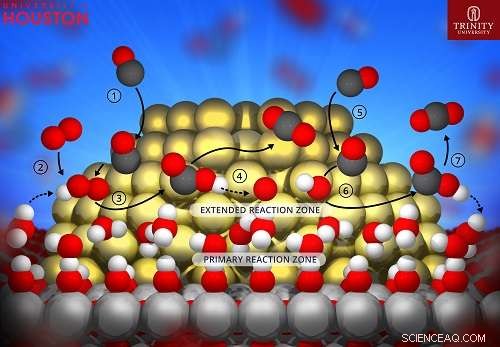
Schematische weergave van de laagste energieroute voor CO-oxidatie op goud-titania-katalysatoren. De waterlaag op de titania-drager verlengt de reactiezone op de gouden nanocluster en levert protonen die helpen bij de zuurstofdissociatiestap. Krediet:Hieu Doan, Universiteit van Houston
Onderzoekers van de Universiteit van Houston en Trinity University hebben voor het eerst direct bewijs geleverd van een watergemedieerd reactiemechanisme voor de katalytische oxidatie van koolmonoxide.
Het werk gebruikte gouden nanodeeltjes en titaniumdioxide als katalysator om het proces te versnellen en stelde vast dat water dient als co-katalysator voor de reactie die koolmonoxide omzet in kooldioxide. Terwijl onderzoekers jarenlang hebben gewerkt met koolmonoxide-oxidatie met behulp van goudkatalysatoren en zich hebben gerealiseerd dat water de reactie kan veranderen, niemand heeft eerder volledig kunnen verklaren waarom het werkte.
Het werk wordt beschreven in de editie van 5 september van het tijdschrift Wetenschap .
"We kunnen met een hoge mate van zekerheid zeggen dat we nu de rol van elk van de componenten begrijpen en wat ze doen tijdens deze katalytische reactie, " zei Lars Grabow, assistent-professor chemische en biomoleculaire engineering aan de Universiteit van Houston. Hij en Hieu Doan, een doctoraat student aan het UH Cullen College of Engineering, ontwikkelde computationele simulaties ter ondersteuning van experimenten van de chemici van de Trinity University, Bert Chandler, Christopher Pursell en Johnny Saavedra.
Chandler, hoogleraar scheikunde aan Trinity, zei dat het werk een echte samenwerking was.
"Het kostte ons allemaal om het te laten gebeuren, " zei hij. "Wat we deden is de kloof tussen oppervlaktewetenschap en computationele mensen overbruggen. We wisten dat water de reactie hielp, maar begrepen de rol ervan niet helemaal. Nu weten we dat water een co-katalysator is voor deze reactie."
Bij gebruik in sieraden, goud wordt gewaardeerd om zijn niet-reactieve eigenschappen - het roest of dof niet wanneer het wordt blootgesteld aan lucht of water. En onderzoekers weten al lang dat ondanks zijn reputatie als inert metaal, gouden nanodeeltjes kunnen werken als een katalysator om de chemische reactie te versnellen.
Maar niemand wist precies waarom het werkte. Water bleek de sleutel te zijn, zelfs als het niet expliciet aan het proces wordt toegevoegd, zei Grabow.
Sporen van water uit de lucht dreven de reacties op het oppervlak van de goudkatalysatoren, hij zei.
Tijdens de experimenten en computationele studie, keken de onderzoekers hoe water, oppervlaktehydroxylen en het grensvlak van metaal en drager interageerden tijdens koolmonoxide-oxidatie over een goud-titania-katalysator.
"In alle gevallen, een in wezen barrièrevrije protonenoverdracht verlaagde de totale energie van het systeem, genereren van H2O2 of OOH. Toen OOH eenmaal was gevormd, het migreerde langs het Au-deeltje, atomen dichtbij laten, maar niet strikt op, de metaal-ondersteuningsinterface om deel te nemen aan de reactie, schreven ze om hun bevindingen te beschrijven, verwijzend naar de vorming van waterstofperoxide of hydroperoxyl en de migratie van hydroperoxyl langs de gouddeeltjes.
Eigenlijk, ze ontdekten dat protonen van een dunne laag water die zich over het oppervlak van de katalysator uitstrekt, zich losmaken van de watermoleculen en zich hechten aan zuurstofmoleculen, kort bewegend op het oppervlak van de katalysator om de reactie te stimuleren alvorens terug te keren naar de waterlaag.
Eerdere modellen waren meestal gericht op individuele componenten van de reactie, Grabow zei, waardoor dit project het eerste is dat alle facetten samenbrengt in één enkel model dat de experimentele waarnemingen van de Trinity-chemici volledig ondersteunt. Chandler zei dat het werk een manier zou kunnen bieden om schone waterstof te produceren uit aardolie en aardgas.
 Wat is een neerslagreactie?
Wat is een neerslagreactie?  Onderzoekers ontwikkelen dubbellaagse verf die warmte reflecteert
Onderzoekers ontwikkelen dubbellaagse verf die warmte reflecteert Doorbraak voor het volgen van RNA met fluorescentie
Doorbraak voor het volgen van RNA met fluorescentie NIST pH-standaardreferentiematerialen ondersteunen een van de meest gemeten eigenschappen van de productie
NIST pH-standaardreferentiematerialen ondersteunen een van de meest gemeten eigenschappen van de productie Zeer stabiele waterelektrolysekatalysator voor de productie van waterstof en zuurstof
Zeer stabiele waterelektrolysekatalysator voor de productie van waterstof en zuurstof
 De luchtkwaliteit is sinds 2016 verslechterd, geassocieerd met meer vroegtijdige sterfgevallen in de VS
De luchtkwaliteit is sinds 2016 verslechterd, geassocieerd met meer vroegtijdige sterfgevallen in de VS Pesticiden en industriële verontreinigende stoffen gevonden in sneeuw bovenop Arctische gletsjers
Pesticiden en industriële verontreinigende stoffen gevonden in sneeuw bovenop Arctische gletsjers Studie gebruikt computer vision-algoritme om Google Street View-afbeeldingen te onderzoeken op tekenen van stedelijke verandering
Studie gebruikt computer vision-algoritme om Google Street View-afbeeldingen te onderzoeken op tekenen van stedelijke verandering Informatie van burgers kan de modellering van overstromingen verbeteren
Informatie van burgers kan de modellering van overstromingen verbeteren Sneeuwvalpatronen kunnen aanwijzingen geven voor de Groenlandse ijskap
Sneeuwvalpatronen kunnen aanwijzingen geven voor de Groenlandse ijskap
Hoofdlijnen
- Wat is één reden waarom de classificatie van protisten in één koninkrijk moeilijk is?
- Deze pijnbomen leunen bijna altijd naar de evenaar
- Hoe MRNA van een cel te isoleren
- Projectideeën voor biotechnologie
- Wat is het doel van de fibreuze capsule?
- Telofase: wat gebeurt er in deze fase van mitose en meiose?
- Invasieve kikkers geven invasieve vogels een boost op Hawaï
- S-fase: wat gebeurt er tijdens deze subfase van de celcyclus?
- Hoe de dalingssnelheid te berekenen
- Tape van koolstofnanobuisjes blijft plakkerig bij extreme temperaturen

- Onderzoekers creëren eenstaps grafeenpatroonmethode
- Zebravisembryo's helpen te bewijzen wat er met nanodeeltjes in het bloed gebeurt
- Synthetische synapsen gaan meer op een echt brein lijken

- Een nanotransistor gemaakt van grafeen nanoribbons

 Het onderwijzen van kleuters nummers, gevoel voor hoeveelheid & tellen
Het onderwijzen van kleuters nummers, gevoel voor hoeveelheid & tellen  Onderwater robotglijders bieden een belangrijk hulpmiddel om oceaangeluidsniveaus te meten
Onderwater robotglijders bieden een belangrijk hulpmiddel om oceaangeluidsniveaus te meten Bronnen van fouten in gelelektroforese
Bronnen van fouten in gelelektroforese  Skiërs gewond door rondvliegende stenen op Japanse vulkaan
Skiërs gewond door rondvliegende stenen op Japanse vulkaan New Horizons stuurt de laatste stukjes van de flyby-gegevens van 2015 terug naar de aarde
New Horizons stuurt de laatste stukjes van de flyby-gegevens van 2015 terug naar de aarde Bodemwetenschappers gebruiken mijnafval om door mensen veroorzaakte woestenij te herstellen
Bodemwetenschappers gebruiken mijnafval om door mensen veroorzaakte woestenij te herstellen 737 MAX testvlucht nog niet gepland:FAA
737 MAX testvlucht nog niet gepland:FAA Wetenschappers ontwikkelen topologische defectdetectiemethode
Wetenschappers ontwikkelen topologische defectdetectiemethode
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Italian | Norway |

-
Wetenschap © https://nl.scienceaq.com

