
Wetenschap
Het corrigeren van een truc van het licht brengt moleculen in beeld
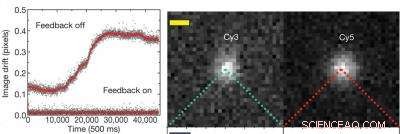
De grafiek links laat zien dat met het actieve feedbacksysteem uitgeschakeld er een resolutieafwijking is van ongeveer 0,3 pixels of 19 nanometer, maar met het feedbacksysteem wordt de resolutie op beter dan 0,01 pixels gehouden, of ongeveer 0,64 nanometer. De afbeelding rechts toont individuele cyanine (Cy) fluorescerende kleurstofmoleculen -- Cy3 en Cy5 -- die worden gebruikt om 20 basenparen dubbelstrengs DNA te labelen. Krediet:met dank aan de onderzoeksgroep van Steven Chu
Conventionele wijsheid stelt dat optische microscopie niet kan worden gebruikt om iets zo klein als een individueel molecuul te "zien". Maar zoals het gewoon is, slimme wetenschap heeft de conventionele wijsheid opnieuw omvergeworpen. minister van Energie, Nobelprijswinnaar en voormalig directeur van het Lawrence Berkeley National Laboratory (Berkeley Lab) Steven Chu leidde de ontwikkeling van een techniek die het gebruik van optische microscopie mogelijk maakt om objecten of de afstand ertussen in beeld te brengen met resoluties zo klein als 0,5 nanometer - de helft van een miljardste van een meter, of een orde van grootte kleiner dan de vorige beste.
"Het vermogen om sub-nanometerresolutie te krijgen in biologisch relevante waterige omgevingen heeft het potentieel om de biologie te revolutioneren, in het bijzonder structurele biologie, ", zegt secretaris Chu. "Een van de motivaties voor dit werk, bijvoorbeeld, was om afstanden te meten tussen eiwitten die multidomein vormen, zeer complexe structuren, zoals de eiwitassemblage die het menselijke RNA-polymerase II-systeem vormt, die DNA-transcriptie initieert."
Secretaris Chu is de co-auteur van een artikel dat nu in het tijdschrift verschijnt Natuur die dit onderzoek beschrijft. Het artikel is getiteld "Subnanometer single-molecule localization, registratie en afstandsmetingen." De andere auteurs zijn Alexandros Pertsinidis, een postdoctoraal onderzoeker en lid van Chu's onderzoeksgroep aan de University of California (UC) Berkeley, die nu assistent-professor is aan het Sloan-Kettering Institute, en Yunxiang Zhang, een lid van Chu's onderzoeksgroep aan de Stanford University.
Volgens een natuurkundige wet die bekend staat als de "diffractielimiet, " het kleinste beeld dat een optisch systeem kan oplossen, is ongeveer de helft van de golflengte van het licht dat wordt gebruikt om dat beeld te produceren. Voor conventionele optica, dit komt overeen met ongeveer 200 nanometer. Ter vergelijking, een DNA-molecuul is ongeveer 2,5 nanometer breed.
Hoewel niet-optische beeldvormingssystemen, zoals elektronenmicroscopen, kan objecten tot ver in de subnanometerschaal oplossen, deze systemen werken onder omstandigheden die niet ideaal zijn voor de studie van biologische monsters. Detectie van individuele fluorescerende labels die zijn bevestigd aan biologische moleculen van belang met behulp van ladingsgekoppelde apparaten (CCD's) - arrays van siliciumchips die binnenkomend licht omzetten in een elektrische lading, heeft resoluties van maar liefst vijf nanometer opgeleverd. Echter, tot nu toe was deze technologie niet in staat om afzonderlijke moleculen of afstanden tussen een paar moleculen van veel minder dan 20 nanometer in beeld te brengen.
Chu en zijn co-auteurs waren in staat om dezelfde CCD-fluorescentietechnologie te gebruiken om afstanden op te lossen met subnanometerprecisie en nauwkeurigheid door een truc van het licht te corrigeren. De elektrische ladingen in een CCD-array worden gecreëerd wanneer fotonen het silicium raken en elektronen losmaken, waarbij de sterkte van de lading evenredig is met de intensiteit van de invallende fotonen. Echter, afhankelijk van waar een foton precies het oppervlak van een siliciumchip raakt, er kan een klein verschil zijn in hoe het foton wordt geabsorbeerd en of het een meetbare lading genereert. Deze niet-uniformiteit in de respons van de CCD-siliciumarray op binnenkomende fotonen, wat waarschijnlijk een artefact is van het fabricageproces van de chip, resulteert in een vervaging van pixels waardoor het moeilijk is om twee punten op te lossen die zich binnen enkele nanometers van elkaar bevinden.
"We hebben een actief feedbacksysteem ontwikkeld waarmee we het beeld van een enkel fluorescerend molecuul overal op de CCD-array kunnen plaatsen met subpixelprecisie, wat ons op zijn beurt in staat stelt om in een regio te werken die kleiner is dan de typische lengteschaal van drie pixels van de CCD-niet-uniformiteit, " zegt Pertsinidis, wie is de hoofdauteur van de Nature-paper. "Met dit feedbacksysteem plus het gebruik van extra optische stralen om het microscoopsysteem te stabiliseren, we kunnen een gekalibreerd gebied op de siliciumarray creëren waar de fout als gevolg van niet-uniformiteit wordt teruggebracht tot 0,5 nanometer. Door de moleculen die we willen meten in het midden van dit gebied te plaatsen, kunnen we subnanometerresolutie verkrijgen met behulp van een conventionele optische microscoop die je in elk biologielab kunt vinden."
Chu zegt dat de mogelijkheid om het podium van een microscoop over kleine afstanden te verplaatsen en het geometrische centrum (zwaartepunt) van het beeld te berekenen, het niet alleen mogelijk maakt om de niet-uniformiteit van de fotorespons tussen pixels te meten, maar ook om de niet-uniformiteit binnen elke afzonderlijke pixel te meten.
"Als we deze niet-uniformiteit kennen, kunnen we correcties aanbrengen tussen de schijnbare positie en de werkelijke positie van het zwaartepunt van de afbeelding, ", zegt Chu. "Omdat deze niet-uniforme reactie is ingebouwd in de CCD-array en niet van dag tot dag verandert, ons actieve feedbacksysteem stelt ons in staat om herhaaldelijk beelden te maken op dezelfde positie van de CCD-array."
Pertsinidis blijft samen met Chu en anderen in de groep werken aan de verdere ontwikkeling en toepassing van deze superresolutietechniek. Naast het humane RNA-polymerase II-systeem, hij en de groep gebruiken het om de structuur te bepalen van de epitheliale cadherine-moleculen die verantwoordelijk zijn voor de cel-tot-cel-adhesie die weefsel en andere biologische materialen bij elkaar houdt. Pertsinidis, Zhang, en een andere postdoc in de onderzoeksgroep van Chu, Zong Ryul-park, gebruiken deze techniek ook om 3D-metingen te maken van de moleculaire organisatie in hersencellen.
"Het idee is om de structuur en dynamiek te bepalen van het vesikelfusieproces dat de neurotransmittermoleculen vrijgeeft die door neuronen worden gebruikt om met elkaar te communiceren, Pertsinidis zegt. "Op dit moment krijgen we in-situ metingen met een resolutie van ongeveer 10 nanometer, maar we denken dat we deze resolutie naar binnen twee nanometer kunnen duwen."
In een samenwerking met Joe Gray, Berkeley Lab's Associate Director voor Life Sciences en een vooraanstaand kankeronderzoeker, postdocs in de onderzoeksgroep van Chu gebruiken ook de superresolutietechniek om de aanhechting van signaalmoleculen aan het RAS-eiwit te bestuderen, die in verband is gebracht met een aantal kankers, inclusief die van de borst, alvleesklier, long en dikke darm. Dit onderzoek zou kunnen helpen verklaren waarom kankertherapieën die bij sommige patiënten goed werken, bij andere niet effectief zijn.
Naast de biologische toepassingen, Pertsinidis, Zhang en Chu in hun Natuur paper zegt dat hun superresolutietechniek ook waardevol zou moeten zijn om nauwkeurige fotometrische beeldvormingssystemen in atoomfysica of astronomie te karakteriseren en te ontwerpen, en nieuwe instrumenten in optische lithografie en nanometrologie mogelijk te maken.
 Duel van de inflammatoire hoofdregulatoren - inzichten voor het ontdekken van medicijnen
Duel van de inflammatoire hoofdregulatoren - inzichten voor het ontdekken van medicijnen Strategie suggereert manieren om zich voor te bereiden op opkomende antibioticaresistente superbacteriën
Strategie suggereert manieren om zich voor te bereiden op opkomende antibioticaresistente superbacteriën Onderzoekers ontsluiten kankerverwekkend mechanisme van E. coli-toxine met synthetische biologie
Onderzoekers ontsluiten kankerverwekkend mechanisme van E. coli-toxine met synthetische biologie Synthetische chemie haalt antikankerverbindingen uit de zeeslak en het laboratorium in
Synthetische chemie haalt antikankerverbindingen uit de zeeslak en het laboratorium in Eiwitstructuur zou nieuwe behandelingen voor cystische fibrose kunnen ontsluiten
Eiwitstructuur zou nieuwe behandelingen voor cystische fibrose kunnen ontsluiten
Hoofdlijnen
- Gemuteerd kikkergen stoot roofdieren af
- Drie mechanismen van genetische recombinatie in prokaryoten
- Wie heeft klonen bedacht en wanneer?
- De isovormen van het HP1-eiwit reguleren de organisatie en structuur van heterochromatine
- Manitobas goudvleugelzangers:'s werelds laatste pure populatie die wordt geraakt door lokale en verre instandhoudingsproblemen
- The Differences in Fraternal & Paternal Twins
- Verander je geliefde in een boom met Bios Urn
- IJsbeerblogs onthullen gevaarlijke kloof tussen feiten en meningen over klimaatverandering
- Cel Life Functies
- Nanodeeltjes zorgen ervoor dat kankercellen zichzelf vernietigen

- Nanostructuren met meerdere componenten met instelbare optische eigenschappen
- Nieuw systeem kan cocaïne in lage concentraties detecteren

- Toediening van geneesmiddelen met nanodeeltjes zorgt voor pijnverlichting en een effectiever alternatief voor opioïden in dierstudies

- Nieuwslaserontwerp biedt goedkopere meerkleurenuitvoer

 Onderzoekers ontwikkelen een op grafeenoxide gebaseerde snelle test om infecties op te sporen
Onderzoekers ontwikkelen een op grafeenoxide gebaseerde snelle test om infecties op te sporen Simple Robotic Arm & Hand Science Projects
Simple Robotic Arm & Hand Science Projects Wat is de toekomst van kernenergie?
Wat is de toekomst van kernenergie?  Nieuw collider-concept zou kwantumtheorieën tot het uiterste drijven
Nieuw collider-concept zou kwantumtheorieën tot het uiterste drijven Drijvende steden:de toekomst of een aangespoeld idee?
Drijvende steden:de toekomst of een aangespoeld idee? Kinderen leren hoe een Compass te gebruiken
Kinderen leren hoe een Compass te gebruiken Hoe het Scroll Grid te gebruiken in het Everyday Math-programma
Hoe het Scroll Grid te gebruiken in het Everyday Math-programma Nieuw boek laat zien dat het bestaan van transgenders geen recent fenomeen is
Nieuw boek laat zien dat het bestaan van transgenders geen recent fenomeen is
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | Dutch | Danish | Norway | Portuguese | German |

-
Wetenschap © https://nl.scienceaq.com

