
Wetenschap
Als het gaat om de levering van medicijnen, Grootte doet er toe
(PhysOrg.com) -- Een van de grote beloften van nanotechnologieën ligt in het vermogen om medicijnbevattende nanodeeltjes te creëren die zijn versierd met targetingmoleculen die kankercellen herkennen en zich eraan binden, het verschaffen van medicijnafgifte alleen op de plaats van de beoogde cellen. Een dergelijke plaatsspecifieke medicijnafgifte zou niet alleen de kankerdodende activiteit van een medicijnlading verhogen, maar ook mogelijke bijwerkingen verminderen door de hoeveelheid medicijn die gezond weefsel bereikt sterk te beperken of zelfs te elimineren.
Het blijkt, Hoewel, dat niet alle combinaties van targeting agent-nanodeeltjes in staat zijn om hun doelen met dezelfde effectiviteit te bereiken en binnen te gaan. Om wat rationaliteit te brengen in het proces van het ontwerpen van gerichte geneesmiddelen voor het afleveren van medicijnen, K. Dane Wittrup, doctoraat, en afgestudeerde student Micheal Schmidt van het Massachusetts Institute of Technology hebben een wiskundig model ontwikkeld dat de omvang en specificiteit voorspelt van de tumoropname van vehikels voor medicijnafgifte, variërend in grootte van kleine peptiden tot grote liposomen. Dit werk is gepubliceerd in het tijdschrift Moleculaire kankertherapieën .
Het model ontwikkeld door de Schmidt en Wittrup, die lid is van het MIT-Harvard Center of Cancer Nanotechnology Excellence, is verantwoordelijk voor de grootte van een bepaald medicijnafgiftemiddel en een verscheidenheid aan gemakkelijk te meten eigenschappen, inclusief hoe gemakkelijk het biologische barrières passeert en hoe stevig het bindt aan een doelwit in reageerbuisexperimenten. De onderzoekers merken op dat ondanks de eenvoud van hun model, het voorspelt nauwkeurig het gedrag van HER2-gerichte constructies in een muismodel van kanker en van CEA-gerichte constructies bij mensen. In feite, het lijkt erop dat grootte en doelaffiniteit verantwoordelijk zijn voor het grootste deel van de variabiliteit in tumoropname.
Een interessante voorspelling die het model doet, is dat grote constructies, zoals nanodeeltjes, en kleintjes, inclusief targeting peptiden, zal meer medicijn in een tumor afgeven dan mediumconstructies, zoals gemanipuleerde antilichaamfragmenten. Echter, het model voorspelt ook dat de afgifte aan tumoren door nanodeeltjes met een diameter van meer dan 50 nanometer niet veel zal verbeteren wanneer gerichte middelen aan de nanodeeltjes worden toegevoegd.
Dit werk, die gedetailleerd wordt beschreven in een document met de titel, "Een modelleringsanalyse van de effecten van moleculaire grootte en bindingsaffiniteit op tumortargeting, " werd ondersteund door de NCI Alliance for Nanotechnology in Cancer, een alomvattend initiatief dat is ontworpen om de toepassing van nanotechnologie op de preventie te versnellen, diagnose, en behandeling van kanker. Een samenvatting van dit artikel is beschikbaar op de website van het tijdschrift.
Aangeboden door National Cancer Institute (nieuws:web)
 Het energiebeleid van China moet de luchtkwaliteit in evenwicht brengen, doelstellingen voor koolstofemissies en waterschaarste
Het energiebeleid van China moet de luchtkwaliteit in evenwicht brengen, doelstellingen voor koolstofemissies en waterschaarste Langdurige studie toont snelle vorming van micro- en nanoplastics in het milieu
Langdurige studie toont snelle vorming van micro- en nanoplastics in het milieu How Long Do Crickets Live?
How Long Do Crickets Live?  Everest:ik reisde de doodszone in om 's werelds hoogste weerstation te installeren
Everest:ik reisde de doodszone in om 's werelds hoogste weerstation te installeren Hernieuwbare energie is een gemeenschappelijke basis voor Democraten en Republikeinen
Hernieuwbare energie is een gemeenschappelijke basis voor Democraten en Republikeinen
Hoofdlijnen
- Pharmacy Research Topics
- De voordelen van het hebben van een groot aantal chromosomen
- Hoe de Amoeben zich reproduceren?
- De microbiologische kunst van het maken van een betere worst
- Nieuwe CRISPR-tool richt zich op RNA in zoogdiercellen
- Welk enzym is verantwoordelijk voor het verlengen van de RNA-keten?
- In de mangoestenmaatschappij immigranten zijn een bonus - als ze tijd krijgen om zich te vestigen
- Verschillen en overeenkomsten tussen eencellig en cellulair
- Waar bevinden zich lipiden in het lichaam?
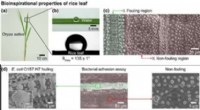
- Onderzoekers bestuderen superafstotende oppervlakken voor veiliger fruit, groenten
- Oplossing van DNA en gouden nanostaafjes die in staat zijn tot zes fundamentele logische bewerkingen
- Tweedimensionale multiferroics in monolaaggroep IV monochalcogeniden

- Diamond verbetert de prestaties van elektronische apparaten

- Team beweert een monster van stanene te hebben gemaakt

 Trapkracht:de opkomst van bakfietsen in Duitsland
Trapkracht:de opkomst van bakfietsen in Duitsland Emissievrije dieselverbranding met een niet-evenwichtsplasma-ondersteund MnO2-filter
Emissievrije dieselverbranding met een niet-evenwichtsplasma-ondersteund MnO2-filter Ticketmaster UK zegt dat klantinformatie mogelijk is gestolen
Ticketmaster UK zegt dat klantinformatie mogelijk is gestolen Nieuwe recensie zegt dat de theorie van ineffectieve leerstijlen aanhoudt in het onderwijs
Nieuwe recensie zegt dat de theorie van ineffectieve leerstijlen aanhoudt in het onderwijs Glad als het droog is
Glad als het droog is Afstembare metalen nanostructuren voor brandstofcellen, batterijen en zonne-energie
Afstembare metalen nanostructuren voor brandstofcellen, batterijen en zonne-energie Greenpeace bekritiseert palmolie-industrie in Indonesië vanwege ontbossing
Greenpeace bekritiseert palmolie-industrie in Indonesië vanwege ontbossing Een uitzonderlijk stabiele katalysator met één atoom
Een uitzonderlijk stabiele katalysator met één atoom
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

