
Wetenschap
Door biologische moleculen te modelleren over langere tijdschalen, een nieuw algoritme kan helpen om ziekten beter te begrijpen

Structureel model van Alzheimer Amyloïde A-beta 1-42 peptidefibril afgeleid van een experimentele structuur (VOB:2MXU). De fibrillaire aggregaten werken als celtoxines bij het begin en de progressie van de ziekte van Alzheimer. Krediet:Emanuel Peter
eiwitten, de alomtegenwoordige werkpaarden van de biochemie, zijn enorme moleculen waarvan de functie afhangt van hoe ze zich vouwen tot ingewikkelde structuren. Om te begrijpen hoe deze moleculen werken, onderzoekers gebruiken computermodellering om te berekenen hoe eiwitten vouwen.
Nutsvoorzieningen, een nieuw algoritme kan die vitale simulaties versnellen, waardoor ze fenomenen kunnen modelleren die voorheen onbereikbaar waren. De resultaten kunnen wetenschappers uiteindelijk helpen om ziekten zoals Alzheimer beter te begrijpen en te behandelen. zei Emanuel Peter, een chemicus aan de Universiteit van Regensburg. Zijn werk aan de nieuwe techniek wordt deze week beschreven in The Journal of Chemical Physics .
Conventionele simulaties, met behulp van moleculaire dynamica en Monte Carlo-methoden, zijn over het algemeen succesvol geweest in het modelleren van biologische moleculen zoals eiwitten. Om te bepalen hoe eiwitten vouwen, de simulatie zoekt naar configuraties die overeenkomen met lagere en lagere energietoestanden. Eventueel, het vindt de laagste energietoestand, wat een stabiele vouw geeft. Maar terwijl de simulatie zoekt, het kan een configuratie tegenkomen met een iets hogere energie, die een barrière vormt die het algoritme belemmert.
Als gevolg van deze vertragingen, conventionele methoden kunnen alleen moleculair gedrag simuleren dat optreedt over korte tijdschalen van een paar honderd microseconden. Veel verschijnselen, zoals bepaalde eiwitplooien of een geneesmiddel dat bindt aan een mogelijk doelwit, gebeuren in de loop van een paar seconden, minuten of zelfs dagen. Het simuleren van zulke lange tijdschalen zou te veel rekentijd vergen met alleen conventionele benaderingen.
Om de simulaties te versnellen, onderzoekers kunnen energie in het systeem injecteren, die het model over alle energiebarrières duwt. Maar een van de grootste uitdagingen voor deze methoden is het definiëren van de coördinaten die het systeem beschrijven - wat, bijvoorbeeld, kan de lengte zijn tussen atomen in het molecuul, en de hoeken tussen bindingen. traditioneel, onderzoekers bepalen de coördinaten voordat ze met de simulatie beginnen. Elke tijdstap langs elke coördinaat is afhankelijk van de vorige stap. Maar deze afhankelijkheid kan de simulatie vertekenen.
Het nieuwe algoritme van Peter vermijdt deze vooringenomenheid. Hij vond een gegeneraliseerd coördinatensysteem waarin elke tijdstap niet afhankelijk is van de vorige stap. "Er zijn maar een paar parameters nodig, en er is geen menselijke intuïtie vereist, die het simulatieresultaat mogelijk kunnen vertekenen, " hij zei.
Om het nieuwe algoritme te testen, Peter gebruikte het om water te modelleren, een peptide genaamd dialanine, het vouwen van een ander peptide genaamd TrpCage, en het klonteren van amyloïde-beta 25-35, dat zijn eiwitfragmenten die geassocieerd zijn met de ziekte van Alzheimer. In ieder geval, zijn techniek meldt de simulaties te hebben versneld. En de simulaties van amyloïde-bèta zouden kunnen helpen verklaren waarom de ziekte van Alzheimer moeilijk te behandelen is.
Bij de ziekte van Alzheimer, amyloïde-bèta-eiwitfragmenten aggregeren samen, vormt harde plaque die zich tussen neuronen ophoopt en deze verstoort. Amyloïde-beta is ook een toxine, wat leidt tot neuronale celdood en degeneratie van neuronale functie. De nieuwe simulaties suggereren dat amyloïde-bèta een reeks structuren kan aannemen. Deze structurele flexibiliteit zou de reden kunnen zijn waarom sommige medicijnen die de aggregatie proberen te remmen, niet succesvol zijn geweest. zei Petrus. Wanneer die medicijnen binden aan amyloïde-bèta, de amyloïde-bèta verandert gewoon van vorm, waardoor het blijft samenklonteren. Het medicijn wordt opgenomen in het aggregaat en de plaque.
Deze vorm van structurele flexibiliteit, conformatie-entropie genoemd, is ook een belangrijk kenmerk van andere peptiden die toxische plaques vormen bij ziekten zoals de ziekte van Huntington, Type 2 diabetes, en de ziekte van Parkinson. Het nieuwe algoritme kan daarom ook nuttig zijn om deze andere ziekten te begrijpen.
 Smaakwetenschappers creëren een lexicon van termen om nuances van rum te beschrijven
Smaakwetenschappers creëren een lexicon van termen om nuances van rum te beschrijven Vallen voor energiebronmoleculen in cellen
Vallen voor energiebronmoleculen in cellen De lengte van een gebogen lijn berekenen
De lengte van een gebogen lijn berekenen Ontdekking van hoe mensen de geur van de dood ervaren, kan levens redden
Ontdekking van hoe mensen de geur van de dood ervaren, kan levens redden Studie ontrafelt het mysterie van antimicrobiële kikkersecreties
Studie ontrafelt het mysterie van antimicrobiële kikkersecreties
 Het omzetten van voedselafval in diervoeder kan een deel van de uitstoot van vee wegnemen
Het omzetten van voedselafval in diervoeder kan een deel van de uitstoot van vee wegnemen CO2 bereikt hoogste niveau in meer dan 4 miljoen jaar
CO2 bereikt hoogste niveau in meer dan 4 miljoen jaar Bosbranden zetten huizen in brand, land in 10 staten in het westen van de VS
Bosbranden zetten huizen in brand, land in 10 staten in het westen van de VS Kooldioxidegehalte lager dan gedacht tijdens superkasperiode
Kooldioxidegehalte lager dan gedacht tijdens superkasperiode Onderzoekers simuleren processen die heersen in vroege magma-oceanen
Onderzoekers simuleren processen die heersen in vroege magma-oceanen
Hoofdlijnen
- Bioreactoren op een chip vernieuwen beloften voor algenbiobrandstoffen
- Wetenschappers volgen haaien die DNA-fragmenten uit de zee plukken
- Hoe wordt glucose opgeslagen in plantencellen?
- Het belang van het bestuderen van de DNA-genetica van het menselijk geslacht
- Kruising met Neanderthalers gaf mensen virusbescherming
- Wat gebeurt er met plantaardige en dierlijke cellen wanneer ze worden geplaatst in hypertone, hypotone en isotone omgevingen?
- Wat is Ceramide?
- Als het gaat om de dreiging van uitsterven, grootte doet er toe
- Stamcelvaccins: de nieuwe grens in kanker-therapie?
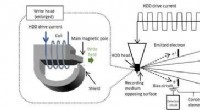
- Nieuwe analytische technologie voor de schrijfkop van de harde schijf kan de capaciteit van de harde schijf vergroten
- Onderzoekers nemen terahertz-datalinks door de bocht

- Op zoek naar donkere materie in de buurt van neutronensterren met radiotelescopen
- Hoe verplaatst elektriciteit zich van de windturbine naar de bedrijven en gemeenschappen die het kopen?

- Fotosynthese in een nieuw licht gezien door snelle röntgenpulsen

 Mechanische voordeelschroeven berekenen
Mechanische voordeelschroeven berekenen Drie variabelen die van invloed kunnen zijn op activiteiten van een enzym
Drie variabelen die van invloed kunnen zijn op activiteiten van een enzym Bosbranden woeden over miljoen hectare terwijl hittegolf het westen van de VS verstikt, Canada
Bosbranden woeden over miljoen hectare terwijl hittegolf het westen van de VS verstikt, Canada Belemmeringen om te stemmen bij verkiezingen in verband met een grotere kans om onverzekerd te zijn
Belemmeringen om te stemmen bij verkiezingen in verband met een grotere kans om onverzekerd te zijn Sla heeft het:machine learning voor cr-optimalisatie
Sla heeft het:machine learning voor cr-optimalisatie Onderzoekers onderzoeken Turkije om de impact van de klimaattoezeggingen van Parijs in 2015 op een nationale economie te beoordelen
Onderzoekers onderzoeken Turkije om de impact van de klimaattoezeggingen van Parijs in 2015 op een nationale economie te beoordelen Onderzoekers ontwikkelen moleculaire LEGO-kit om nanoblokjes te maken
Onderzoekers ontwikkelen moleculaire LEGO-kit om nanoblokjes te maken Op weg naar de ontwikkeling van medicijnen voor aan veroudering gerelateerde ziekten
Op weg naar de ontwikkeling van medicijnen voor aan veroudering gerelateerde ziekten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

