
Wetenschap
Ammoniakdissociatie in waterige oplossing:de reactievergelijking
Wanneer een opgeloste stof in water oplost, kan deze eenvoudigweg dissociëren in de samenstellende ionen of reageren met het oplosmiddel. Natriumchloride ioniseert bijvoorbeeld tot Na⁺ en Cl⁻ zonder de watermoleculen te veranderen. Ammoniak gedraagt zich anders:het accepteert als basis een proton uit water en vormt daarbij nieuwe ionen.
Jupiterimages/Photos.com/Getty Images
Stap 1:Identificeer de reactanten
De formule voor ammoniak is NH₃ en voor water is dit H₂O.
Stap 2:een proton overdragen
Door een proton (H⁺) uit water te verwijderen, ontstaat het hydroxide-ion (OH⁻). Door dat proton aan ammoniak toe te voegen, wordt het omgezet in het ammoniumion (NH₄⁺).
Stap 3:Kosten toewijzen
Door de protonenoverdracht blijft water negatief geladen (OH⁻) en ammoniak positief geladen (NH₄⁺). Daarom dragen de producten deze kosten.
Stap 4:schrijf de gebalanceerde vergelijking
NH₃ + H₂O → NH₄⁺ + OH⁻
Omdat de evenwichtsconstante voor deze basehydrolyse (K_b ≈ 1,8×10⁻⁵) klein is, is de reactie slechts gedeeltelijk voltooid; ammoniak blijft grotendeels ongedissocieerd in verdunde oplossingen.
Voor een diepere duik, raadpleeg het Journal of Chemical Education of de RSC Learning Chemistry pagina.
 Wat is de formule voor ijzerjodaten met ferrische jodide?
Wat is de formule voor ijzerjodaten met ferrische jodide?  Aardolieraffinage:belangrijke stoffen en processen - Katalysatoren uitgelegd
Aardolieraffinage:belangrijke stoffen en processen - Katalysatoren uitgelegd  Wat is een atoom dat het meest nauwkeurig wordt beschreven?
Wat is een atoom dat het meest nauwkeurig wordt beschreven?  Zijn de eigenschappen van verbindingen zoiets als een gemiddelde zijn samenstellende elementen?
Zijn de eigenschappen van verbindingen zoiets als een gemiddelde zijn samenstellende elementen?  Wat maakt koolstof plus zuurstof?
Wat maakt koolstof plus zuurstof?
 Hoe de Amerikaanse chemische oorlogvoering in Vietnam een blijvende ramp ontketende
Hoe de Amerikaanse chemische oorlogvoering in Vietnam een blijvende ramp ontketende Onderzoekers pleiten voor consensus in de voedselvoorzieningsketen
Onderzoekers pleiten voor consensus in de voedselvoorzieningsketen Een voorbeeld van behoudsmassa?
Een voorbeeld van behoudsmassa?  Welk klimaattype wordt geassocieerd met kaal land?
Welk klimaattype wordt geassocieerd met kaal land?  Onderzoekers onderzoeken hoe burgers agenten kunnen worden van veranderingen in het milieu
Onderzoekers onderzoeken hoe burgers agenten kunnen worden van veranderingen in het milieu
Hoofdlijnen
- Decennia lang onderzoek wijst uit dat bedreigde walvissen minder baby's krijgen
- Wat is het idee dat nakomelingen een mix van genetisch materiaal van beide ouders zijn?
- Hoe worden Saccos gevormd?
- Verloren Australische duiker zwom mijlen naar kust gestalkt door haai
- Wat doen de ribosomen voor dierencel?
- Wat zijn twee soorten RNA?
- Wat is het trechtervormige deel van je oor dat wordt genoemd?
- Louis Pasteur:de vader van de bacteriologie - ontdekkingen en impact
- Wat zijn enkele veel voorkomende wetenschapsonderwerpen?
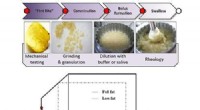
- Een betere magere aardappelchips ontwerpen
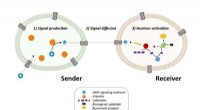
- Levensechte cellen kunnen nu over lange afstanden communiceren via signaalversterking
- Een veranderende platina-elektrode observeren

- Een manier ontwerpen om zuurstof injecteerbaar te maken

- Onderzoekers halen natuurlijk voorkomende melanine op grote schaal uit paddenstoelen

 Hoe wetenschappers afstemmen op het universum, Mens
Hoe wetenschappers afstemmen op het universum, Mens Atlas is rockstar cross-stepper over lastig terrein
Atlas is rockstar cross-stepper over lastig terrein Bestaat Gamma Ray voornamelijk uit pure energie en geen massa?
Bestaat Gamma Ray voornamelijk uit pure energie en geen massa?  Genetici ontdekken nieuwe ondersoorten van wilde geiten via oud DNA
Genetici ontdekken nieuwe ondersoorten van wilde geiten via oud DNA Hoe werken glow-in-the-dark dingen?
Hoe werken glow-in-the-dark dingen?  Wat zijn de hoofdsteden van binnenvlaktes?
Wat zijn de hoofdsteden van binnenvlaktes?  Met SpaceX-partnerschap, ISS gaat zijn Gouden Eeuw in, maar wat komt er daarna?
Met SpaceX-partnerschap, ISS gaat zijn Gouden Eeuw in, maar wat komt er daarna? Betekent kinetische energie om te bewegen?
Betekent kinetische energie om te bewegen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

