
Wetenschap
Het schrijven van chemische formules beheersen:een praktische gids
Adrian Hernandez/iStock/Getty Images
Gebruik het periodiek systeem
Het schrijven van chemische formules begint met een goed begrip van het periodiek systeem. In de tabel staan alle bekende elementen vermeld, waarbij de volledige naam wordt gecombineerd met een beknopt symbool:H voor waterstof, Cl voor chloor, enzovoort. Sommige symbolen volgen de Engelse naam van het element (bijvoorbeeld O voor zuurstof), terwijl andere van Latijnse of Griekse wortels komen (Na voor natrium, afgeleid van *natrium*). Als een symbool niet meteen duidelijk is, is het periodiek systeem uw referentie.
Chemische symbolen identificeren
Voordat u een formule opstelt, identificeert u elk atoom in de verbinding of het molecuul. Het gewone keukenzout is bijvoorbeeld natriumchloride; schrijf Na voor natrium en Cl voor chloride. De resulterende formule is NaCl. Voor covalente verbindingen – die gevormd tussen twee niet-metalen – vertalen de namen zich vaak rechtstreeks in symbolen. Voorvoegsels geven meerdere atomen aan:koolstofdioxide wordt CO₂ omdat het voorvoegsel ‘di-’ twee zuurstofatomen signaleert.
De valentie bepalen
Ionische verbindingen omvatten geladen atomen. Veel periodieke tabellen vermelden typische valenties. Metalen uit groep 1 zijn +1 kationen, groep 2 zijn +2 en overgangsmetalen (groepen 3–12) kunnen een reeks ladingen vertonen. Elementen in groepen 13–18 kunnen variabele ladingen hebben, terwijl groepen 15–17 doorgaans anionen met negatieve ladingen vormen. Het kennen van deze kosten is essentieel voor het in evenwicht brengen van de algemene formule.
De kosten in evenwicht brengen
Breng de totale lading in evenwicht om ervoor te zorgen dat de verbinding neutraal is. Magnesium (Mg) heeft bijvoorbeeld een lading van +2 en het oxide-ion (O²⁻) heeft –2. Het combineren van één Mg²⁺ met één O²⁻ levert MgO op, een neutrale formule. Op dezelfde manier zijn voor het balanceren van magnesiumchloride twee chloride-ionen (Cl⁻) nodig voor elk magnesiumion, waardoor MgCl₂ ontstaat.
De chemische formule schrijven
Subscripts geven het aantal atomen van elk element aan. Er wordt geïmpliceerd dat er sprake is van een enkel atoom, dus er wordt geen subscript “1” geschreven. In MgO duidt de afwezigheid van een subscript één magnesium- en één zuurstofatoom aan. Als er meerdere atomen van hetzelfde element aanwezig zijn, volgt het subscript het symbool van het element:MgCl₂ toont twee chlooratomen per magnesium.
Aanvullende tips
- Verbindingen die eindigen op “‑ide” behoren meestal tot de groepen 15–17.
- Romeinse cijfers tussen haakjes, zoals Fe(II), geven de lading van het ion aan (hier +2).
- Polyatomische ionen (bijvoorbeeld hydroxide OH⁻) worden tussen haakjes gegroepeerd als ze meerdere keren voorkomen:Al(OH)₃ is aluminiumhydroxide.
Als u deze regelmatig oefent, worden deze richtlijnen een tweede natuur, waardoor u met vertrouwen nauwkeurige chemische formules kunt schrijven.
 Een nieuwe energiebesparende LED-fosfor
Een nieuwe energiebesparende LED-fosfor Hoe reageert muriatinezuur met asfalt?
Hoe reageert muriatinezuur met asfalt?  Welke chemische structuren en bindingen zou u verwachten te vinden in een onverzadigde aromatische koolwaterstof?
Welke chemische structuren en bindingen zou u verwachten te vinden in een onverzadigde aromatische koolwaterstof?  Naarmate de temperatuur de snelheid van een enzym-gekatalyseerde reactie verlaagt, ook waarom?
Naarmate de temperatuur de snelheid van een enzym-gekatalyseerde reactie verlaagt, ook waarom?  Welk periodiek systeem is het meest reactief?
Welk periodiek systeem is het meest reactief?
 Nieuw project zal de ontwikkeling van de Iraanse economie bestuderen
Nieuw project zal de ontwikkeling van de Iraanse economie bestuderen Hoe duurzame landbouw
Hoe duurzame landbouw  Smaaktest:kan smaakzin de levensduur beïnvloeden?
Smaaktest:kan smaakzin de levensduur beïnvloeden?  Zalmstudie kan het plan van Trump om de waterleveringen aan Central Valley-boerderijen te stimuleren, verijdelen
Zalmstudie kan het plan van Trump om de waterleveringen aan Central Valley-boerderijen te stimuleren, verijdelen Waarom zou een veer in natte gebieden uit de grond kunnen stromen?
Waarom zou een veer in natte gebieden uit de grond kunnen stromen?
Hoofdlijnen
- Waar vindt anaërobe ademhaling plaats?
- Wat zijn de organismen zoals bacteriën en schimmels die ontleeden?
- Waarom vrouwen zich vaak kouder voelen dan mannen:de wetenschappelijke en systemische factoren
- Hoe beslissen wetenschappers welke informatie te verzamelen?
- Welke structuur van bacteriën wordt bepaald door gramkleuring?
- Informatieverwerking beperkt de manier waarop E. coli-bacteriën door chemische gradiënten navigeren
- Wat scheidt de klasse insecta in Morethan één deel?
- Speciatie zonder geografische isolatie wordt hoe genoemd?
- Wat doen wetenschappers na een onderzoek?
- Exotische koolstofmicrokristallen in meteorietstof

- Geminiaturiseerde massaspectrometer voor verkenning van Mars heeft een enorm potentieel

- Moleculaire dynamische simulatie werpt nieuw licht op de vorming van methaanhydraat

- Een efficiëntere op membraan gebaseerde generator voor het oogsten van osmotisch vermogen (update)
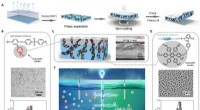
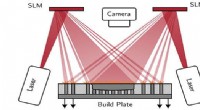
- Holografische bundelvorming om metallic 3D-printen een boost te geven
 Israëlische startups sluiten zich aan bij bedrijven die in het laboratorium gekweekt schoon vlees maken
Israëlische startups sluiten zich aan bij bedrijven die in het laboratorium gekweekt schoon vlees maken Wat is verplaatsing in de wiskunde?
Wat is verplaatsing in de wiskunde?  Een woud van nanostaafjes:verbazingwekkende nanostructuren gecreëerd door depositie onder een flitsende hoek
Een woud van nanostaafjes:verbazingwekkende nanostructuren gecreëerd door depositie onder een flitsende hoek Waarom is de belangrijkste reden dat oceanische korst zwaarder is dan continentale korst?
Waarom is de belangrijkste reden dat oceanische korst zwaarder is dan continentale korst?  Het publiek oordeelt snel over nieuwe technologieën
Het publiek oordeelt snel over nieuwe technologieën Geeft een niet -metaal elektronen weg in chemische reactie?
Geeft een niet -metaal elektronen weg in chemische reactie?  Wat gebeurt er als wit licht door een groene glazen fles gaat?
Wat gebeurt er als wit licht door een groene glazen fles gaat?  Is nevels zichtbaar op een heldere nacht met het blote oog?
Is nevels zichtbaar op een heldere nacht met het blote oog?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

