
Wetenschap
Het bindingsvermogen van koolstof:valentie-elektronen begrijpen
Dit is waarom:
* Elektronische configuratie: Koolstof heeft atoomnummer 6, wat betekent dat het 6 elektronen heeft. De elektronische configuratie is 2,4. Dit betekent dat het 2 elektronen in de eerste schil heeft en 4 elektronen in de tweede schil.
* Valentie-elektronen: De buitenste schilelektronen worden valentie-elektronen genoemd. In het geval van koolstof zijn dit de 4 elektronen in de tweede schil.
* Delen: Koolstof kan zijn vier valentie-elektronen delen met andere atomen om covalente bindingen te vormen. Hierdoor kan het een stabiel octet (8 elektronen) in zijn buitenste schil bereiken.
Dit vermogen om vier bindingen te vormen maakt koolstof tot een uniek en veelzijdig element, waardoor het een breed scala aan organische moleculen kan creëren.
 Is het aantal atomen in een moleculaire formule altijd groter dan empirisch?
Is het aantal atomen in een moleculaire formule altijd groter dan empirisch?  Waarom maakte de Zwitserse chemicus Aime Argand de olielamp?
Waarom maakte de Zwitserse chemicus Aime Argand de olielamp?  Wat is het atomaire massagetal van een isotoop met 5 en 6 neutronen?
Wat is het atomaire massagetal van een isotoop met 5 en 6 neutronen?  Hoe breng je CH3OH O2 in evenwicht CO2 H2O?
Hoe breng je CH3OH O2 in evenwicht CO2 H2O?  Hoeveel protrons en elektronen zijn aanwezig in een kaliumatoom?
Hoeveel protrons en elektronen zijn aanwezig in een kaliumatoom?
 Circulaire steden van de wereld:wat kan groene infrastructuur doen?
Circulaire steden van de wereld:wat kan groene infrastructuur doen? De barmsijsvink-saga:hoe twee vogelsoorten zojuist één zijn geworden
De barmsijsvink-saga:hoe twee vogelsoorten zojuist één zijn geworden  Onderzoek onthult hoe planten en bodembiota in de loop van de tijd ecosystemen vormen
Onderzoek onthult hoe planten en bodembiota in de loop van de tijd ecosystemen vormen  Parels van wijsheid:Japanse gekweekte boerderijen glinsteren nog steeds
Parels van wijsheid:Japanse gekweekte boerderijen glinsteren nog steeds Napels schrijlings op een rommelende megavulkaan
Napels schrijlings op een rommelende megavulkaan
Hoofdlijnen
- Welke organel is verantwoordelijk voor beweging en ondersteuning van de cel?
- Waarom wordt de cultuurbouillon voortdurend gemengd?
- Wat ondersteunen recente onderzoeksresultaten Darwins Evolution Theory of Evolution?
- Hoe vleermuizen, wolven en motten ons leven kunnen vormen
- Ecosysteemherstel is een integraal onderdeel van het herstel van de mensheid van COVID-19
- Wat voor soort cellen reproduceren zich door de procesmeiose?
- Onderzoek naar de pijlers van de microbiologie:domeinen, groepen, disciplines en kernactiviteiten
- Waar vindt transcriptie plaats in de cel?
- Is de beste definitie van een prokaryote?
- Nieuw, gladde toiletcoating zorgt voor schoner doorspoelen, bespaart water

- Hoe gestresste tumorcellen aan celdood ontsnappen:nieuw mechanisme ontdekt
- Wetenschappers duwen microscopie naar submoleculaire resolutie

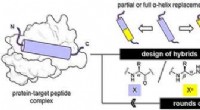
- Oligourea-foldamers bootsen peptiden alfa-helices na en binden effectief aan medicijndoelen
- Video:Waarom Antarctische vissen niet doodvriezen

 Rusland meldt niet-standaard luchtlek op ruimtestation
Rusland meldt niet-standaard luchtlek op ruimtestation Verschillende onderwerpen voor onderzoeksprojecten
Verschillende onderwerpen voor onderzoeksprojecten Verkoop Renault daalt in verzwakkende automarkt
Verkoop Renault daalt in verzwakkende automarkt Vrouwen in gesimuleerde ruimtemissies demonstreren duurzamer leiderschap
Vrouwen in gesimuleerde ruimtemissies demonstreren duurzamer leiderschap Waarom deze plantenetende dinosaurus bloeide en zijn tijdperk domineerde
Waarom deze plantenetende dinosaurus bloeide en zijn tijdperk domineerde  Is de som van alle energiemoleculen een object dat object temperatuur wordt genoemd?
Is de som van alle energiemoleculen een object dat object temperatuur wordt genoemd?  Welke wetenschapper beschreef alle stralende energie als zich gedragen als een stroom deeltjes?
Welke wetenschapper beschreef alle stralende energie als zich gedragen als een stroom deeltjes?  Wat zijn de prominenten van de zon?
Wat zijn de prominenten van de zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

