
Wetenschap
Zuurstof versus selenium:verschillen in elektronegativiteit begrijpen
Elektronegativiteit is de neiging van een atoom om elektronen naar zichzelf toe te trekken in een chemische binding. Elektronegativiteit neemt over het algemeen toe naarmate u zich door een periode verplaatst en neemt af naarmate u een groep lager in het periodiek systeem beweegt.
Zuurstof bevindt zich in de tweede periode en groep 16, terwijl Selenium zich in de vierde periode en groep 16 bevindt. Daarom is zuurstof kleiner en heeft het een grotere nucleaire lading, waardoor het elektronegatiever is dan Selenium.
Hier is een vereenvoudigde uitleg:
* Zuurstof is kleiner: De elektronen bevinden zich dichter bij de kern, wat leidt tot een sterkere aantrekkingskracht.
* Zuurstof heeft een hogere effectieve nucleaire lading: Het aantal protonen in de kern is groter dan dat van Selenium, wat leidt tot een sterkere aantrekkingskracht op de elektronen.
Daarom is zuurstof elektronegatiever dan selenium .
 Opinie:Geen poot om op te staan – waarom de VS haar standpunt over herstelbetalingen voor het klimaat moeten heroverwegen
Opinie:Geen poot om op te staan – waarom de VS haar standpunt over herstelbetalingen voor het klimaat moeten heroverwegen  Sentinel-3 vliegt tandem
Sentinel-3 vliegt tandem Mozambique-stad vocht tegen klimaatverandering, maar de cycloon raasde binnen
Mozambique-stad vocht tegen klimaatverandering, maar de cycloon raasde binnen Waarom is ecosysteem moeilijk te definiëren?
Waarom is ecosysteem moeilijk te definiëren?  Onderzoekers vinden onverwachte impact van orkanen op stroomgebied van Puerto Rico
Onderzoekers vinden onverwachte impact van orkanen op stroomgebied van Puerto Rico
Hoofdlijnen
- Hoe zit het met de moderne organismen die Darwin bestudeerde, leidde hem tot idee is afkomst met modificatie?
- Beschrijf waar het menselijke Sry -gen woont en de betekenis ervan?
- Hoeveel DNA -moleculen zitten er in een chromosoom vlak voor mitiose?
- Wetenschappers ontdekken hoe sommige bacteriën antibiotica overleven
- Wat zijn de 3 delen van theorie -evolutie?
- Geef het substraat van enzym maltase?
- MS-onderzoek:Myeline beïnvloedt hoe hersencellen signalen verzenden
- Wat is de hoogste en laagste taxonomische categorie?
- Welke techniek zou een wetenschapper gebruiken om specifieke organel te isoleren?
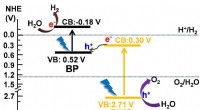
- Ultradunne zwarte fosfor voor door zonne-energie aangedreven waterstofeconomie
- Nieuwe technologie kan helpen water af te stoten, levens redden door verbeterde medische hulpmiddelen

- Convectie versus advectie:inzicht in de verschillende rollen van warmteoverdracht in vloeistoffen

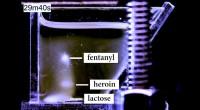
- Nieuwe technologie kan wetshandhavers helpen kleinere hoeveelheden fentanyl met een hogere mate van nauwkeurigheid te detecteren
- De ontwikkeling van laagdimensionale nanomaterialen kan een revolutie teweegbrengen in toekomstige technologieën
 Hoe wordt de energie in ATP gebruikt cel?
Hoe wordt de energie in ATP gebruikt cel?  Wat is een geosymbol?
Wat is een geosymbol?  Een nieuwe geweldige röntgen-'reality'-show debuteert
Een nieuwe geweldige röntgen-'reality'-show debuteert  Wanneer vingertikken op smartphones kunnen leiden tot een zijkanaalaanval
Wanneer vingertikken op smartphones kunnen leiden tot een zijkanaalaanval NASA's Terra-satelliet bespioneert Typhoon Talims groot oog
NASA's Terra-satelliet bespioneert Typhoon Talims groot oog Hoe wordt het genoemd als Moleculen energie gebruikt om over een semipermeabiel membraan te bewegen?
Hoe wordt het genoemd als Moleculen energie gebruikt om over een semipermeabiel membraan te bewegen?  Flexibele maar stevige robot is ontworpen om te groeien als een plant
Flexibele maar stevige robot is ontworpen om te groeien als een plant Welke titel beschrijft het huidige geologische tijdperk het beste?
Welke titel beschrijft het huidige geologische tijdperk het beste?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

