
Wetenschap
Waarom covalente verbindingen geen elektriciteit geleiden (zelfs gesmolten)
* Covalente bindingen: Bij covalente bindingen worden elektronen gedeeld tussen atomen. Deze gedeelde elektronen worden stevig vastgehouden in het molecuul en kunnen niet vrij bewegen.
* Smelten: Het smelten van een covalente verbinding verzwakt de intermoleculaire krachten, waardoor de moleculen vrijer kunnen bewegen. De elektronen in de moleculen blijven echter gebonden en kunnen geen elektrische stroom geleiden.
Contrast met ionverbindingen:
Ionische verbindingen daarentegen zijn goede geleiders van elektriciteit wanneer ze gesmolten zijn. Dit komt omdat:
* Ionische bindingen: Bij ionische bindingen worden elektronen van het ene atoom naar het andere overgebracht, waardoor positieve en negatieve ionen ontstaan.
* Smelten: Wanneer een ionische verbinding smelt, kunnen de ionen vrij bewegen, waardoor ze een elektrische stroom kunnen geleiden.
Voorbeelden:
* Slechte geleiders (covalent): Suiker (sacharose), water (H₂O), methaan (CH₄)
* Goede geleiders (ionisch): Natriumchloride (NaCl), kaliumbromide (KBr), calciumoxide (CaO)
 Is het beste om twee elektronen te verwijderen?
Is het beste om twee elektronen te verwijderen?  Wat vereist meer warmteveranderend water van een vloeistof naar vaste of IT -gas?
Wat vereist meer warmteveranderend water van een vloeistof naar vaste of IT -gas?  Wat is het reactieproduct tussen CuSO4 en KF?
Wat is het reactieproduct tussen CuSO4 en KF?  Welke twee metalen zijn in grote hoeveelheden de binnenste kern te vinden?
Welke twee metalen zijn in grote hoeveelheden de binnenste kern te vinden?  Binaire verbindingen:inzicht in de '-ide'-uitgang en uitzonderingen
Binaire verbindingen:inzicht in de '-ide'-uitgang en uitzonderingen
 EU-hof verwerpt klimaatzaak historische burgers
EU-hof verwerpt klimaatzaak historische burgers Wetenschappers wijzen op Antarctische ijsomwenteling als reactie op prehistorische klimaatverandering
Wetenschappers wijzen op Antarctische ijsomwenteling als reactie op prehistorische klimaatverandering Welk kenmerk van levende wezens wordt niet in alles waargenomen en welk ding toont dit kenmerk?
Welk kenmerk van levende wezens wordt niet in alles waargenomen en welk ding toont dit kenmerk?  Vervuild Libanonmeer spuwt tonnen dode vis uit
Vervuild Libanonmeer spuwt tonnen dode vis uit Delhi wankelt terwijl de zomernevel de Indiase hoofdstad overrompelt
Delhi wankelt terwijl de zomernevel de Indiase hoofdstad overrompelt
Hoofdlijnen
- Hoe verschilt eencellig van multicellular?
- Welke structuur is 5-10 procent van de celcyclus?
- Hoe verschillen sekscellen van gewone cellen?
- Wat is de houder en beschermer van DNA?
- Onderzoekers beschrijven voor het eerst hoe sommige bacteriën mannen doden:ze dringen de moeder binnen
- Het geheim van een lang leven? Vraag een geelbuikmarmot
- Waar kan DNA worden gevonden in plantencellen?
- Wordt flagella gevonden in plantencellen?
- De bananenspin:waarom hij wordt beschouwd als de meest giftige ter wereld
- Een periodiek systeem van moleculaire knopen
- Voedselverspilling omzetten in bioplastics

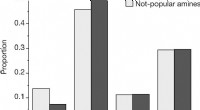
- Chemici laten zien hoe vooringenomenheid kan opduiken in de resultaten van machine learning-algoritmen
- Hoe technologieën voor schoon water een boost kunnen krijgen van röntgensynchrotrons

- Nieuwe materialen voor duurzame, goedkope batterijen

 Astronomen vinden kosmische gouden naald die al twee decennia begraven ligt
Astronomen vinden kosmische gouden naald die al twee decennia begraven ligt Voorstanders waaieren uit in een mondiale steunbetuiging voor de wetenschap
Voorstanders waaieren uit in een mondiale steunbetuiging voor de wetenschap  Trinidad Java en Kyushu zijn voorbeelden van wat voor soort fysiek kenmerk?
Trinidad Java en Kyushu zijn voorbeelden van wat voor soort fysiek kenmerk?  Is een theorie of hypothese?
Is een theorie of hypothese?  Welke functie heeft emb-agar?
Welke functie heeft emb-agar?  Hernieuwbare energiebronnen kunnen de gezondheidseffecten van energieopwekking met 80 procent verminderen
Hernieuwbare energiebronnen kunnen de gezondheidseffecten van energieopwekking met 80 procent verminderen Optimalisatie van de groei van coatings op nanodraadkatalysatoren
Optimalisatie van de groei van coatings op nanodraadkatalysatoren Geheime berichten voor Alexa en Co
Geheime berichten voor Alexa en Co
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

