
Wetenschap
Metaalbinding versus covalente binding:waarom metalen geen gigantische covalente structuren vormen
* Metaalbinding: Metalen vormen metaalbindingen, geen covalente bindingen. Bij metaalbinding is sprake van een ‘zee’ van gedelokaliseerde elektronen die worden gedeeld door alle metaalatomen in de structuur. Deze elektronen kunnen zich vrij door het metaal bewegen, waardoor metalen hun uitstekende geleidbaarheid krijgen.
* Covalente binding: Covalente binding omvat het delen van elektronen tussen atomen om sterke bindingen te vormen. Deze elektronen bevinden zich tussen de atomen en kunnen niet vrij bewegen.
Hier is een overzicht van de eigenschappen van metalen en gigantische covalente structuren:
| Eigendom | Metalen | Gigantische covalente structuren |
|---|---|---|
| Verbindingstype | Metaal | Covalent |
| Elektrische geleidbaarheid | Uitstekend | Slecht (behalve grafiet) |
| Maakbaarheid | Hoog | Over het algemeen broos |
| Ductiliteit | Hoog | Over het algemeen broos |
| Smeltpunt | Over het algemeen hoog | Over het algemeen hoog (behalve grafiet) |
Voorbeelden:
* Metalen: IJzer, koper, goud, natrium
* Gigantische covalente structuren: Diamant, siliciumdioxide (kwarts)
Samengevat: Metalen zijn uitstekende geleiders van elektriciteit vanwege hun metaalbinding, die vrije beweging van elektronen mogelijk maakt. Gigantische covalente structuren hebben daarentegen gelokaliseerde elektronen en zijn over het algemeen slechte geleiders.
 VN-klimaatchef waarschuwt dat huidige pad naar catastrofe leidt
VN-klimaatchef waarschuwt dat huidige pad naar catastrofe leidt Welke man is het meest geassocieerd met naturalisme?
Welke man is het meest geassocieerd met naturalisme?  Smeltende ijsbergen sleutel tot volgorde van een ijstijd, wetenschappers vinden
Smeltende ijsbergen sleutel tot volgorde van een ijstijd, wetenschappers vinden 10 Earth Day-activiteiten om onze planeet te vieren
10 Earth Day-activiteiten om onze planeet te vieren  Synthesepaper onthult sterke en zwakke punten van milieubeloften van bedrijven
Synthesepaper onthult sterke en zwakke punten van milieubeloften van bedrijven
Hoofdlijnen
- Wat zijn de voorbeelden van Mito?
- Hoe kun je zien of het een dierlijke cel of een plantencel is?
- Wat zijn voorbeelden van nucleotide?
- Welke vorm zijn dierencellen?
- Welk organisme is een herbivoor?
- Beschrijft de celcyclus van een eukaryotie de reproductie van geboortegroei en dodencel?
- Analyse van het potentieel van AlphaFold bij het ontdekken van geneesmiddelen
- Wat is de vraag naar een moleculaire bioloog?
- Een cel met talloze ribosomen is waarschijnlijk gespecialiseerd?
- Kalium-aangedreven oplaadbare batterijen:een poging tot een duurzamer milieu

- Natuurkundigen krijgen nieuwe inzichten in nanosystemen met bolvormige opsluiting

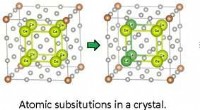
- Het benutten van symmetrieën:de computationele studie van solide oplossingen versnellen
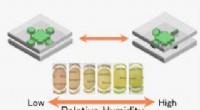
- Functionele films gemaakt van milieuvriendelijke kleimineralen en kleurstoffen
- Hoe enzymen waterstof produceren

 Hoe classificeren wetenschappers virussen?
Hoe classificeren wetenschappers virussen?  Nepbeving:melding van een grote ramp in Californië, een vals alarm
Nepbeving:melding van een grote ramp in Californië, een vals alarm Wat is een voetpad? Een pad waarop mensen kunnen lopen?
Wat is een voetpad? Een pad waarop mensen kunnen lopen?  Hoogleraar mijlpaal in kernfysica probeert het universum zelf te begrijpen
Hoogleraar mijlpaal in kernfysica probeert het universum zelf te begrijpen Afbeelding:geërodeerde lagen in Shalbatana Valles
Afbeelding:geërodeerde lagen in Shalbatana Valles Studie onderzoekt door druk geïnduceerde supergeleidende overgang in elektroden
Studie onderzoekt door druk geïnduceerde supergeleidende overgang in elektroden Wat is een canglomeraat?
Wat is een canglomeraat?  Waar wordt groene steen gewonnen?
Waar wordt groene steen gewonnen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

