
Wetenschap
Heliumverbindingen:onderzoek naar de uitzonderingen op inertheid
Hier is een overzicht:
Waarom helium niet reactief is:
* Edelgasconfiguratie: Helium heeft een volledige buitenste schil van elektronen (2 elektronen in zijn 1s-orbitaal). Dit maakt het zeer stabiel en bestand tegen het verkrijgen of verliezen van elektronen om chemische bindingen te vormen.
* Hoge ionisatie-energie: Het kost veel energie om een elektron uit een heliumatoom te verwijderen, waardoor de deelname aan chemische reacties verder wordt belemmerd.
* Zwakke interatomaire krachten: Heliumatomen hebben slechts een zwakke interactie met elkaar, voornamelijk door van der Waals-krachten. Hierdoor is het zelfs bij zeer lage temperaturen een gas.
Bekende heliumverbindingen:
* Helium-excimeren: Dit zijn kortlevende moleculen in een opgewonden toestand die worden gevormd wanneer heliumatomen worden blootgesteld aan omstandigheden met hoge energie, zoals elektrische ontladingen of laserexcitatie. Voorbeelden hiervan zijn He2* en HeNe*.
* Heliumhydride-ion (HeH+): Dit is de enige bekende stabiele heliumverbinding die onder normale omstandigheden bestaat. Het wordt gevormd in het interstellaire medium en is spectroscopisch waargenomen.
* Heliumclusters: Bij extreem lage temperaturen kunnen heliumatomen zwak met elkaar associëren en clusters vormen. Dit zijn echter geen echte chemische verbindingen in de traditionele zin.
Algemeen:
Hoewel helium inderdaad extreem onreactief is en zeer weinig verbindingen vormt, is het niet helemaal juist om te zeggen dat er geen verbindingen bestaan. Er zijn een handvol bekende uitzonderingen, waaronder excimeren, het heliumhydride-ion en clusters. De overgrote meerderheid van helium blijft echter ongebonden vanwege de unieke elektronische configuratie en hoge stabiliteit.
 Wat is het verschil tussen licht en duisternis?
Wat is het verschil tussen licht en duisternis?  In historisch rood omlijnde buurten is vandaag de dag meer kans op groen
In historisch rood omlijnde buurten is vandaag de dag meer kans op groen Historisch klimaat belangrijk voor bodemreacties op toekomstige klimaatverandering
Historisch klimaat belangrijk voor bodemreacties op toekomstige klimaatverandering Saber-tooth Kittens waren groot uitgebeend
Saber-tooth Kittens waren groot uitgebeend  Te midden van droogte, Colorado-spanten trekken naar oases terwijl ze kunnen
Te midden van droogte, Colorado-spanten trekken naar oases terwijl ze kunnen
Hoofdlijnen
- CRISPR helpt onderzoekers ontdekken hoe koralen zich aanpassen aan de opwarming van de oceanen
- Vraag ons het type bioloog meestal werkt in binnenlaboratoria?
- Wat zijn enkele subvelden van biotechnologie?
- Wat is de functie van een vacoule in plantencel?
- Hoe het epigenetische landschap de binding van pioniertranscriptiefactoren moduleert
- Wat is DNA in de mitochondria?
- Beïnvloedt lichaamsritmes en interageert met de biologische klok?
- Wat zijn de basisparen bij het repliceren van DNA?
- Welk patroon wordt gebruikt in eiwitsynthese?
- Chemische gevarensymbolen begrijpen:OSHA- en NFPA-richtlijnen

- Voedselzekerheid:bestraling en etherische oliedampen voor de behandeling van granen

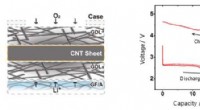
- Ontwikkeling van lithium-luchtbatterijen met ultrahoge capaciteit met behulp van CNT-blad-luchtelektroden
- Eeuwenoud probleem opgelost met allereerste 3D-atomaire beeldvorming van een amorfe vaste stof
- Wetenschappers synthetiseren gipsvervanger

 Napels schrijlings op een rommelende megavulkaan
Napels schrijlings op een rommelende megavulkaan Klimigratie:wanneer gemeenschappen moeten verhuizen vanwege klimaatverandering
Klimigratie:wanneer gemeenschappen moeten verhuizen vanwege klimaatverandering Onderzoekers bieden een unieke manier om de koolstofemissies in waterlichamen te monitoren
Onderzoekers bieden een unieke manier om de koolstofemissies in waterlichamen te monitoren  Hoeveel dagen duurt het voordat de aarde en de maan om de zon draaien?
Hoeveel dagen duurt het voordat de aarde en de maan om de zon draaien?  Waar in de mitochondrion doet elektrontransportketen?
Waar in de mitochondrion doet elektrontransportketen?  Wanneer was de maanlanding van Apollo 11?
Wanneer was de maanlanding van Apollo 11?  De aantrekkingskracht tussen natriumionen en chloorvormen?
De aantrekkingskracht tussen natriumionen en chloorvormen?  Hoe vaak groter is de botsingskracht als de rijsnelheid verdubbeld is?
Hoe vaak groter is de botsingskracht als de rijsnelheid verdubbeld is?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

