
Wetenschap
De aantrekkingskracht tussen natriumionen en chloorvormen?
Dit is waarom:
* natrium (na) is een metaal met één valentie -elektron. Het verliest gemakkelijk dit elektron om een stabiele elektronenconfiguratie te bereiken.
* chloor (Cl) is een niet -metaal met zeven valentie -elektronen. Het krijgt gemakkelijk één elektron om een stabiele elektronenconfiguratie te bereiken.
* Wanneer natrium zijn elektron verliest, wordt het een positief geladen ion (Na+).
* Wanneer chloor een elektron krijgt, wordt het een negatief geladen ion (Cl-).
* De tegenovergestelde ladingen van deze ionen trekken elkaar sterk aan en vormen een ionische binding .
Deze sterke elektrostatische aantrekkingskracht tussen de positieve en negatieve ionen creëert een stabiele kristalroosterstructuur in natriumchloride.
 Welk metaal in de eerste 20 elementen is het meest reactief?
Welk metaal in de eerste 20 elementen is het meest reactief?  Hoeveel atomen zitten er in 1 g waterstofgas?
Hoeveel atomen zitten er in 1 g waterstofgas?  Wat zijn twee manieren om de isotoop van bromide te schrijven die 10 meer neutronen heeft dan het atoomnummer?
Wat zijn twee manieren om de isotoop van bromide te schrijven die 10 meer neutronen heeft dan het atoomnummer?  Wat gebeurt er als ammoniumdichromaat sterk wordt verwarmd?
Wat gebeurt er als ammoniumdichromaat sterk wordt verwarmd?  Wat is het kookpunt van isopropylalcohol wanneer de externe druk toenam. naar standaard druk?
Wat is het kookpunt van isopropylalcohol wanneer de externe druk toenam. naar standaard druk?
 Welke belangrijke attitudes bezitten een succesvolle wetenschapper?
Welke belangrijke attitudes bezitten een succesvolle wetenschapper?  Quinoa is een baken van hoop voor de Andesgemeenschappen in een tijd van wereldwijde crisis
Quinoa is een baken van hoop voor de Andesgemeenschappen in een tijd van wereldwijde crisis De grote verscheidenheid aan planten en dieren?
De grote verscheidenheid aan planten en dieren?  Robots om olievlekken en algenbloei op te sporen in het met ijs bedekte Noordpoolgebied
Robots om olievlekken en algenbloei op te sporen in het met ijs bedekte Noordpoolgebied Bolivia:bijdrage van inheemse volkeren aan de strijd tegen klimaatverandering hangt aan een zijden draadje
Bolivia:bijdrage van inheemse volkeren aan de strijd tegen klimaatverandering hangt aan een zijden draadje
Hoofdlijnen
- Hoe kan obesitas genetisch zijn?
- Wat is het verschil tussen erfelijke en milieudefecten?
- Wat is intracellulair systeem?
- Hoe muizen de beste vluchtroute kiezen
- Wat is de wetenschappelijke naam voor een shag met blauwe ogen?
- Heeft Facebook een generatie ‘in zichzelf gekeerde spindoctors’ gecreëerd?
- Waar bevinden zich lipiden in het lichaam?
- Hoe een tRNA-reeks te krijgen van een DNA-reeks
- Welke processen worden het meest geholpen door de aanwezigheid van bacteriën in het menselijk lichaam?
- Een gepatenteerde oplossing voor het verlichten van droge mond en de ontwikkeling van voedingsproducten
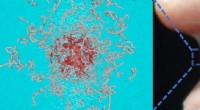
- Gevriesdroogde aardbeien en ijs zorgen voor een zeer stabiele relatie

- Virushydrofobiciteit kan helpen bij het zuiveren van vaccins
- Het begin van een revolutie in verpakkingen

- Flow chemie techniek biedt snellere, veiligere manier om te screenen, bestuderen en optimaliseren van industriële chemische reacties

 Palestijnse boeren profiteren van het watertechnologieproject in Birmingham
Palestijnse boeren profiteren van het watertechnologieproject in Birmingham Sleutel tot koolstofvrije auto's? Kijk naar de sterren
Sleutel tot koolstofvrije auto's? Kijk naar de sterren In welk land zien mensen altijd de zon in de zuidelijke hemel?
In welk land zien mensen altijd de zon in de zuidelijke hemel?  Hoe heet de grond in een bos?
Hoe heet de grond in een bos?  Studie onthult twee schrijvers die historische inscripties hebben geschreven in Samaria uit de achtste eeuw v.Chr
Studie onthult twee schrijvers die historische inscripties hebben geschreven in Samaria uit de achtste eeuw v.Chr De zee met de lucht verbinden in het hoge Noordpoolgebied
De zee met de lucht verbinden in het hoge Noordpoolgebied Wat doet astriods en?
Wat doet astriods en?  De SI -eenheid die u zou gebruiken om de breedte van uw klaslokaal te meten?
De SI -eenheid die u zou gebruiken om de breedte van uw klaslokaal te meten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

