
Wetenschap
Waterstof versus helium:molaire massa en atoomgewicht begrijpen
* Atomen versus mollen: Een mol is een meeteenheid die een specifiek aantal deeltjes vertegenwoordigt (6,022 x 10^23 deeltjes, ook bekend als het getal van Avogadro). Dus 1 mol waterstofatomen bevat 6,022 x 10^23 waterstofatomen.
* Atoommassa: Waterstof en helium hebben verschillende atoommassa's. Waterstof heeft een atoommassa van ongeveer 1 atomaire massa-eenheid (amu), terwijl helium een atoommassa heeft van ongeveer 4 amu. Dit betekent dat een heliumatoom ongeveer vier keer zwaarder is dan een waterstofatoom.
Daarom:
* 1 mol waterstofatomen weegt 1 gram.
* 1 mol heliumatomen weegt 4 gram.
Hoewel ze hetzelfde aantal deeltjes bevatten (6,022 x 10^23), zullen de twee monsters verschillende massa's hebben omdat de individuele atomen verschillende massa's hebben.
 Vloeistoffen die geen vorm in lagen mengen wanneer ze verschillende dichtheden waar of onwaar hebben?
Vloeistoffen die geen vorm in lagen mengen wanneer ze verschillende dichtheden waar of onwaar hebben?  Hoe wordt zuiver cesium opgeslagen?
Hoe wordt zuiver cesium opgeslagen?  Welke vormen rond condensatie -kernen?
Welke vormen rond condensatie -kernen?  Wanneer verzadigde oplossingen worden ze meestal onverzadigd geraakt?
Wanneer verzadigde oplossingen worden ze meestal onverzadigd geraakt?  Wetenschappers berekenen stralingsdosis in botresten van slachtoffer bomaanslag Hiroshima
Wetenschappers berekenen stralingsdosis in botresten van slachtoffer bomaanslag Hiroshima
 Het perfecte getij nabootsen om wetlands aan de kust te beschermen tegen stijgende zeespiegels
Het perfecte getij nabootsen om wetlands aan de kust te beschermen tegen stijgende zeespiegels Vulkaanuitbarsting, resulterende chaos doden minstens 15 in Congo
Vulkaanuitbarsting, resulterende chaos doden minstens 15 in Congo Welk ecosysteem komt voor op 30 graden noord- en zuiden?
Welk ecosysteem komt voor op 30 graden noord- en zuiden?  Overstromingen in China om de Amerikaanse economie te treffen - klimaateffecten via handelsketens
Overstromingen in China om de Amerikaanse economie te treffen - klimaateffecten via handelsketens Afwatering van veengebieden in Zuidoost-Azië draagt bij aan klimaatverandering
Afwatering van veengebieden in Zuidoost-Azië draagt bij aan klimaatverandering
Hoofdlijnen
- Wetenschappers vinden potentiële wapens voor de strijd tegen antibioticaresistentie
- UA maakt deel uit van een groep die ontrafelt hoe de hersenen het geheugen beheren
- Welke fase van mitose scheiden de gerepliceerde chromosomen?
- Wat is belangrijk aan een ribosoom in de dierencel?
- Welke celstructuren worden alleen aangetroffen in eukaryotische cel?
- Glucose begrijpen:een enkel suikermolecuul
- Biochemici gaan onderzoeken hoe gewassen de eiwitproductie kunnen verhogen
- Wat gebruiken bacteriën voor beweging?
- Wat voor soort overerving wanneer het genotype noch homozygoot of heterozygoot is?
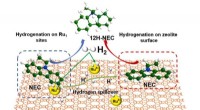
- Synergistische katalysatoren voor zeer efficiënte waterstofopslag
- Onschadelijke elementen kunnen giftig lood in elektronica vervangen

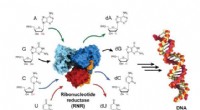
- Biochemici vangen en visualiseren een enzym wanneer het actief wordt
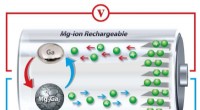
- Zelfherstellende vloeistof brengt nieuw leven in batterijalternatief
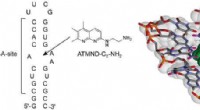
- Het strakste niet-aminoglycoside-ligand voor de bacteriële ribosomale RNA A-site
 Nieuwe aanpak maakt het gemakkelijker om nieuwe medicijnen te vinden
Nieuwe aanpak maakt het gemakkelijker om nieuwe medicijnen te vinden Invloed van ouders op opleidingsniveau veel groter dan eerder werd gedacht, nieuwe onderzoeksresultaten
Invloed van ouders op opleidingsniveau veel groter dan eerder werd gedacht, nieuwe onderzoeksresultaten FTC:Website voor consumentenfinanciering gaf de voorkeur aan bedrijven die betaalden
FTC:Website voor consumentenfinanciering gaf de voorkeur aan bedrijven die betaalden Hoe scheid je loodsulfaat en chloride?
Hoe scheid je loodsulfaat en chloride?  Warmteverlies voorkomen door straling en geleiding?
Warmteverlies voorkomen door straling en geleiding?  Effecten van een tsunami op het mariene ecosysteem
Effecten van een tsunami op het mariene ecosysteem  Wat is de functie van natriumcarbonaatoplossing in ethylacetaatexperiment?
Wat is de functie van natriumcarbonaatoplossing in ethylacetaatexperiment?  Waarom werd Pluto gediskwalificeerd als een planeet?
Waarom werd Pluto gediskwalificeerd als een planeet?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

