
Wetenschap
Waarom is de thermische geleidbaarheid van een vloeistof groter dan gas?
1. Hogere dichtheid: Vloeistoffen hebben veel hogere dichtheden dan gassen. Dit betekent dat moleculen veel dichter bij elkaar zijn verpakt in een vloeistof, wat leidt tot frequentere botsingen en energieoverdracht.
2. Sterkere intermoleculaire krachten: Vloeistoffen ervaren sterkere intermoleculaire krachten (bijvoorbeeld waterstofbinding, dipool-dipoolinteracties) in vergelijking met gassen. Deze krachten houden de moleculen dichter bij elkaar en vergemakkelijken de overdracht van warmte door trillingen en moleculaire botsingen.
3. Frequentere botsingen: De verhoogde dichtheid en sterkere interacties resulteren in frequentere botsingen tussen vloeibare moleculen. Dit leidt tot efficiëntere energieoverdracht, wat bijdraagt aan een hogere thermische geleidbaarheid.
4. Geleiding en convectie: Vloeistoffen kunnen warmte overdragen door zowel geleiding (directe energieoverdracht door botsingen) en convectie (massabeweging van verwarmde vloeistof). Gassen zijn voornamelijk afhankelijk van geleiding, wat minder efficiënt is vanwege de grotere afstand tussen moleculen.
5. Lager gemiddelde gratis pad: Het gemiddelde vrije pad (gemiddelde afstand die een molecuul reist voordat ze botsen) is veel kleiner in vloeistoffen dan in gassen. Dit kortere pad betekent dat energieoverdracht sneller en efficiënter plaatsvindt.
Het is belangrijk op te merken dat:
* Uitzonderingen bestaan: Er zijn enkele vloeistoffen met een lagere thermische geleidbaarheid dan bepaalde gassen. Kwik heeft bijvoorbeeld een hogere thermische geleidbaarheid dan lucht, maar lager dan sommige andere gassen zoals waterstof.
* Temperatuur en druk: De thermische geleidbaarheid van zowel vloeistoffen als gassen wordt beïnvloed door temperatuur en druk. Over het algemeen neemt de thermische geleidbaarheid toe met temperatuur en druk.
Samenvattend, de hogere dichtheid, sterkere intermoleculaire krachten en frequentere botsingen in vloeistoffen leiden tot een hogere snelheid van energieoverdracht en dus een hogere thermische geleidbaarheid in vergelijking met gassen.
 Wat is het verschil tussen organisch materiaal waaruit steenkool ontstaat en aardolie-aardgasvormen?
Wat is het verschil tussen organisch materiaal waaruit steenkool ontstaat en aardolie-aardgasvormen?  Welke aminozuren in schelpen ons kunnen vertellen over mensen uit de Bronstijd
Welke aminozuren in schelpen ons kunnen vertellen over mensen uit de Bronstijd  Wat heeft meer massa dan een potlood?
Wat heeft meer massa dan een potlood?  Hoeveel liter van een 10 procent ammoniakoplossing moet worden gemengd met 50 30 om een 15-oplossing te maken?
Hoeveel liter van een 10 procent ammoniakoplossing moet worden gemengd met 50 30 om een 15-oplossing te maken?  Nieuwe verbindingen uit de zeester van het Kuril-bekken tonen werkzaamheid tegen kankercellen.
Nieuwe verbindingen uit de zeester van het Kuril-bekken tonen werkzaamheid tegen kankercellen.
Hoofdlijnen
- Wat is de naam van cellen die insuline produceert?
- Kuifduiven gebruiken veren om alarm te slaan
- Is het verschil tussen glycogeen en zetmeel?
- Welke bloedcel helpt om bacteriën te bestrijden?
- Wat betekent anaërobe metabolisme?
- DNA-onderzoek in de Stille Oceaan onthult een toename van 2000 procent in onze kennis van de biodiversiteit van weekdieren
- Maak kennis met Cheddar Man:Your New Stone Age Crush
- Wat is selectie in de wetenschap?
- Wat zijn Canela -planten?
- NIST-software helpt bij de analyse van geïnstrumenteerde charpy-tests
- Een gevierde AI heeft een nieuwe truc geleerd:scheikunde doen
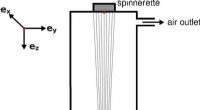
- Simuleren en optimaliseren van industriële spinprocessen
- Nieuwe biomaterialen kunnen worden verfijnd voor medische toepassingen

- Kooldioxidemineralisatie in geologisch veel voorkomende gesteenten voor koolstofopslag

 Hoe 'Pokemon Go' van grap naar fenomeen ging
Hoe 'Pokemon Go' van grap naar fenomeen ging  Nanobellen-gecontroleerd nanofluïdisch transport
Nanobellen-gecontroleerd nanofluïdisch transport Wat beschrijft energieoverdracht het beste in een gesloten systeem?
Wat beschrijft energieoverdracht het beste in een gesloten systeem?  Is een nikkel pure substantie?
Is een nikkel pure substantie?  Recycle anesthetica om de CO2-uitstoot van de gezondheidszorg te verminderen, studie concludeert
Recycle anesthetica om de CO2-uitstoot van de gezondheidszorg te verminderen, studie concludeert Werken alle cellen precies hetzelfde?
Werken alle cellen precies hetzelfde?  Hoge inkomens hebben steviger vangnet na baanverlies
Hoge inkomens hebben steviger vangnet na baanverlies Stuiteren poreuze materialen geluidsgolven rond?
Stuiteren poreuze materialen geluidsgolven rond?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

