
Wetenschap
Kan chloride in kaliumgas af en verdampen als chloor?
Dit is waarom:
* chemische binding: Kaliumchloride (KCL) is een ionische verbinding. Dit betekent dat het bestaat als een kristalrooster met sterke elektrostatische attracties tussen positief geladen kaliumionen (k+) en negatief geladen chloride-ionen (Cl-). Chloorgas (CL2) is daarentegen een covalent molecuul met een gedeeld elektronenparen tussen twee chlooratomen.
* Verdamping versus sublimatie: Chloorgas kan verdampen vanuit een vloeibare toestand en rechtstreeks in een gasfase overstappen. Kaliumchloride is echter een vaste stof bij kamertemperatuur. Om een gas te worden, zou het sublimatie moeten ondergaan - een directe overgang van vast naar gas.
* Hoge sublimatietemperatuur: Kaliumchloride heeft een zeer hoge sublimatietemperatuur (ongeveer 1415 ° C of 2581 ° F). Dit betekent dat het veel energie vereist om de sterke ionische bindingen en overgang in een gasvormige toestand te doorbreken.
* Ontleding: Als u kaliumchloride zou verwarmen tot extreem hoge temperaturen, zou dit waarschijnlijk ontleden voordat het sublimeert. Dit betekent dat de verbinding zou afbreken in zijn samenstellende elementen, kalium (K) en chloor (CL), in plaats van kaliumchloridegas te vormen.
Samenvattend: Terwijl chloorgas kan verdampen, verdampt kaliumchloride niet als chloor. Het heeft een zeer hoge sublimatietemperatuur en zou waarschijnlijk ontleden voordat het in een gasvormige toestand zou kunnen overgaan.
 Deze mijn in Alaska zou $1 miljard per jaar kunnen genereren. Is het het risico voor zalm waard?
Deze mijn in Alaska zou $1 miljard per jaar kunnen genereren. Is het het risico voor zalm waard?  Top 5 manieren om de planeet te redden met fietsen
Top 5 manieren om de planeet te redden met fietsen  Nieuwe studie bevestigt omvangrijke gaslekken in de Noordzee
Nieuwe studie bevestigt omvangrijke gaslekken in de Noordzee Onderzoek toont aan dat het kooldioxidegehalte wordt beïnvloed door aardbevingen
Onderzoek toont aan dat het kooldioxidegehalte wordt beïnvloed door aardbevingen VN-rapport om dringende behoefte aan natuurreddingsplan te benadrukken
VN-rapport om dringende behoefte aan natuurreddingsplan te benadrukken
Hoofdlijnen
- Somatische en genetische schade veroorzaakt door straling
- De herfst is de beste tijd om nestkasten voor kerkuilen schoon te maken
- Wrens-oproepen onthullen subtiele verschillen tussen ondersoorten
- Wat hebben variabelen en onafhankelijk gemeen?
- Welke organel als leeg zou de plant ertoe leiden dat?
- Wat een organisme ziet eruit als gevolg van zijn genen?
- Wat zijn het 3 -deel van een cel?
- Hoe wordt een karyotype gemaakt?
- In welk cel organelpolymorfisme wordt gevonden?
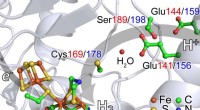
- Nieuwe röntgenspectroscopie onderzoekt waterstofgenererende katalysator
- Nieuwe theorie gaat in op hoe het leven op aarde is ontstaan uit de oorspronkelijke modder

- Zullen sterke en snel wisselende kunstmatige spieren haalbaar zijn?
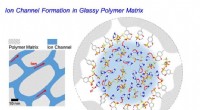
- Ontwikkeling van betere fabricagetechnieken voor pH-responsieve microcapsules

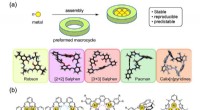
- Metaalcomplexen gemaakt van cyclische moleculen
 Hoeveel elektronen zijn er in het hoogst bezette energieniveau van een neutraal chlooratoom?
Hoeveel elektronen zijn er in het hoogst bezette energieniveau van een neutraal chlooratoom?  Waarom social distancing een grote uitdaging is in veel Afrikaanse landen
Waarom social distancing een grote uitdaging is in veel Afrikaanse landen Wat is de algehele volgorde van reactie?
Wat is de algehele volgorde van reactie?  Hoe de visserij zeehonden en zeeleeuwen in Zuid-Amerika bedreigt
Hoe de visserij zeehonden en zeeleeuwen in Zuid-Amerika bedreigt  Verbindingen die helpen om te voorkomen dat de pH van een oplossing een grote deal wordt genoemd, worden hoe genoemd?
Verbindingen die helpen om te voorkomen dat de pH van een oplossing een grote deal wordt genoemd, worden hoe genoemd?  Is energie nodig voor celbeweging?
Is energie nodig voor celbeweging?  Het vijfde kwartet:opgewonden ontdekking van neon kan sterkwaliteiten onthullen
Het vijfde kwartet:opgewonden ontdekking van neon kan sterkwaliteiten onthullen Veldspaat mengen met water en het produceren van kleipineralen is mechanisch of chemisch?
Veldspaat mengen met water en het produceren van kleipineralen is mechanisch of chemisch?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

