
Wetenschap
Verbindingen die helpen om te voorkomen dat de pH van een oplossing een grote deal wordt genoemd, worden hoe genoemd?
Dit is waarom:
* buffers weerstaan veranderingen in pH: Ze doen dit door te reageren met zowel zuren als basen, ze te neutraliseren en grote verschuivingen in de concentratie waterstofionen te voorkomen ([H+]).
* Hoe ze werken: Een buffersysteem bestaat meestal uit een zwak zuur en de conjugaatbasis (of een zwakke basis en het conjugaatzuur). Wanneer een zuur wordt toegevoegd, neutraliseert de basiscomponent van de buffer het. Wanneer een basis wordt toegevoegd, neutraliseert de zuurcomponent deze.
Voorbeeld:
Een gemeenschappelijk buffersysteem is koolzuur (H2CO3) en bicarbonaat (HCO3-) in ons bloed. Dit systeem helpt de pH van het bloed binnen een smal bereik te behouden, essentieel voor de juiste lichaamsfunctie.
 Wat maakt de naturalistische seculiere humanistische en atheïstische existesialistische?
Wat maakt de naturalistische seculiere humanistische en atheïstische existesialistische?  Intrusies van de Golfstroom voeden hotspots van diatomeeën
Intrusies van de Golfstroom voeden hotspots van diatomeeën Verlies van Arctisch zee-ijs leidt tot frequentere sterke El Niño-gebeurtenissen
Verlies van Arctisch zee-ijs leidt tot frequentere sterke El Niño-gebeurtenissen Verloren nanoplastic uit de oceaan kan vast komen te zitten aan kusten
Verloren nanoplastic uit de oceaan kan vast komen te zitten aan kusten Duurzaamheid definiëren en meten
Duurzaamheid definiëren en meten
Hoofdlijnen
- Onderzoek naar genexpressie in gewone blauwgroene algen onthult wat deze giftig maakt
- De eerste gekweekte Chesapeake-zalm versus de laatste steur? Voorgestelde viskwekerij aan de oostkust wekt bezorgdheid op
- Reproduceert Plant hun eigen soort?
- Wat is de voormanen ovale en ductus venosus?
- Wat zijn de 5Kingdoms die u gebruikt om organismen te classificeren?
- Hoe wetenschap het voedsel dat je eet en koopt?
- Welke dieren verspreiden zaden?
- Wat is een koolhydraat gevonden in een celwand van plantencellen?
- Wat zijn de functies van organen in een cel?
- Van nata de coco tot computerschermen:Cellulose krijgt een kans om te schitteren
- Nieuwe katalysator overtreft platina voor de productie van waterstof

- Onderzoek toont aan dat de oxidatietoestand van zink kan worden gemaakt +3, de elementenchemie fundamenteel veranderen

- Vastleggen van het gedrag van katalysatoren met één atoom onderweg

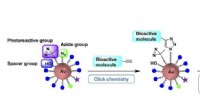
- Eenvoudig te monteren steigers van gouden nanodeeltjes dienen als moleculaire sonde
 Hoe wordt de oplosbaarheid van gassen in vloeistoffen beïnvloed door temperatuurveranderingen?
Hoe wordt de oplosbaarheid van gassen in vloeistoffen beïnvloed door temperatuurveranderingen?  Modellen tonen aan dat koralen beter bestand zijn tegen de opwarming van de oceaan als ze ruilen voor hittebestendige algenvariëteiten
Modellen tonen aan dat koralen beter bestand zijn tegen de opwarming van de oceaan als ze ruilen voor hittebestendige algenvariëteiten  Kinderexperts dienen FTC-klacht in tegen Facebook kids app
Kinderexperts dienen FTC-klacht in tegen Facebook kids app Wat is het smeltpunt van de zoutoplossing?
Wat is het smeltpunt van de zoutoplossing?  Preview:Marvel Powers United VR laat spelers de superhelden zijn
Preview:Marvel Powers United VR laat spelers de superhelden zijn Wat zijn de functies van erfelijk materiaal?
Wat zijn de functies van erfelijk materiaal?  Wat bevat 2 chromatiden bij elkaar?
Wat bevat 2 chromatiden bij elkaar?  Wat betekent rotscompositie?
Wat betekent rotscompositie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

