
Wetenschap
Hoeveel waterstofatomen zijn aanwezig in 75.0 van G H2O?
1. Vind de molaire watermassa (H₂o):
* Waterstof (H) heeft een molaire massa van 1,01 g/mol
* Zuurstof (O) heeft een molaire massa van 16,00 g/mol
* Molaire massa van H₂o =(2 * 1.01 g/mol) + 16,00 g/mol =18,02 g/mol
2. Bereken het aantal mol water:
* Mol =massa / molaire massa
* Mol =75,0 g / 18,02 g / mol =4.16 mol H₂o
3. Bepaal het aantal mol waterstofatomen:
* Elk watermolecuul (H₂O) bevat 2 waterstofatomen.
* Mol waterstofatomen =4,16 mol H₂o * (2 mol H / 1 mol H₂o) =8,32 mol H
4. Converteer mol waterstofatomen in het aantal atomen:
* Het nummer van Avogadro vertelt ons dat er 6.022 x 10²³ atomen in één mol zijn.
* Aantal waterstofatomen =8,32 mol H * (6.022 x 10²³ atomen/mol) = 5,01 x 10²⁴ Waterstofatomen
Daarom zijn er ongeveer 5,01 x 10²⁴ waterstofatomen aanwezig in 75,0 g H₂o.
 Waarom koralen niet altijd symbionten doorgeven aan hun nakomelingen
Waarom koralen niet altijd symbionten doorgeven aan hun nakomelingen De economie van klimaatverandering zal de armoede in de wereld beïnvloeden, deskundige zegt:
De economie van klimaatverandering zal de armoede in de wereld beïnvloeden, deskundige zegt: Wil je weten wat oude koala's aten? Controleer de tanden van moderne koala's
Wil je weten wat oude koala's aten? Controleer de tanden van moderne koala's  Wat kunnen oceanen vormen als de atmosfeer verandert?
Wat kunnen oceanen vormen als de atmosfeer verandert?  Canada, Amerikaanse hittegolf op steroïden door klimaatverandering, zeggen experts
Canada, Amerikaanse hittegolf op steroïden door klimaatverandering, zeggen experts
Hoofdlijnen
- Celcontractie drijft de initiële vorming van menselijke embryo's aan, zo blijkt uit onderzoek
- Dit is wat u moet weten over de Varroamijt
- Beschrijf de functies van celdeling in zowel eencellige als meercellige organismen?
- Wat zijn de relevantie van de wetenschap voor de samenleving?
- Wat kan het effect zijn van het erven van meer dan normaal aantal chromosomen bij een mens?
- Zooplankton Vs. fytoplankton
- Techniek op de plaats delict die wordt gebruikt om schildpadden te volgen
- Hoe kan het leven anders zijn als cellen actief transport moesten gebruiken, elke stof verplaatsen?
- Wat is een voorbeeld van een embryonale plant?
- Halfgeleiderchip die uitgeademd gas met hoge gevoeligheid bij kamertemperatuur detecteert

- Ontdek de sleutel tot veiligere apparaten voor energieopslag die oververhitting voorkomen

- Hydrogel geneest zonder toevoegingen
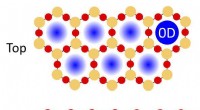
- Het bedekken van metalen katalysatoroppervlakken met dunne tweedimensionale oxidematerialen kan chemische reacties versterken
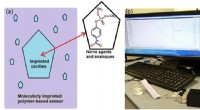
- Snelle detectie van toxische verbindingen
 Wereldwijde gletsjersmelt verhoogt de zeespiegel en put een ooit betrouwbare waterbron uit
Wereldwijde gletsjersmelt verhoogt de zeespiegel en put een ooit betrouwbare waterbron uit Belang van Hydrogen
Belang van Hydrogen Natuurkundigen leggen uit hoe het type aurora op Mars wordt gevormd
Natuurkundigen leggen uit hoe het type aurora op Mars wordt gevormd  Twitter lijkt terug te zijn na storing
Twitter lijkt terug te zijn na storing Waarom blijft het Dirty Dancing Lake leeglopen?
Waarom blijft het Dirty Dancing Lake leeglopen?  Wat is de oorspronkelijke energiebron in olie?
Wat is de oorspronkelijke energiebron in olie?  Wat zal er in de toekomst gebeuren met baobabbomen in Madagaskar?
Wat zal er in de toekomst gebeuren met baobabbomen in Madagaskar?  Waarom moet water behoud nodig hebben, hoewel grote oceanen worden omgeven door landmassa?
Waarom moet water behoud nodig hebben, hoewel grote oceanen worden omgeven door landmassa?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

