
Wetenschap
Wat is de pH -waarde van ammoniumhydroxide -oplossing?
Dit is waarom:
* Zwakke basis: Ammoniumhydroxide (NH₄OH) ioniseert niet volledig in water, wat betekent dat het niet al zijn hydroxide -ionen vrijgeeft (OH⁻). Dit is anders dan sterke bases zoals natriumhydroxide (NaOH), die volledig ioniseren.
* evenwicht: De ionisatie van ammoniumhydroxide is een evenwichtsreactie:
NH₄OH (aq) ⇌ nH₄⁺ (aq) + oh⁻ (aq)
* concentratie: De concentratie van hydroxide -ionen (OH⁻) in oplossing bepaalt de pH. Een hogere concentratie hydroxide -ionen resulteert in een hogere pH (meer basic).
Om de exacte pH te bepalen, moet u de concentratie van de ammoniumhydroxide -oplossing kennen en de evenwichtsconstante (KB) gebruiken voor zijn ionisatie.
Laat het me weten als je de concentratie hebt en de pH wilt berekenen.
 Hoe belangrijk is geografische isolatie bij soortvorming?
Hoe belangrijk is geografische isolatie bij soortvorming?  Cyclone Feiten voor kinderen
Cyclone Feiten voor kinderen China zegt geen mijnbouw in zijn onmiddellijke plannen voor Antarctica (update)
China zegt geen mijnbouw in zijn onmiddellijke plannen voor Antarctica (update) Hergebruik van servies kan verspilling door online voedselbezorging verminderen
Hergebruik van servies kan verspilling door online voedselbezorging verminderen Anemonen nemen de hitte met een beetje hulp van hun vrienden
Anemonen nemen de hitte met een beetje hulp van hun vrienden
Hoofdlijnen
- Studie:Hoe een unieke familie bacteriën zich verbergt voor het immuunsysteem
- Wat is de meest dodelijke ziekteverwekker?
- Waarom begon Mendel zijn experimenten door eren te laten pollineren voor meerdere generaties?
- Wat zijn de meest levende organismen op aarde die vandaag zijn geclassificeerd?
- Hoe vormen zich tetraploïden en aneuploïden?
- Studie:Hoe roodrot suikerriet aantast
- Tonen dieren bewustzijn? | Hoe dingen werken
- Waarom sommige vuurvliegjes femme fatales worden in hun race om te overleven
- Hoe telomeren werken
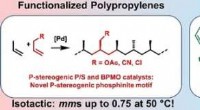
- Katalysatoren voor isotactische polaire polypropylenen
- Een concrete stap in de richting van nul CO2-uitstoot bij de cementproductie

- De frontlinieverdediging van het immuunsysteem bevriest bacteriën in hun sporen

- Met de steigermethode kunnen biochemici eiwitten in opmerkelijk detail zien

- Video:Wordt het kombucha?

 Is kwik een metaal of metalloïde?
Is kwik een metaal of metalloïde?  Wat moet je weten om molariteit te berekenen?
Wat moet je weten om molariteit te berekenen?  Hoe aardbevingen werken
Hoe aardbevingen werken  Studie identificeert knelpunten in vroege zeegrasgroei
Studie identificeert knelpunten in vroege zeegrasgroei Hoe dieren genen hergebruiken om beide ledematen en ogen te ontwikkelen
Hoe dieren genen hergebruiken om beide ledematen en ogen te ontwikkelen Startup bevordert koolstofvrije brandstoffen via UConn-partnerschap
Startup bevordert koolstofvrije brandstoffen via UConn-partnerschap Wat zijn de gevaren van elektromagneten?
Wat zijn de gevaren van elektromagneten?  Welk deel van het menselijk lichaam heeft functie mitochondria?
Welk deel van het menselijk lichaam heeft functie mitochondria?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

