
Wetenschap
Wat zijn zouten van oxo-zuren?
Hier is een uitsplitsing:
* Oxo-zuren: Dit zijn zuren die zuurstof, waterstof en ten minste één ander element bevatten. De zure waterstof is altijd gebonden aan een zuurstofatoom. Voorbeelden zijn zwavelzuur (H₂so₄), salpeterzuur (HNO₃) en fosforzuur (H₃PO₄).
* zoutvorming: Wanneer een oxo-zuur reageert met een basis (meestal een metaalhydroxide of een metaaloxide), worden de waterstofionen (H+) van het zuur vervangen door het metaalkation of een positief geladen polyatomisch ion. Dit resulteert in de vorming van zout en water.
Hier is een voorbeeld:
Reactie van zwavelzuur (H₂so₄) met natriumhydroxide (NaOH):
H₂so₄ (aq) + 2naOH (aq) → na₂so₄ (aq) + 2h₂o (l)
* Zwavelzuur (H₂so₄) is een oxo-zuur.
* Natriumhydroxide (NaOH) is een basis.
* Natriumsulfaat (Na₂so₄) is het gevormde zout.
Key-kenmerken van zouten van oxo-zuren:
* ionische aard: Deze zouten zijn ionische verbindingen, wat betekent dat ze zijn samengesteld uit positief geladen kationen en negatief geladen anionen.
* Anionisch component: Het anion van het zout wordt afgeleid van de oxo-zuur door de waterstofionen (H+) te verwijderen en een negatieve lading toe te voegen voor elke verwijderde waterstof. Het sulfaatanion (SO₄²⁻) wordt bijvoorbeeld gevormd uit zwavelzuur (H₂so₄) door twee waterstofionen te verwijderen.
* naamgeving: Zouten van oxo-zuren worden typisch genoemd door het "-ic" of "-bezit" achtervoegsel van het zuur te vervangen door respectievelijk "-ate" of "-ite". Bijvoorbeeld, zwavelzuur (h₂so₄) vormt sulfaten, terwijl zwavelzuur (h₂so₃) sulfieten vormt.
Voorbeelden van zouten van oxo-zuren:
* Natriumchloride (NaCl) - gevormd uit zoutzuur (HCl)
* Kaliumnitraat (kno₃) - gevormd uit salpeterzuur (hno₃)
* Calciumcarbonaat (caco₃) - gevormd uit koolzuur (H₂co₃)
* Ammoniumfosfaat ((NH₄) ₃po₄) - gevormd uit fosforzuur (H₃po₄)
Het begrijpen van zouten van oxo-zuren is cruciaal voor het begrijpen van chemische reacties en nomenclatuur in anorganische chemie.
 Wat gebeurt er als je Clorox mengt met zout?
Wat gebeurt er als je Clorox mengt met zout?  Moleculen die dienen als chemicaliën om reacties te laten werken, zoals de afbraak van voedselmoleculen?
Moleculen die dienen als chemicaliën om reacties te laten werken, zoals de afbraak van voedselmoleculen?  Wat bevat grotere OH-ionen, een zuur of een base?
Wat bevat grotere OH-ionen, een zuur of een base?  Op weg naar platina:een niet-giftige katalysator voor schoon, herbruikbaar water
Op weg naar platina:een niet-giftige katalysator voor schoon, herbruikbaar water Wat gebeurt er PO43- reactswith Water?
Wat gebeurt er PO43- reactswith Water?
 Wat in de aarde?
Wat in de aarde?  San Diego lanceert campagne om stad weerbaarder te maken tegen klimaatverandering
San Diego lanceert campagne om stad weerbaarder te maken tegen klimaatverandering Betrokkenheid van lokale belanghebbenden essentieel voor inzicht in het beschermingsniveau van beschermde mariene gebieden
Betrokkenheid van lokale belanghebbenden essentieel voor inzicht in het beschermingsniveau van beschermde mariene gebieden Een nadere blik op de creatie van een metamorfe zool
Een nadere blik op de creatie van een metamorfe zool Over een groot deel van de planeet warmen nachten sneller op dan dagen
Over een groot deel van de planeet warmen nachten sneller op dan dagen
Hoofdlijnen
- Hoe kleine watermonsters echt grote dieren kunnen vinden
- Wat wordt het proces dat wordt genoemd door welke wetenschapper controleert of anderen eerder werken in publicatiewetenschappelijke tijdschriften?
- Welke observatie is bewijs dat een eencellulair organisme niet eukaryote?
- Wat is een zin die het woord microbiologie gebruikt?
- Toen Europa werd overspoeld door de oceanen
- Welke moleculen behouden de vorm die nodig is om biologisch actief te zijn vanwege intermoleculaire krachten?
- Onderzoekers onthullen hoe planten zichzelf beschermen tegen virale infecties door deacetylering te reguleren
- Wat zijn de bouwstenen van dit biomolecuul Amylase?
- De effecten van algen in drinkwater
- Chemie en informatica bundelen krachten om kunstmatige intelligentie toe te passen op chemische reacties

- Ontdekking leidt tot nieuwe verouderingscrème en kippenvoer

- Nieuwe methode maakt generieke polymeren lichtgevend
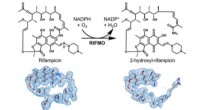
- Onderzoekers ontdekken nieuw mechanisme van antibioticaresistentie bij lepra en tuberculose
- Onderzoekers ontwikkelen ultrasterke aerogels met materialen die worden gebruikt in kogelwerende vesten

 Heeft Sprite er koolstofdioxide in?
Heeft Sprite er koolstofdioxide in?  Een nieuwe manier om medicijnen af te leveren met nauwkeurige targeting
Een nieuwe manier om medicijnen af te leveren met nauwkeurige targeting Wanneer licht een donker voorwerp raakt, wordt het dan geabsorbeerd?
Wanneer licht een donker voorwerp raakt, wordt het dan geabsorbeerd?  Wetenschappers vestigen record voor interactie tussen licht en materie
Wetenschappers vestigen record voor interactie tussen licht en materie Organotinvergiftiging kan zwaarlijvigheid veroorzaken, medici zeggen:
Organotinvergiftiging kan zwaarlijvigheid veroorzaken, medici zeggen: De volgende generatie datacenters binnen handbereik dankzij nieuwe energiezuinige switches
De volgende generatie datacenters binnen handbereik dankzij nieuwe energiezuinige switches Werk je vanuit huis? Stel een tijd in, geen kamer
Werk je vanuit huis? Stel een tijd in, geen kamer  Hoe de gyroscoop werkt
Hoe de gyroscoop werkt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

