
Wetenschap
Wat is de valentie van een monoatomisch chloorion?
De valentie van een monoatomisch chloorion is -1 .
Dit is waarom:
* Chloor's elektronenconfiguratie: Chloor heeft 7 elektronen in zijn buitenste schaal.
* octetregel: Om een stabiele elektronenconfiguratie te bereiken, heeft chloor de neiging om één elektron te krijgen om zijn octet te voltooien (8 elektronen in de buitenste schaal).
* ionenvorming: Wanneer chloor een elektron krijgt, wordt het een negatief geladen ion, met name een chloride -ion (CL⁻). Deze negatieve lading betekent een valentie van -1.
 Wat is chemische verandering voor zuiveringszout?
Wat is chemische verandering voor zuiveringszout?  Hoeveel verschil is er tussen de energie die vrijkomt tijdens chemische reactie en nucleaire reacties?
Hoeveel verschil is er tussen de energie die vrijkomt tijdens chemische reactie en nucleaire reacties?  Hoeveel mol stikstof en waterstof zijn nodig om 10 ammoniak te krijgen?
Hoeveel mol stikstof en waterstof zijn nodig om 10 ammoniak te krijgen?  Onderzoekers hebben een effectieve oplossing gecreëerd voor het opvangen van gemorste aardolie
Onderzoekers hebben een effectieve oplossing gecreëerd voor het opvangen van gemorste aardolie Wat bepaalt of materiaal vast of een gas?
Wat bepaalt of materiaal vast of een gas?
 Vervuilde lucht veroorzaakt vroege sterfgevallen in de op fossiele brandstoffen gestookte Balkan
Vervuilde lucht veroorzaakt vroege sterfgevallen in de op fossiele brandstoffen gestookte Balkan Klein plankton herstelt traag na botsing met asteroïden die dinosauriërs doden
Klein plankton herstelt traag na botsing met asteroïden die dinosauriërs doden Wat zijn de ideeën van het darwinisme en hoe verhouden ze zich tot sociaal darwinisme?
Wat zijn de ideeën van het darwinisme en hoe verhouden ze zich tot sociaal darwinisme?  Verlaagt CO2 de ozonlaag?
Verlaagt CO2 de ozonlaag?  780, 000 geëvacueerd in India voorafgaand aan grote cycloon
780, 000 geëvacueerd in India voorafgaand aan grote cycloon
Hoofdlijnen
- Wat kan glycolyse stoppen?
- Welke cel is langer dan de meeste cellen en bevat veel kernen?
- Effecten van de microscoop op Science
- Waar is een kernvirus van gemaakt?
- Een bacterieel stroomdiagram maken
- Een nieuwe ontdekking toont aan dat grote bloeiende planten 150 miljoen jaar ouder zijn dan eerder werd gedacht
- Waarom zijn aanpassingen bewijs van evolutie?
- Waarom geruchten zich snel verspreiden op sociale netwerken
- Wat is ventilatie in de menselijke biologie?
- Onderzoekers smeden nieuwe rekenhulpmiddelen om nauwkeuriger voorspellingen te doen van eiwitstructuren

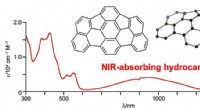
- Moleculaire ontwerpstrategie onthult bijna-infraroodabsorberende koolwaterstof
- Synchrotron onthult belangrijke informatie over het beroemde beeldhouwwerk van Paul Gauguin

- Machine-learning methode creëert een leerbare chemische grammatica om synthetiseerbare monomeren en polymeren te bouwen
- Voedingswetenschappers creëren nieuwe magnetische nanodeeltjes voor snelle screening van bestrijdingsmiddelenresiduen in groenten

 Verborgen figuren niet meer:Lego eert Women of NASA
Verborgen figuren niet meer:Lego eert Women of NASA Als je de oplossing langzaam afkoelt en suiker niet vestigt, is het koelt dat het is?
Als je de oplossing langzaam afkoelt en suiker niet vestigt, is het koelt dat het is?  Zijn katten de ‘kanarie in de kolenmijn’ als het gaat om de gevolgen van natuurbranden voor de menselijke gezondheid?
Zijn katten de ‘kanarie in de kolenmijn’ als het gaat om de gevolgen van natuurbranden voor de menselijke gezondheid?  Twee van de innerlijke planeten zijn?
Twee van de innerlijke planeten zijn?  Een watt elektrische energie is gelijk aan?
Een watt elektrische energie is gelijk aan?  Wat zijn enkele woorden om cellen a tot en met z te beschrijven?
Wat zijn enkele woorden om cellen a tot en met z te beschrijven?  Onderzoekers brengen de Orionnevel in kaart als nooit tevoren
Onderzoekers brengen de Orionnevel in kaart als nooit tevoren  Akoestische uitvinding verbetert echografie om toegang te krijgen tot afgesloten metalen ruimtes
Akoestische uitvinding verbetert echografie om toegang te krijgen tot afgesloten metalen ruimtes
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

