
Wetenschap
Wat zal het meest waarschijnlijk twee elektronen krijgen bij het vormen van een ionische binding?
Dit is waarom:
* Elektronenconfiguratie: Chalcogenen hebben zes valentie -elektronen (elektronen in hun buitenste schaal). Ze hebben nog twee elektronen nodig om een stabiele octetconfiguratie te bereiken, zoals de edelgassen.
* elektronegativiteit: Chalcogenen hebben een relatief hoge elektronegativiteit, wat betekent dat ze een sterke aantrekkingskracht hebben op elektronen.
* ionische binding: Wanneer ze binden met metalen, krijgen ze gemakkelijk twee elektronen en vormen ze een anion met een -2 lading. Dit creëert een stabiele ionische binding.
Voorbeelden van chalcogenen die twee elektronen krijgen:
* zuurstof (O): Vormt oxide -ionen (o²⁻)
* zwavel (s): Vormt sulfide -ionen (s²⁻)
* selenium (SE): Vormt selenide -ionen (se²⁻)
* tellurium (TE): Vormen telluride -ionen (te²⁻)
Laat het me weten als je andere voorbeelden wilt verkennen of meer wilt leren over ionische binding!
 Terwijl we ons fixeren op het coronavirus, De aarde raast op een catastrofe af die erger is dan het uitsterven van de dinosauriërs
Terwijl we ons fixeren op het coronavirus, De aarde raast op een catastrofe af die erger is dan het uitsterven van de dinosauriërs Onderzoek suggereert dat klimaatverandering planten bovengronds meer treft dan onder de grond
Onderzoek suggereert dat klimaatverandering planten bovengronds meer treft dan onder de grond Vuur, rook, warmte, droogte:hoe klimaatverandering je volgende glas California Cabernet kan bederven
Vuur, rook, warmte, droogte:hoe klimaatverandering je volgende glas California Cabernet kan bederven Smog geteisterd Warschau om toegang met de auto te beperken, kolen verwarming
Smog geteisterd Warschau om toegang met de auto te beperken, kolen verwarming Open Ocean Feiten voor kinderen
Open Ocean Feiten voor kinderen
Hoofdlijnen
- Wat zijn de microscopische haarachtige projecties die worden gevonden in cellen langs het grootste deel van de luchtwegen?
- Genzoekers ontdekken atypische genen die meerdere waardevolle eigenschappen van sojabonen controleren
- Hoe wordt DNA gevisualiseerd met behulp van gelelektroforese?
- Vaarwel 'R'-regel? Oesterziektetest kan schelpdieren veiliger maken
- Waar deed James Watson zijn werk aan het structuuron -DNA?
- Elements of Nucleic Acids
- Wat is het verschil tussen dieren- en bacteriecellen?
- Wat is de naam die cellen van planten beschermt?
- Hoe ons album met opnames van vogelgezang naar #2 in de ARIA-hitlijsten schoot
- IJsbestendige coating voor grote constructies is afhankelijk van een prachtige demonstratie van mechanica

- Nieuw kunstmatig enzym breekt taaie, houtachtige lignine af:onderzoek toont belofte voor de ontwikkeling van een nieuwe hernieuwbare energiebron

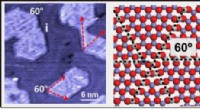
- Atomaire defectlijnen onderdrukken deactivering van ijzeroxidekatalysatoren
- Inheemse Nieuw-Zeelandse boom doet pijn

- Op zoek naar de zee, en bacteriële gevechten, voor nieuwe antibiotica

 Verloren productiviteit tot March Madness een echt fenomeen, studie vondsten
Verloren productiviteit tot March Madness een echt fenomeen, studie vondsten Kleine voetafdrukken, grote ontdekking:reptielensporen oudste ooit gevonden in Grand Canyon
Kleine voetafdrukken, grote ontdekking:reptielensporen oudste ooit gevonden in Grand Canyon Wat zijn de sterke en zwakke punten van theorie -evolutie?
Wat zijn de sterke en zwakke punten van theorie -evolutie?  Geloof het etiket niet - doorspoelbare doekjes verstoppen riolen
Geloof het etiket niet - doorspoelbare doekjes verstoppen riolen De vertrouwensbarrière overwinnen bij metingen van kernwapenverificatie
De vertrouwensbarrière overwinnen bij metingen van kernwapenverificatie Astronomen ontdekken sterrenstelsels die als een uurwerk ronddraaien
Astronomen ontdekken sterrenstelsels die als een uurwerk ronddraaien Onderzoekers ontcijferen elektrische geleidbaarheid in gedoteerde organische halfgeleiders
Onderzoekers ontcijferen elektrische geleidbaarheid in gedoteerde organische halfgeleiders Orkaan Ida zou de duurste weerramp kunnen worden:UN
Orkaan Ida zou de duurste weerramp kunnen worden:UN
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

